CAR-Т-клетки уменьшают фиброз печени у мышей
Фиброз печени — ключевой фактор смертности при метаболически ассоциированном стеатогепатите (МАСГ). Поэтому воздействие на клетки печени, производящие избыточное количество коллагена, может оказать терапевтический эффект. Исследователи из США и Швеции разработали подход к лечению фиброза печени с помощью CAR-Т-клеток, нацеленных на фиброгенные звездчатые клетки. Эти CAR-Т-клетки создаются непосредственно в организме и через некоторое время исчезают, что обеспечивает безопасность. В экспериментах на мышах с МАСГ, который вызывали высококалорийной диетой, CAR-Т-клетки уменьшили проявления фиброза и восстановили функцию печени.
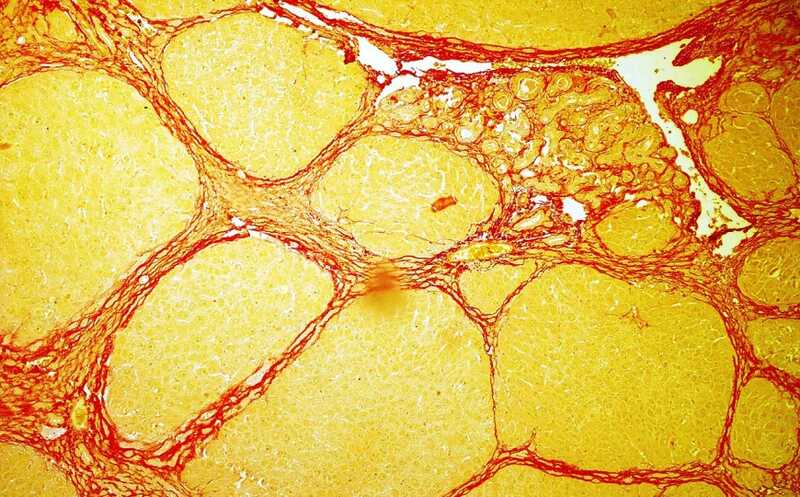
Печень крысы, окрашенная Sirius Red; отложения коллагена имеют красный цвет
Credit:
Метаболически ассоциированный стеатогепатит (МАСГ) — тяжелая форма метаболически ассоциированной жировой болезни печени (МАЖБП), которая развивается у 20% пациентов с этим диагнозом. МАСГ ассоциирован с повышенными рисками фиброза, цирроза и рака. Фиброз при МАСГ, в свою очередь, связан с прогрессированием заболевания и ухудшением прогноза; он является ключевым фактором смертности, поскольку существенно ухудшает функцию печени. Следовательно, развитие болезни может замедлить или обратить воздействие на фиброгенные звездчатые клетки, количество которых возрастает в больной печени. Однако одобренных антифибротических методов лечения при этом диагнозе до сих пор не существует.
Авторы статьи в Science Translational Medicine использовали для этого CAR-Т-клетки и продемонстрировали их действие на мышиной модели заболевания. МАСГ у мышей вызывала богатая углеводами, липидами и жирами «западная» диета.
В качестве мишени, на которую нацелен химерный антигенный рецептор (CAR), выбрали альфа-субъединицу белка активации фибробластов (FAP). Этот белок экспрессируется на поверхности звездчатых клеток и давно рассматривается как перспективная мишень для воздействия на них. Авторы подтвердили, что экспрессия FAP как при человеческом, так и при мышином МАСГ специфична для фиброгенных, но не для нормальных, покоящихся звездчатых клеток.
CAR-Т-клетки создавались in vivo, то есть в организме животного. Мышам с МАСГ вводили липидные наночастицы, взаимодействующие с поверхностным белком лимфоцитов CD5. Эти наночастицы избирательно доставляли в Т-клетки генетическую конструкцию, кодирующую анти-FAP CAR.
При таком подходе популяция CAR-Т-клеток в организме присутствует непродолжительное время (около четырех недель) и затем исчезает, что является преимуществом. Обычные CAR T-клетки, созданные вне организма, чаще всего с помощью лентивирусных векторов, после инфузии в кровь сохраняются в организме длительное время и могут чрезмерно сильно повреждать здоровые клетки.
В 2022 году эта же группа исследователей показалв, что созданные in vivo CAR-Т-клетки, нацеленные на FAP, препятствуют развитию фиброза сердца у мышей.
Чтобы проанализировать влияние анти-FAP CAR Т-клеток на мышиный МАСГ, авторы использовали проточную цитометрию, морфометрию с окрашиванием Sirius Red (азокрасителем для наблюдения за уровнем фиброза в тканях), цифровой патологический анализ и РНК-секвенирование единичных ядер.
CAR Т-клетки снижали количество экспрессирующих FAP профиброгенных клеток. Истощение этой популяции уменьшило фиброз печени и восстановило функции этого органа у мышей. CAR Т-терапия также модулировала иммунные клетки, эндотелиальные клетки и гепатоциты, уменьшая признаки воспаления и восстанавливая гомеостаз печени. Животные хорошо переносили терапию.
Интересно, что секвенирование РНК единичных ядер показало рост количества сенесцентных звездчатых клеток печени как у мышей с МАСГ, получавших CAR Т-клетки, так и у мышей без заболевания на здоровой диете.
Можно предположить, что лечение CAR Т-клетками окажется успешной стратегией контроля МАСГ и других фиброзных заболеваний печени, причем не только за счет уменьшения фиброзных явлений, но и за счет косвенного воздействия на другие типы клеток.
Утечка митохондриальной РНК и активация РНК-сенсинга при сенесценции клеток
Источник
Chittampalli N. Yashaswini, et al. Anti-FAP CAR T cells produced in vivo reduce fibrosis and restore liver homeostasis in metabolic dysfunction–associated steatohepatitis // Science Translational Medicine. 21 Jan 2026. Vol 18, Issue 833. DOI: 10.1126/scitranslmed.adx0368


 Меню
Меню





 Все темы
Все темы




 0
0











