Химерный белок ZFTA–RELA запускает опухолевый процесс через образование биомолекулярных конденсатов
Для агрессивной опухоли головного мозга — эпендимомы — характерно образование химерного белка ZFTA-RELA (ZR). Авторы статьи в Nature Cell Biology показали, как ZR способствует развитию этого заболевания. Химерный белок имеет в своем составе неупорядоченные области, которые позволяют ему формировать динамичные биомолекулярные конденсаты в ядре. Это помогает ZR рекрутировать белки, вовлеченные в транскрипцию, к онкогенам. Авторы конструировали белки, в которых неупорядоченные области принадлежали другим белкам, формирующим конденсаты, кроме RELA. И даже в этом случае химерные белки запускали экспрессию онкогенов и инициировали опухолеобразование.
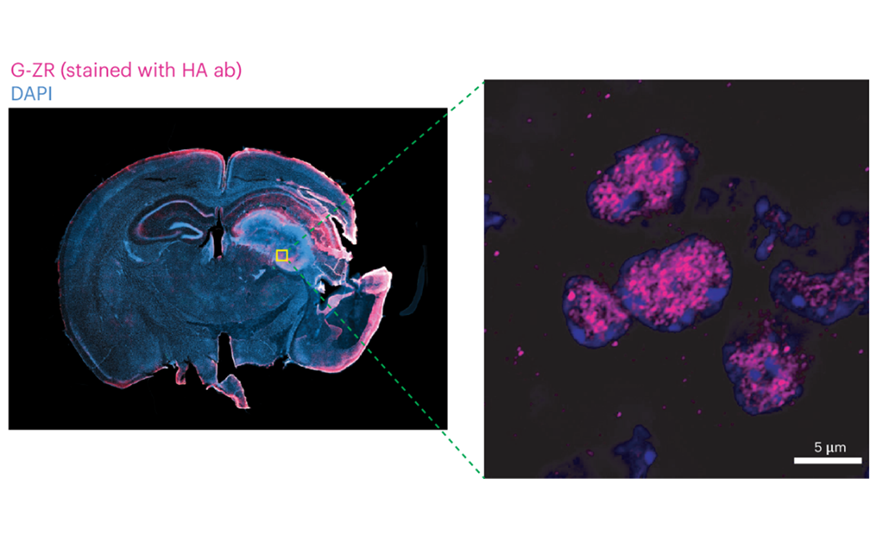
Credit:
Arabzade A., et al. // Nat Cell Biol (2025), DOI: 10.1038/s41556-025-01745-3
Эпендимома — третья по распространенности опухоль головного мозга у детей, которая берет начало из эпендимоцитов. Для многих эпендимом характерно слияние гена ZFTA с геном RELA с образованием химерного белка (ZR). Такие эпендимомы связаны с плохим прогнозом и устойчивы к существующим методам лечения. Одной из первых стадий развития опухоли является связывание ZR с ДНК с помощью доменов «цинковый палец» ZFTA. ZR рекрутирует белки, вовлеченные в транскрипцию (BRD4, EP300, MED1 и РНК-полимерза II), к онкогенам. Однако оставался неясен молекулярный механизм действия ZR. Ученые из Детской исследовательской больницы Св. Иуды Фаддея в Мемфисе и коллабораторы проанализировали молекулярные и биофизические свойства ZR, а также других слитых с ZFTA химерных онкопротеинов.
Методом микроскопии сверхвысокого разрешения авторы показали, что ZR образует четкие точки в ядре, в то время как его отдельные части демонстрируют диффузное распределение; также удалось заснять слияние двух конденсатов ZR в один. Методом FRAP (fluorescence recovery after photobleaching) авторы показали, что конденсаты больше всего напоминали жидкость и могли динамично изменяться. Так авторы доказали, что ZR может формировать динамические жидкие биомолекулярные конденсаты.
Изучение связи конденсатов с активацией онкогенов осуществляли методом иммунофлуоресценции в нейральных стволовых клетках (NSC). Авторы обнаружили, что белки MED1, BRD4 и РНК-полимерза II колокализованы с конденсатами ZR. В местах активной транскрипции онкогенов NOTCH1 и CCND1 (мишеней ZR) было значительно больше конденсатов ZR. Из этого следует, что конденсаты ZR связаны с активной транскрипцией, их становится больше в ключевых сайтах экспрессии онкогенов.
На следующем этапе ученые с помощью биоинформатического анализа определили, какая часть ZR отвечает за образование конденсатов. Они предсказали местоположение трех неупорядоченных областей (IDR) в последовательности ZR. Методом CRISPR/Cas9 исследователи создали серию мутантов ZR с делециями каждой из трех предсказанных IDR (ΔIDR1, ΔIDR2, ΔIDR3). По-видимому, IDR3 (расположен на C-конце RELA) играет самую важную роль в формировании конденсатов. В IDR3 заменили 25%, 50% и 75% аминокислот, важных для конденсации (пролин, аланин, глутамин), на отрицательно заряженные аминокислоты (аспарагиновая и глутаминовая кислоты), создав таким образом мутантов 25DE, 50DE и 75DE, у которых постепенно уменьшалось количество и размеры конденсатов (мутант 75DE был полностью диффузным). Так, очищенный пептид, соответствующий IDR3, мог спонтанно формировать конденсаты, а его мутировавший вариант 75DE — нет. Это подтверждает, что IDR3 является ключевым для фазового разделения и образования конденсатов. Используя метод CUT&RUN, авторы показали, что мутанты ZR-ΔIDR3 могли слабо связываться с ДНК, но теряли способность привлекать MED1, BRD4 и РНК полимеразу II к своим целевым сайтам связывания.
Мышиные NSC, стабильно экспрессирующие ZR-ΔIDR3, не образовывали опухоли при инъекции мышам по сравнению с клетками, стабильно экспрессирующими немутировавший ZR. Другие мутанты, у которых сохранялся некоторый процент активности IDR3, индуцировали образование опухолей, но позже и в меньшем количестве. Следовательно, нарушение способности к образованию конденсатов «выключает» онкогенность ZR. Способность ZFTA связывать ДНК также была необходима для формирования конденсатов на хроматине, экспрессии онкогенов и опухолеобразования.
На следующем этапе авторы определили, является ли этот механизм общим для всех химерных белков с ZFTA. Для этого применили машинное обучение. Модель по аминокислотным последовательностям предсказала, что все проанализированные химерные белки с ZFTA в составе должны образовывать конденсаты.
Для экспериментальной проверки авторы создали другие варианты химер ZFTA (с MAML2, MAML3, NCOA1, NCOA2) и экспрессировали в их клетках NSC. Микроскопия подтвердила, что все варианты химер формировали конденсаты в ядре.
В конце авторы доказали, что достаточно предоставить химерам ZFTA способность к образованию конденсатов, чтобы такие белки способствовали опухолеобразованию. Они заменили IDR3 в ZR на IDR от других белков с известной способностью к образованию конденсатов (FUS, EWS, NUP98). Синтетические химеры успешно формировали конденсаты, активировали онкогенную программу транскрипции и инициировали опухоли у мышей.
Исследование вносит вклад в понимание молекулярных основ эпендимом и раскрывает связи между структурой белка, регуляцией транскрипции и ростом опухоли. Открываются новые возможности для терапии, поскольку химерные белки являются сложными мишенями и, как отмечает один из авторов статьи Ричард Криваки: «Вместо того, чтобы сосредотачиваться на химерном белке, теперь мы можем начать идентифицировать его партнеров в конденсатах, изучать, какие из них необходимы для образования опухоли, и воздействовать на них».
Индивидуальные опухолевые органоиды предсказывают реакцию пациентов на терапию рака мозга
Источники:
Arabzade A., et al. Synthetic ZFTA fusions pinpoint disordered protein domain acquisition as a mechanism of brain tumorigenesis. // Nat Cell Biol (2025), published online 27 August 2025. DOI: 10.1038/s41556-025-01745-3
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0










