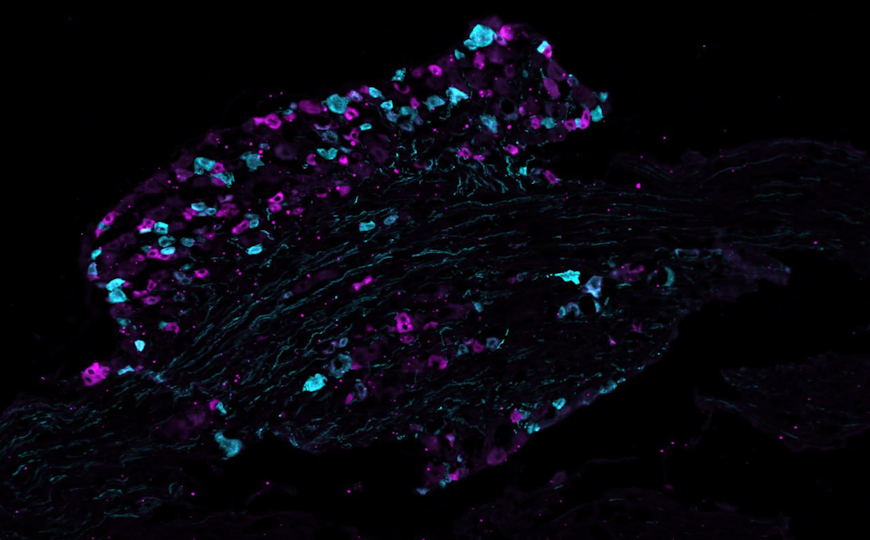
Клональная архитектура опухоли Вильмса может маскировать мутационную нагрузку
Секвенирование опухоли Вильмса — детского рака почки — часто демонстрирует парадокс: необъяснимо низкую мутационную нагрузку, иногда ниже, чем в нормальных тканях. Авторы статьи в Nature Communications, показали, что тотальное секвенирование может «не замечать» мутации в опухолях этого типа, если они присутствуют в небольших клеточных популяциях.
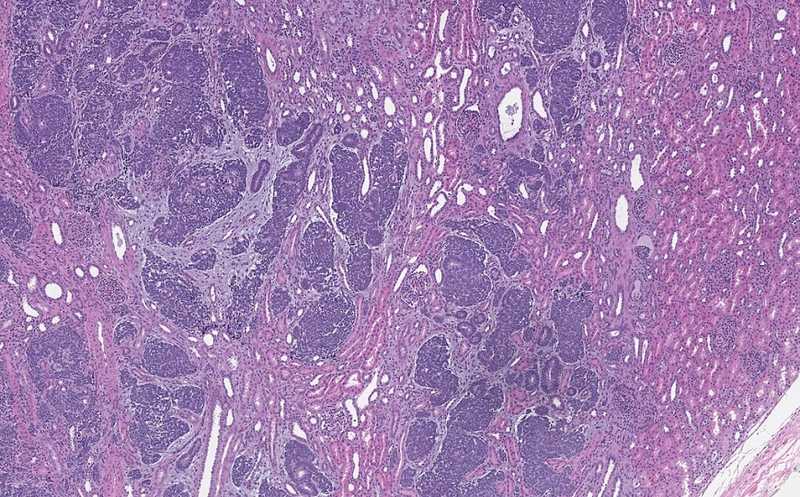
Принято считать, что злокачественные опухоли у детей имеют меньше мутаций. Предполагали даже, что у некоторых из них мутационная нагрузка ниже, чем в здоровой ткани, из которой они развились. Международная группа ученых, статья которых опубликована в Nature Communications, исследовала этот парадокс на примере детской опухоли почки, нефробластомы (опухоль Вильмса). Глубокое секвенирование РНК и ДНК и методы молекулярной эволюции показали, что мутаций в опухолях Вильмса в действительности не так уж мало. Прежние результаты были артефактом, вызванным клональной архитектурой опухоли.
Опухолевая мутационная нагрузка (tumour mutational burden, TMB) — это общее число соматических мутаций в определенной области генома опухоли: важный показатель, который отражает фундаментальную биологию раковой опухоли и в то же время ценен для клинической практики. Большое число мутаций в опухоли соответствует разнообразию неоантигенов и служит предиктором успеха иммунотерапии, вероятности развития резистентности и прогрессирования рака до более поздних стадий.
Исследования раковых опухолей детского возраста ранее демонстрировали в среднем сниженную мутационную нагрузку. Более того, в здоровой соответствующей ткани человека того же возраста мутаций могло быть даже больше. Это парадоксально, ведь злокачественное перерождение по определению ассоциировано с большей скоростью мутаций.
Авторы новой статьи анализировали образцы опухоли Вильмса (нефробластомы). Эта агрессивная эмбриональная опухоль происходит из развивающихся тканей почек. Опухоль Вильмса — самое распространенное злокачественное новообразование мочеполового тракта у детей, которое обычно развивается в возрасте до 5 лет с одинаковой частотой у мальчиков и девочек.
Исследователи оценили истинную мутационную нагрузку в опухолях почки и здоровой ткани. Оказалось, что стандартные методы секвенирования приводят к систематической ошибке — значительно заниженному числу мутаций.
Для начала исследователи исключили роль погрешности конкретных методик секвенирования. Их проверили на клетках почечной карциномы взрослых. Тотальное полногеномное секвенирование (bulk whole-genome sequencing) и дуплексное секвенирование, то есть секвенирование обеих нитей ДНК, которое повышает точность и позволяет выявлять низкочастотные мутации, показали хорошую корреляцию. Однако на образцах опухолей Вильмса результаты двух методов резко разошлись: дуплексное секвенирование детектировало в несколько раз больше новых мутаций, и их было больше, чем в нормальной ткани почки. Предстояло найти специфические биологические причины «парадокса гипомутированной опухоли» у детей.
Тотальное секвенирование детектирует широко представленные в ткани мутации, общие для большинства клеток, но пропускает индивидуальные, присущие отдельным клеткам и небольшим популяциям. Можно было предположить, что в опухолях маленьких детей популяции клеток с той или иной мутацией малочисленны.
Чтобы подтвердить это предположение, авторы статьи реконструировали эволюцию (то есть историю накопления мутаций и изменений клеток) для опухолей Вильмса с большим и малым числом мутаций, определенным стандартными методами. Для образцов двух пациентов удалось получить органоиды из раковых и окружающих опухоль нормальных тканей. В этом случае эволюция опухоли была описана на уровне отдельных клеток. Остальные образцы изучили с помощью сэмплирования (отобрали с помощью лазерной микродиссекции десятки биопсий примерно по 100 клеток).
Эти подходы выявили клональную архитектуру каждой опухоли, то есть ее гетерогенную внутреннюю структуру и межклеточные генетические различия. Хотя клетки опухоли «с низкой мутационной нагрузкой» происходили от общего «предка», они имели лишь 9–26 общих мутаций, а затем достаточно рано накапливали десятки и сотни собственных уникальных мутаций (то есть на самом деле мутационная нагрузка низкой не была). По всей видимости, они возникали у плода уже на первых месяцах беременности. Опухоли Вильмса с высокой мутационной нагрузкой развивались иначе: их клетки имели больше изначальных общих мутаций (которые легче обнаруживаются с помощью тотального секвенирования), а разнообразие они приобретали позднее.
Затем авторы проанализировали драйверные мутации — те, что приводят к росту опухоли и обеспечивают выживаемость злокачественных клеток. В гипермутированных опухолях было более одной драйверной мутации, в том числе в субклонах. Напротив, у «гипомутированных» опухолей не выявили собственных драйверных мутаций в субклонах, несмотря на детальный анализ ДНК, РНК и метилирования ДНК. Однако на «стволовом» отрезке развития одной из опухолей (до расхождения субпопуляций) описана мутация одного аллеля гена-онкосупрессора REST и инактивация второго. В опухолях еще трех младенцев обнаружили драйверную мутацию гена FOXR2, который недавно привлек внимание исследователей детского рака. В результате перестройки гена он попал под управление другим промотором, что привело к гиперэкспрессии FOXR2, а также протоонкогена MYCN. Возможно, перестройка FOXR2 характеризует определенный вариант опухоли Вильмса у младенцев.
Авторы предполагают, что если одной драйверной мутации достаточно для распространения опухоли, то формируется клональная архитектура с длинным стволом и заниженной стандартными методами мутационной нагрузкой. Если же требуется несколько драйверных мутаций, то уже на раннем этапе могут возникнуть субпопуляции, более обширные и лучше детектируемые.
Результаты исследования говорят о том, что стандартные методики секвенирования могут давать неточные оценки мутационной нагрузки в опухолях. Это касается не только нефробластомы, но и других новообразований с необычной траекторией клеточного развития. Такие факторы необходимо учитывать в клинической практике онколога.
Источник
Lee-Six, H., et al. High resolution clonal architecture of hypomutated Wilms tumours // Nature Communications (2025), 16, 4647. DOI: 10.1038/s41467-025-59854-4


 Меню
Меню





 Все темы
Все темы




 0
0