МД-2025. ВИЧ-инфекция: диагностика, эпидемиология, профилактика
Как научное сообщество пытается «обогнать» рекомбинирующий вирус иммунодефицита человека, какие меры позволят улучшить своевременную диагностику вертикальной передачи ВИЧ, в чем состоит двойственность транскриптомного ответа иммунных клеток на инфекцию, и как повлияют на подход к диагностике длительно действующие препараты против ВИЧ? Эти и многие другие вопросы обсудили на секции «ВИЧ-инфекция: диагностика, эпидемиология, профилактика».

Андрей Константинов
Первым в секции прозвучал доклад Анастасии Антоновой, к.б.н., с.н.с. ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи», посвященный рекомбинации ВИЧ.
ВИЧ представляет собой глобальную проблему общественного здравоохранения. В мире около 40,8 млн человек живут с ВИЧ, из них 927 тысяч — в России. Основную проблему терапии представляют высокое генетическое разнообразие вируса и мутации, связанные с лекарственной устойчивостью. Рекомбинация способствует объединению таких мутаций в вирусном геноме, следовательно, для преодоления устойчивости важно понимать сам механизм рекомбинации и его особенности.
Рекомбинация происходит по механизму смены матрицы (template switch) и начинается на стадии обратной транскрипции. Ключевое условие для нее — наличие коинфекции или суперинфекции вирусами разных генетических вариантов. Среди вариантов ВИЧ выделяют циркулирующие рекомбинантные формы (CRF) и уникальные рекомбинанты. В первом случае вирус конкретного генотипа должен быть выявлен минимум у трех несвязанных пациентов.
Так, в странах Азии преобладает CRF01_AE, в Африке — CRF02_AG, на американском континенте — CRF07_BC. Для российской популяции характерен субсубтип A6, попавший в когорту потребителей инъекционных наркотиков в конце 90-х годов, и субтип B, распространявшийся среди мужчин, практикующих секс с мужчинами (МСМ). CRF02_AG проникла в РФ из Африки через страны Азии в 2000-х годах и теперь циркулирует, создавая новые рекомбинантные формы, например, выявляемую в Сибири CRF63_02A6.
Клиническое значение рекомбинантных форм ВИЧ-1, во-первых, состоит в повышенной патогенности и, вероятно, также более высокой трансмиссивности вируса.
Во-вторых, они осложняют задачу диагностики и мониторинга — их особенности важно учитывать при разработке тест-систем. По данным исследования, проведенного лабораторией вирусов лейкоза НИЦЭМ им. Н.Ф. Гамалеи, точки рекомбинации чаще встречаются в пределах pol — вирусного гена, кодирующего полипротеин, который затем разрезается на протеазу, обратную транскриптазу и интегразу (наиболее часто они располагаются именно в домене обратной транскриптазы). Также точки рекомбинации обнаруживаются по фланкам гена env, а в самом гене и в начале gag встречаются реже.
Наконец, рекомбинантные формы могут приобретать лекарственную устойчивость, которая делает антиретровирусную терапию (АРТ) неэффективной.
Как отвечает на этот вызов научное сообщество? В первую очередь — разработкой новых классов препаратов, новейшими из которых являются ингибиторы капсида. К ним относится, например, ленакапавир — пролонгированная инъекционная форма АРТ, которая показала 83% эффективность у пациентов с мультирезистентными штаммами ВИЧ. Анастасия Антонова подчеркивает, что длительность действия препарата важна еще и потому, что снижает стигматизацию — многие люди, живущие с ВИЧ, признают, что стесняются пить таблетки.
Другое направление включает генную терапию с помощью CRISPR или препараты широконейтрализующих антител. Развитие методов диагностики, для которого также важно понимать биологию ВИЧ-1, важно для молекулярного эпиднадзора.
Докладчица подытоживает: «Борьба с ВИЧ — это постоянная гонка между эволюцией вируса и достижениями науки. Понимание механизмов, подобных рекомбинации, дает нам инструменты для того, чтобы оказаться на шаг впереди».
Лариса Афонина, к.м.н., ФГБОУ ВО СЗГМУ им. И.И. Мечникова (Санкт-Петербург) рассказала о ранней диагностике ВИЧ у детей с перинатальным контактом. В начале выступления она подчеркнула, что будет говорить про ВИЧ у детей именно с позиции врача-клинициста.
В сентябре 2003 года вышел
приказ Минздрава №442 «Об утверждении учетных форм для регистрации детей, рожденных ВИЧ-инфицированными матерями». Сама же история педиатрической ВИЧ-инфекции, с которой в России и началось распространение ВИЧ, уходит корнями в 90-е. Первым случаем заражения стала так называемая элистинская трагедия (1982 год). Ребенок, зараженный вертикально, болел с первых месяцев и лечился в детской больнице Элисты, позднее другие инфицированные дети оттуда направлялись в стационары других городов. Из-за этого к началу 90-х годов было инфицировано 268 детей, у всех был ВИЧ-1 одного субтипа — G.
С 1996 года наблюдался резкий рост доли инфицированных в результате внутривенных инъекций психоактивных веществ, с 2002 года стали доминировать случаи вертикальной передачи — от ВИЧ-положительной матери ребенку, с 2016 года основным путем передачи стал гетеросексуальный.
Говоря о современной статистике, докладчица приводит данные о почти 9 тысячах детей (0-17 лет), из которых почти 92% заразились вертикально. «Впервые выявить у такого 17-летнего пациента ВИЧ означает, что 17 лет он не получал АРТ», — подчеркивает она.
Профилактика вертикальной передачи в России достигла существенных успехов — 97% беременных женщин с ВИЧ состоят на учете и получают АРТ. Однако для защиты ребенка от заражения необходимо начать терапию до зачатия, и сейчас это удается в 75% случаев.
По идее, с такой тенденцией мы должны ожидать, что у нас не останется детей, рожденных от ВИЧ-положительных женщин. И количество новых случаев ВИЧ у детей действительно снижается, равно как и возраст диагностирования.
Однако сейчас только треть новых случаев вертикальной передачи составляют дети, рожденные в этом году. Статистика, сопоставляющая год рождения и год установления диагноза ВИЧ-инфицированных детей, на 4 марта 2025 года, говорит о том, что каждый четвертый ребенок с вертикальной инфекцией ВИЧ родился от серонегативной матери. Особенный риск здесь представляет заражение матери в период грудного вскармливания — в таком случае ВИЧ вряд ли своевременно обнаружат и даже вряд ли направят женщину на анализ, если только не выявят у нее инфицированного полового партнера. Из этого следует вывод — подход к выявлению ВИЧ надо пересматривать, как уже пересматривали подход к терапии, и внедрять в скрининг методы молекулярной диагностики. Важно также совершенствовать их методы, чтобы снизить предел обнаружения вирусной РНК.
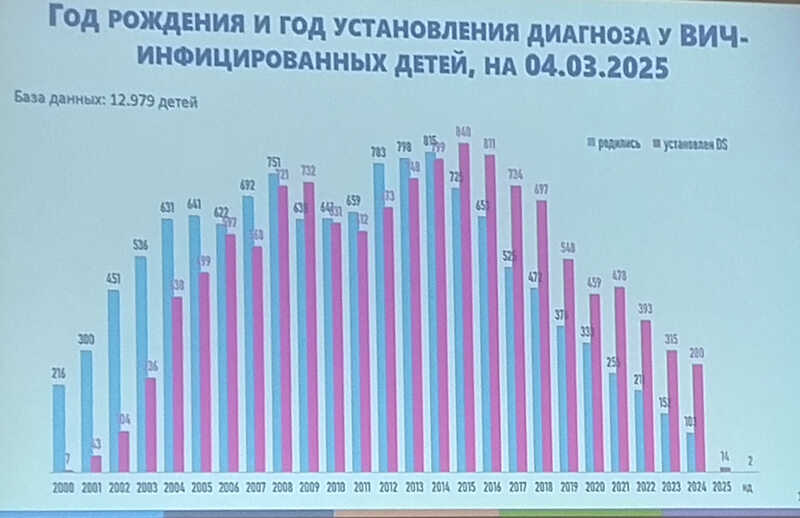
Из-за позднего выявления у детей с ВИЧ развивается выраженный иммунодефицит и высокая вирусная нагрузка — это объясняется тем, что они не получают своевременного лечения. Это, в свою очередь, выступает фактором быстрой смерти.
Раньше детям назначали АРТ в возрасте год и старше, сейчас этот возраст снизился до пяти месяцев, если ребенок родился от серопозитивной матери. В случае с рождением от серонегативной женщины ситуацию осложняет позднее выявление, из-за которого ребенку начнут терапию в возрасте старше года. Сейчас у 60% перинатально зараженных детей, получающих АРТ, не детектируется вирусная РНК, а показатели иммунного статуса достоверно лучше.
В завершение доклада Лариса Афонина подчеркнула, что терапия снижает стигматизацию и дискриминацию пациентов, но ключ к ее успеху — это раннее выявление ВИЧ. «Главная цель, — сказала она, — это не потерять ни одного ребенка». Докладчица заключает, что обследовать на ВИЧ надо не только беременных женщин, но и их половых партнеров, в том числе раскрывать их статус инфицирования, чтобы информировать женщину.
Андрей Шемшура, к.м.н., ГБУЗ КЦ ПБ СПИД МЗ (г. Краснодар) рассказал об актуальных трендах генетических характеристик ВИЧ в Краснодарском крае.
Тенденция к снижению внушает оптимизм, если смотреть на число новых случаев. При этом пораженность населения растет, — доля людей, живущих с ВИЧ, приближается к 1% населения, — но это связано со снижением смертности больных. Кроме того, увеличивается средний возраст выявления. С 31,4 лет в 1999 году он вырос до 42,2 лет в 2024 году. Иными словами, эпидемия ВИЧ «стареет» — это еще один признак ее стабилизации.
Также участилось выявление более ранних стадий. Число выявляемых ежегодно случаев инфекции, наоборот, снижается — это говорит о том, что либо уже всех выявили, либо они все вымерли. Еще одним подтверждением стабилизации можно считать, что ВИЧ чаще стали выявлять в острой стадии — то есть через несколько месяцев после заражения.
Динамика субтипов, которыми заражались жители Краснодарского края, отражает, что до 2010 года на этой территории циркулировал субтип A6. Со временем его удельный вес стал снижаться — сейчас относительно более распространенными становятся субтип B и CRF63, предположительно более вирулентный. Различные варианты субтипа А6 циркулируют в нескольких очагах.
Данные прежних лет, на которые также наложены данные 2025 года, равномерно вплетаются в эти очаги — раньше в когорте МСМ преобладал субтип B, теперь тем же путем передается и распространяется в этой когорте А6, теперь к ним добавился CRF63.

Нашей главной мерой, подчеркнул докладчик, является всеобщее обследование, которое обеспечит выявление, и не менее всеобщее лечение. Он привел спектр вирусологической эффективности первой линии АРТ в Краснодарском крае, сравнивая порог резистентности для разных препаратов. Эффективнее всего пока что действуют ингибиторы интегразы (97,9% успеха), суммарная эффективность достигла 88%. Однако 12% случаев все же представляют собой вирусологическую неудачу — в крови пациента на терапии сохраняется более 500 копий вирусной РНК на мл, в том числе это связано с перекрестными мутациями. Самое неприятное состоит в том, что начала возникать устойчивость и к ингибиторам интегразы. Актуальность проблемы лекарственной устойчивости состоит в том, что она повышает риск передачи резистентных штаммов и их распространения.
Андрей Шемшура и соавторы проанализировали вариабельность вирусного генома у отдельных людей с ВИЧ, оценивая ее по уровню несинонимичных замен. Исследование показало, что вариабильность генома внутри пациента начинает расти после прохождения острой стадии без АРТ. В 2025 году они отследили 12 случаев передачи резистентного ВИЧ, из которых 10 произошло через гетеросексуальный контакт, 1 — через гомосексуальный, и 1 приходился на вертикальный путь передачи. Половину из них составлял субтип А6, еще 5 — рекомбинант 63. Таким образом, частота передачи резистентности в Краснодарском крае составляет около 14%, и это ставит вопрос о введении систематического контроля.
Однако в целом реализация государственной стратегии по борьбе с ВИЧ идет успешно — растет охват людей с ВИЧ антиретровирусной терапией, снижается количество летальных исходов, увеличивается продолжительность жизни пациентов.
Следующий доклад представил Кирилл Елфимов, м.н.с. ФБУН Центра Вирусологии и Биотехнологии «Вектор» Роспотребнадзора (Кольцово, Новосибирская область). Темой доклада стал анализ транскриптомного профиля единичных мононуклеаров периферической крови в период острой стадии ВИЧ-инфекции.
Российские штаммы ВИЧ-1 имеют низкую представленность за пределами РФ, поэтому они изучены слабее, чем распространенные субтипы и CRF. Отдельный интерес представляет циркулирующая рекомбинантная форма CRF63_02A6.
Анализ единичных клеток, в частности, секвенирование их РНК (scRNA-seq) позволяет исследовать сложные клеточные популяции. Этот метод лег в основу изучения мононуклеаров периферической крови ВИЧ-положительных пациентов. В когорту вошли три человека с ВИЧ в острой фазе инфекции и три здоровых контроля. Криоконсервированные мононуклеары всех участников анализировали на платформе Chromium 10x Genomics.
Аннотация клеточных субпопуляций в зависимости от ВИЧ-статуса показала, что при инфицировании ВИЧ активируется хемотаксис и транспорт антигенов. При более подробном рассмотрении клеточной популяции становится ясно, что клетки однозначно экспрессируют положительные и отрицательные (в контексте прогноза для пациента) сигналы.
В центральных CD4+ Т-клетках памяти положительными сигналами стали гены электронтранспортной цепи (COX7B, UQCRB), экспрессия которых говорит о высокой потребности в энергии, и негативных регуляторов TGF-β (SMAD7, SKIL), подавляющих транскрипцию ВИЧ. Экспрессия CXCR4 увеличивает число чувствительных к ВИЧ клеток, повышение уровня FOSL2 ассоциировано со снижением защитного барьера слизистых оболочек, подавление экспрессии SKAP1 — c нарушением пролиферации. Поэтому такие сигналы в данном случае являются отрицательными.
Для центральных CD8+ T-клеток памяти в число положительных сигналов вошла экспрессия MHC-I и его защита от деградации, поскольку это противодействует репликации ВИЧ, а также формирование ядерных параспеклов при участии белка NEAT2 — они задерживают вирусные транскрипты. Отрицательными сигналами были высокая экспрессия рецептора интерлейкина IL21R, ассоциированная с большой вирусной нагрузкой, и снижение экспрессии HLA-C.
Положительными сигналами эффекторных CD8+ Т-клеток были низкий уровень ST6GAL1 — этот мембранный фермент ассоциирован с проникновением ВИЧ в клетку — и экспрессия супрессоров TGF-β.
Неклассические моноциты (CD14+ CD16+) в большей степени, чем классические, участвуют в противовирусном ответе. Положительные сигналы для них характеризовались повышенной экспрессией DUSP2, IER3 и PPARG — ингибиторам сигналинга NF-κB. AREG поддерживает целостность эпителиальных оболочек, продукт гена C15ORF48 индуцирует аутофагию и защиту от активных форм кислорода (АФК). В число отрицательных сигналов для неклассических моноцитов вошли экспрессия индукторов IL1B или CD69 — их высокий уровень может привести к истощению популяции CD4+ T-клеток, — факторы некроза и уже упомянутый CXCR4, повышающий уязвимость клеток к ВИЧ.
Анализ перестройки сигнальных путей показал, что общее число активных сигнальных путей во время острой ВИЧ-инфекции снижается, но количество уже используемых лигандов и рецепторов остается прежним. Некоторые сигнальные каскады, однако, особо активируются — в первую очередь хемотаксис (CCL), интерфероновый ответ II типа (IFN-II), воспалительный ответ (PAR), пролиферация и дифференцировка, а также индукция апоптоза (FASLG).
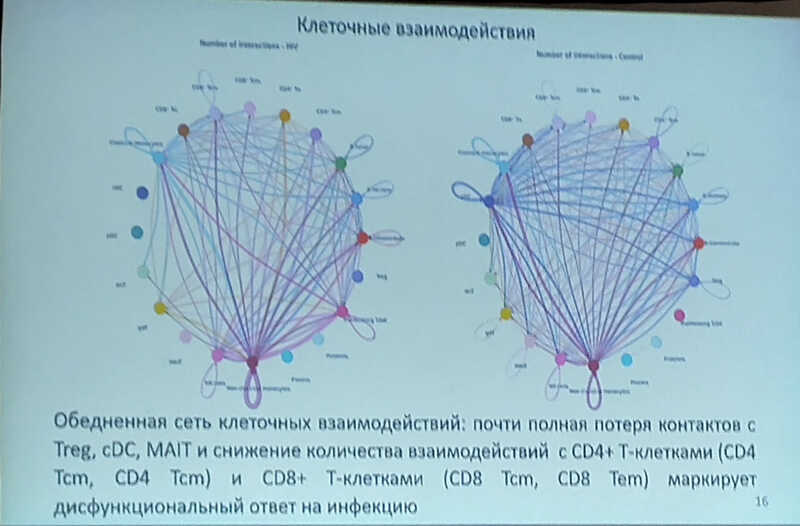
При этом ключевую роль в активации сигнальных путей, ассоциированных с ВИЧ-инфекцией, играют именно неклассические моноциты. Они способны контролировать число провирусных резервуаров. В этом контексте THBS1 выглядит геном, экспрессия которого имеет двойственную роль — его уровень ассоциирован как с положительными, так и отрицательными в контексте клинической картины сигналами.
Сеть клеточных взаимодействий при острой фазе ВИЧ-инфекции сильно обеднена — в ней почти полностью исчезают контакты с регуляторными Т-клетками и дендритными клетками, снижается число взаимодействий с CD4+ и CD8+ (как клетками памяти, так и эффекторными). Такое изменение маркирует дисфункциональный ответ на инфекцию.
Наконец, в антивирусных популяциях периферических мононуклеаров высоко экспрессируются гены CREM, SKIL и GPR132. CREM подавляет активность факторов, ассоциированных с прогрессией ВИЧ-инфекции, и его уровни повышены у элитных контроллеров. Ген SKIL, с одной стороны, снижает транскрипцию вирусных генов, а с другой, способен подавлять противовирусный ответ клеток. Докладчик выдвигает предположение, сделанное в ходе исследования: эти гены могут определять баланс между защитной реакцией и прогрессированием ВИЧ.
Это и стало основным выводом работы: ключевые иммунные субпопуляции демонстрируют дуалистический ответ, сочетающий повышенную экспрессию генов противовирусной защиты и генов, ассоциированных с прогрессией ВИЧ-инфекции.
Алексей Машарский (к.б.н., ФГБУ «НИИ гриппа им. А.А. Смородинцева») поделился опытом применения NGS для широкомасштабного мониторинга разнообразия субтипов и межсубтипических рекомбинантов ВИЧ-1 в регионах РФ.
В базе данных всем известной лаборатории Лос-Аламоса присутствует 366 полных нуклеотидных последовательностей ВИЧ-1. Существует также база RuHIV, содержащая около 400 полных геномов ВИЧ и специализирующаяся на выявлении мутаций, связанных с лекарственной устойчивостью. По сравнению с десятками тысяч для SARS-CoV-2 это немного. В 2000 году были опубликованы первые полные геномы российских штаммов ВИЧ. Чтобы полнее охарактеризовать характерные для РФ варианты, специалисты из НИИ гриппа решили увеличить количество секвенированных образцов.
Коллекция геномов должна отражать генетическое разнообразие и охватывать все доступные федеральные округа РФ. На текущий момент она охватывает шесть из них и содержит 9 436 образцов из 24 регионов, в том числе с территорий ДНР, ЛНР и Крыма. В основном образцы представляют собой замороженную плазму крови, взятой у людей с ВИЧ.
Для секвенирования ВИЧ нужна амплификация полноразмерного генома или набора перекрывающихся ампликонов. В исследовании, о котором идет речь, применяли второй подход — по словам докладчика, личный опыт использования показал, что он эффективнее.
В ходе анализа сотрудники НИИ гриппа секвенировали до полутора тысяч отдельных вирусных образцов за запуск. Сборка полного генома ВИЧ-1 осуществлялась при помощи метода
shiver — он заключается в картировании сырых прочтений на уже имеющиеся референсы разных субтипов параллельно со сборкой de novo. Глубина покрытия при таком объединении получается достаточно высокой, более 1000х.
Однако полногеномное секвенирование ВИЧ — довольно дорогая и не всегда экономически целесообразная задача. Поэтому к выявлению мутаций лекарственной устойчивости исследователи разработали более дешевый протокол мультиплексной ПЦР.
На данный момент проанализированы еще не все вошедшие в коллекцию образцы: полных геномов собрано 300, последовательности генов pol и env пролучены для 1888 образцов.
«Мы не получили никаких оригинальных результатов, — прокомментировал Алексей Машарский, — выявленная картина распределения генетических вариантов выглядит привычно». Анализ мутаций лекарственной устойчивости также не выявил резко неожиданных вариантов.

Проблемы, с которыми столкнулись специалисты в ходе данного исследования, связаны с переходом от секвенирования по Сэнгеру на NGS. Чтобы их преодолеть, необходима оптимизация качества сборки генома, а также разработка и внедрение методов анализа и валидации минорных вариантов. Остальные трудности связаны с необходимостью оптимизировать амплификацию методом ПЦР для подобного анализа, чтобы избавиться от артефактов в результатах. «Сейчас приходится балансировать между повышением чувствительности и снижением специфичности», — объяснил докладчик. Наконец, для масштабного продолжения работы необходима инфраструктура, которая позволит хранить образцы и структурированно накапливать собранную эпидемиологическую информацию.
Заключительный доклад в секции прочитал Феликс Урусов, к.б.н., ФГБУ «ЦСП» ФМБА России. Речь шла о препаратах пролонгированного действия как о новом тренде в лечении и профилактике ВИЧ. Основную трудность для этого направления представляет приверженность пациентов лечению. Препарат ленакапавир производит на сегодняшний день революцию, особенно в сфере доконтактной профилактики, поскольку клиренс позволяет применять его раз в 6 месяцев. Для профилактики он показал впечатляющие результаты — в группе под клиническим наблюдением пока не заразился никто. Полноценное применение в качестве средства терапии пока рассматривается, хотя данные об эффективности, полученные в ходе КИ, говорят о перспективности ленакапавира для лечения. Сейчас этот препарат назначают в сложных случаях.
Однако нет ничего идеального — у 14 из 72 участников исследования обнаружили мутации устойчивости к ленакапавиру, и у половины из этих людей стала детектироваться вирусная нагрузка. Все пациенты были инфицированы штаммами ВИЧ с множественной лекарственной устойчивостью. Поэтому необходимо разрабатывать новые препараты пролонгированного действия против ВИЧ.
В ЦСП ФМБА занимаются разработкой препаратов, действие которых основано на широконейтрализующих антителах. Ключевые эпитопы широконейтрализующих антител, обнаруженных в крови пациентов, легли в основу двух препаратов — КомбиМаб1 и КомбиМаб2. Они нацелены на разные области вирусного белка ENV. Последовательности, кодирующие антитела, доставляют в организм пациента с помощью аденоассоциированных вирусов (AAV9) — длительная экспрессия должна обеспечить протективный эффект.
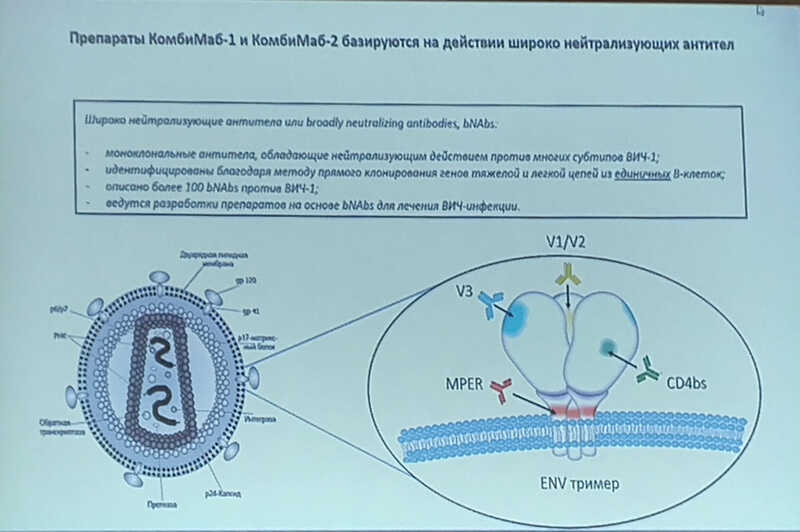
Сейчас проводятся исследования обоих препаратов на животных моделях, в том числе оценка длительности экспрессии антител в организме мышей. КомбиМаб2 показал несколько более продолжительную экспрессию, однако это зависит в том числе от конкретной линии мышей. В целом экспрессия широконейтрализующих антител сохранялась у большинства модельных животных спустя год после введения препарата.
Защитную эффективность КомбиМаб1 и КомбиМаб2 определяли в модели иммунодефицитных мышей, гуманизированных CD4+ T-клетками. Ключевыми параметрами оценки были количество CD4+ T-клеток и вирусная нагрузка. Оба препарата показали протективный эффект. Также проведены доклинические исследования безопасности КомбиМаб1, в которых было продемонстрировано отсутствие всех видов токсичности — острой, хронической, иммунной. Единственным нежелательным явлением стало местное раздражение в области инъекции, которое быстро проходило без дополнительных вмешательств. Исследования биораспределения показало, что AAV-вектор сохраняется в органах животных в течение 1,5 лет, обеспечивая поддержание экспрессии антител против ВИЧ.
Также Феликс Урусов рассказал о
клиническом испытании комбинированной терапии — ВИЧ-инфицированные пациенты одновременно получали препараты моноклональных широконейтрализующих антител (3BNC117 и 10-1074) и ленакапавир. После предварительного скрининга на чувствительность вируса к антителам в КИ набрали две группы по 10 человек. Группы отличались режимом дозирования антител, период наблюдения составил 6 месяцев. За это время у 18 из 20 участников вирусная нагрузка снизилась до менее чем 50 копий/мл, однако у двух других человек этого добиться не удалось.
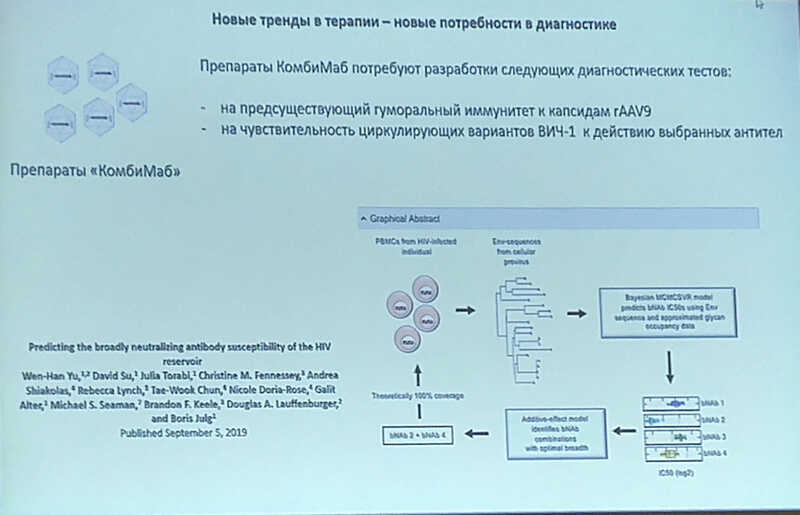
Прогнозируемые изменения в структуре диагностики ВИЧ-инфекции связаны с тем, как тренды в терапии повлияют на диагностические потребности. В связи с внедрением в практику препаратов пролонгированного действия можно ожидать уменьшения частоты тестирований на вирусную нагрузку и необходимости в разработке специфичных тестов. Для КомбиМаб1, например, потребуется определять лекарственную устойчивость вируса к антителам и оценивать гуморальный иммунитет пациента к капсиду AAV9.
Информация о докладчиках
Антонова Анастасия Александровна, к.б.н., ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи», г. Москва
Афонина Лариса Юрьевна, к.м.н., ФКУ «РКИБ» Минздрава России; ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России, г. Санкт-Петербург
Шемшура Андрей Борисович, к.м.н., ГБУЗ КЦ ПБ СПИД МЗ Краснодарского края, г. Краснодар
Елфимов Кирилл Артемович, ФБУН Центр Вирусологии и Биотехнологии «Вектор» Роспотребнадзора, р.п. Кольцово, Новосибирская область
Машарский Алексей Эльвинович, к.б.н., ФГБУ «НИИ гриппа им. А.А. Смородинцева» Минздрава России, г. Санкт-Петербург
Урусов Феликс Анатольевич, к.б.н., ФГБУ «ЦСП» ФМБА России, г. Москва


 Меню
Меню





 Все темы
Все темы



 0
0












