Мимик естественных киллеров поражает золотистый стафилококк внутри клетки
Золотистый стафилококк способен скрываться внутри клеток, в частости, остеобластов, чтобы избегать действия иммунитета. Исследователи из Китая получили мимик естественных киллеров на основе мезопористых наночастиц кремнезема. При контакте с зараженными клетками частицы разрушаются из-за высокого окислительно-восстановительного потенциала клетки, высвобождая перфорин и гранзим B. Перфорин проделывает отверстия в клеточной мембране, а гранзим B убивает бактерии. Активность наночастиц также привлекает внимание иммунной системы организма.
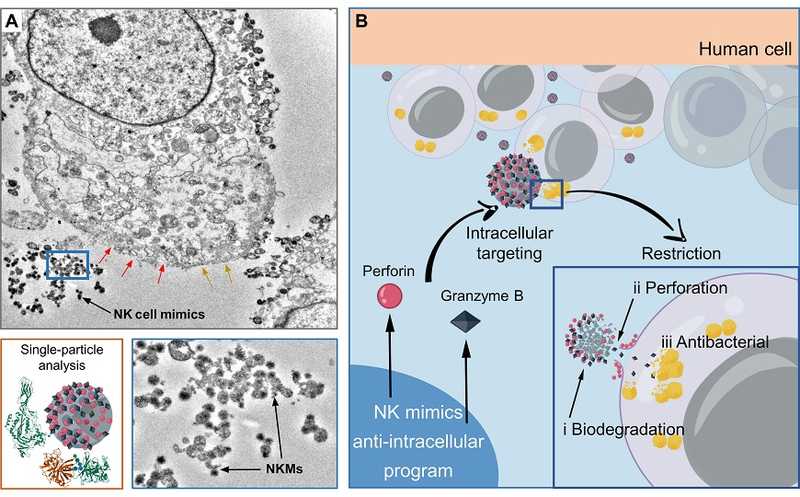
Распространение золотистого стафилококка (Staphylococcus aureus), резистентного к метициллину (MRSA), представляет собой угрозу общественному здравоохранению. Все чаще такой стафилококк становится устойчивым и к ванкомицину. MRSA колонизирует кожу и слизистую носа, вызывая остеомиелит, эндокардит, пневмонию и сепсис. S. aureus проникает внутрь клеток, которые невольно защищают его от антибиотиков и иммунитета. Уничтожение внутриклеточного золотистого стафилококка — важная клиническая задача. Исследователи из Китая использовали наночастицы, которые имитируют действие естественных киллеров и уничтожают стафилококк внутри клеток. Авторы назвали эти их мимиками естественных киллеров (NK cell mimics, NKM).
Сначала исследователи продемонстрировали способность S. aureus заражать остеобласты. Для этого они проанализировали образцы костей пациентов с хронической инфекцией S. aureus. Бактерии визуализировали в остеобластах (в цитозоле), причем они почти не реагировали на ванкомицин.
Потом авторы подняли вопрос, как можно отличить зараженные и незараженные клетки. РНК-секвенирование показало значительные изменения в метаболизме NAD: сильнее экспрессировались гены синтеза NAD (NAPRT и IDO), слабее — гены деградации NAD (NNMT и PAPR). Изменяется окислительно-восстановительный статус зараженной клетки. Окислительно-восстановительный потенциал в основном определяется парами GSH/GSSG, NADH/NAD+ и NADPH/NADP+. Эти соотношения выше в инфицированных клетках, что отличает их от неинфицированных, и это можно использовать для разработки терапии.
Авторы создали NKM, которые активируются только при распознавании зараженных клеток и имитируют действие естественных киллеров. Для этого за основу взяли дендритные мезопористые наночастицы кремнезема с дисульфидными связями, модифицированные полиэтиленгликолем. В поры загрузили перфорин и гранзим B. Сами по себе наночастицы не были цитотоксичными для здоровых клеток. При контакте NKM с зараженной клеткой связи —S—S— разрушаются из-за высокого окислительно-восстановительного потенциала клетки, выпуская перфорин и гранзим B. Перфорин проделывает отверстия в клеточной мембране, а гранзим B убивает бактерии. Так действуют и естественные киллеры.
Чтобы проверить работу NKM, наночастицы инкубировали с зараженными остеобластами. Количество бактерий значительно снизилось. NKM действовали также на зараженные макрофаги, нейтрофилы и стромальные клетки костного мозга и были эффективнее, чем высокие дозы рифампицина. При этом ни NKM, ни супернатант после разрушения частиц не действовали на здоровые клетки даже в дозах выше терапевтических.
РНК-секвенирование зараженных остеобластов после лечения NKM показало значительное изменение транскриптома клеток. Авторы предположили, что это стимулирует T-клетки и естественные киллеры, то есть клеточный иммунный ответ организма. Также воздействие NKM повышает уровни хемокинов и цитокинов (GM-CSF, IL-6 и TNF-α), которые могут рекрутировать макрофаги и активировать T-лимфоциты. То есть NKM не только сами убивают внутриклеточные бактерии, как естественные киллеры, но и усиливают антибактериальный иммунный ответ.
Безопасность NKM для организма проверили на мышах. Ни через неделю, ни через месяц авторы не выявили изменений в параметрах крови и основных органов. У мышей с остеомиелитом NKM собирались в пораженных тканях через 24 часа после введения. Более того, NKM облегчали течение инфекции. Они уменьшали количество бактерий в костном мозге бедренной кости и лакуно-каналикулярной сети остеоцитов. Частицы активируют естественные киллеры и способствуют созреванию дендритных клеток, а также T-клеточному ответу. При этом терапия не повреждает сердце, легкие, печень, почки, селезенку или кости и не влияет на массу тела мыши.
У стафилококка, резистентного к большим дозам антибиотика, есть альтернативный механизм деления
Источник:
Min Ge, et al. A natural killer cell mimic against intracellular pathogen infections // Science Advances (2024), published October 30, 2024, DOI: 10.1126/sciadv.adp3976


 Меню
Меню





 Все темы
Все темы




 0
0










