Моноклональные антитела препятствуют инфицированию вирусом Эпштейна – Барр
Американские исследователи разработали моноклональные антитела, нацеленные на различные участки вируса Эпштейна – Барр (ВЭБ), с которым связано развитие тяжелых заболеваний, в том числе онкологических. Лицензированной вакцины против ВЭБ не существует. При тестировании на клетках человека моноклональные антитела блокировали слияние вирусной оболочки с мембраной клетки. В экспериментах на мышах одно из антител обеспечило почти полную защиту от инфекции ВЭБ и препятствовало развитию лимфомы. Кроме того, ученые обнаружили структуры в оболочке вируса, которые могут стать потенциальными мишенями при разработке вакцины..
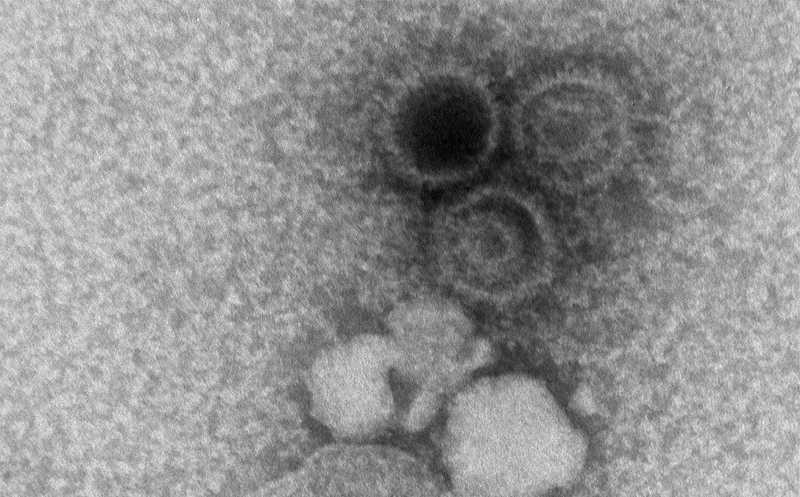
Вирус Эпштейна – Барр (ВЭБ) широко распространен во всем мире. В США, по данным Национального центра инфекционных заболеваний, около 90% взрослых людей служат носителями ВЭБ, причем заражение происходит еще в детском возрасте. У здорового человека инфекция протекает, как правило, бессимптомно, но в некоторых случаях может стать причиной мононуклеоза, а также онкологических (лимфом Ходжкина и Беркитта, назофарингеальной карциномы, рака желудка) и аутоиммунных (рассеянного склероза, системной красной волчанки, ревматоидного артрита) заболеваний. Наибольшему риску их развития подвергаются люди с иммунодефицитом. Специфической профилактики заражения ВЭБ пока не существует.
Ученые из Национального института аллергии и инфекционных болезней (США) в сотрудничестве с исследователями из Армейского исследовательского института Уолтера Рида разработали моноклональные антитела к ВЭБ, которые могут снизить вероятность развития инфекции. Результаты исследования опубликованы в Immunity.
ВЭБ — двуцепочечный ДНК-вирус, относящийся к семейству вирусов герпеса человека. Проникновению вириона в клетку предшествует слияние оболочки вируса с мембраной клетки. В этом процессе участвует гликопротеины gH и gL оболочки ВЭБ. Предыдущие исследования показали, что блокирование этих молекул антителами препятствует развитию инфекции. Ученые получили несколько групп моноклональных антител против gH/gL из В-клеток здоровых доноров. Эксперименты показали, что антитела связывались с оболочкой вируса и эффективно блокировали взаимодействие вируса с мембраной В-клеток и эпителиальных клеток. Далее с помощью рентгеновской кристаллографии была изучена структура полученных комплексов антиген-антитело. Выяснилось, что гликопротеины имеют несколько участков, с которыми возможно связывание различных антител. Интересно, что некоторые из эпитопов ВЭБ оказались схожими с эпитопами других вирусов — вируса ветряной оспы и цитомегаловируса. Авторы работы предполагают, что данные участки могут быть общими мишенями для связывания антител.
Затем исследователи изучили эффективность моноклональных антител на гуманизированных мышах, которым были трансплантированы гемопоэтические стволовые клетки человека. Животных заражали ВЭБ и вводили антитела. Результаты анализов показали, что у мышей, получавших антитела, уровень ДНК вируса в крови был меньше, чем у мышей контрольной группы. Наиболее эффективным антителом оказалось mAb 769B10. Животные, которым его вводили, имели наибольшую выживаемость (60%). Затем было проведено исследование печени, легких и селезенки мышей. У животных, получавших антитела 769B10, значительных поражений органов выявлено не было. Кроме того, признаков развития лимфом у них также не наблюдалось. Результаты гибридизации in situ показали, что у мышей, которым вводили антитела, содержание вируса в тканях было значительно ниже, чем у контрольной группы.
Авторы считают, что использование моноклональных антител против гликопротеинов оболочки вируса Эпштейна – Барр может снизить вероятность инфицирования клеток. Кроме того, участки, обнаруженные в оболочке вируса, могут стать потенциальными мишенями для вакцины. Ученые надеются, что с помощью полученных данных удастся разработать профилактику заражения ВЭБ.
Источник
Chen WH, et al. Epstein-Barr virus gH/gL has multiple sites of vulnerability for virus neutralization and fusion inhibition. Immunity. 2022 Oct 26:S1074-7613(22)00544-1. DOI: 10.1016/j.immuni.2022.10.003


 Меню
Меню





 Все темы
Все темы




 0
0