мРНК в липидных наночастицах может восстановить продукцию сперматозоидов при бесплодии
Мужское бесплодие, которое вызвано мутациями в генах, связанных с мейозом, практически не поддается лечению. У таких пациентов получить подходящие для оплодотворения клетки обычно не удается. Авторы статьи в PNAS показали, что мРНК затронутого мутацией гена, доставленная в липидных наночастицах, запускает развитие сперматозоидов из клеток-предшественников. С помощью этого подхода они получили здоровое потомство от самцов мышей с нокаутом гена Pdha2, который приводил к исчезновению сперматозоидов.
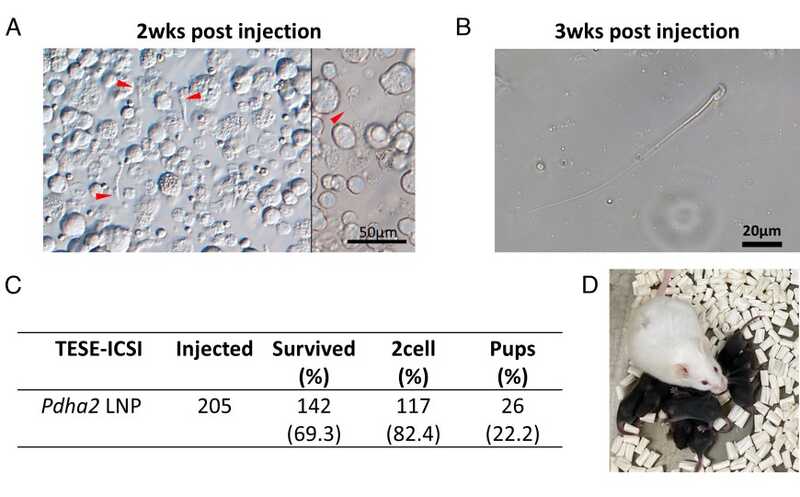
Ткани семенников мыши и сперматозоид через 2 и 3 недели после терапии (А, В), результаты ИКСИ (С) и потомство с матерью (D)
Credit:
PNAS. 2025. DOI: 10.1073/pnas.251657312 | CC BY 4.0
Исследователи из Университета Осаки (Япония) в сотрудничестве с Медицинским колледжем Бейлора (Хьюстон, Техас) предложили инновационный подход лечения мужского бесплодия — инъекции в яичко липидных наночастиц, несущих мРНК гена, который затронут мутацией. В экспериментах на мышах это привело к рождению здорового потомства.
Диагноз «бесплодие» (ненаступление беременности после года регулярной половой жизни без предохранения) ставится как минимум каждой шестой паре, и примерно в половине случаев причиной является мужской фактор. У 10–15% бесплодных мужчин отсутствуют сперматозоиды в эякуляте (азооспермия), причем механические препятствия для их выхода встречаются менее чем в половине этих случаев. В остальных случаях (необструктивная азооспермия, или НОА) таких препятствий нет, но имеют место нарушения сперматогенеза, поэтому получить сперматозоиды, подходящие для интрацитоплазматической инъекции в яйцеклетку (ICSI, или ИКСИ) крайне сложно.
В частности, если у пациента есть мутации в генах, связанных с мейозом, то сперматогенез останавливается на ранней стадии, и сперматозоидов, пригодных для экстракции, может просто не быть. Сегодня существуют диагностические панели для выявления мутаций, ассоциированных с необструктивной азооспермией. Это позволяет избежать бесполезных хирургических вмешательств, но эффективных терапевтических подходов по-прежнему не существует.
С появлением векторов для доставки генов такие возможности начали рассматриваться. Аденовирусные и лентивирусные векторы могут инфицировать клетки Сертоли (соматические клетки семенников, которые поддерживают развивающиеся мужские гаметы и защищают их от атак иммунной системы), а также сами сперматогониальные стволовые клетки. Однако вирусные векторы в данном случае не подходят для клинического применения, так как изменение генома клеток зародышевой линии не может быть одобрено. Поэтому исследователи выбрали доставку мРНК в липидных наночастицах.
В качестве модели мужского бесплодия использовали мышей с нокаутом гена Pdha2, у которых происходит остановка мейоза из-за нарушенной структуры комплекса пируватдегидрогеназы (PDH), крайне важного для получения энергии в форме АТФ. Pdha2 кодирует специфичную для семенников субъединицу E1α комплекса PDH, при этом пик экспрессии его мРНК приходится на сперматоциты в стадии пахитены. Патогенные варианты гомологичного гена у человека были обнаружены у пациентов с НОА.
Липидные наночастицы, несущие мРНК Pdha2, вводили инъекционно в просвет семенных канальцев, так как не было известно, способны ли они преодолеть гематотестикулярный барьер. После этого липидные наночастицы успешно доставляли мРНК как в сперматогенные клетки, так и в клетки Сертоли в яичках. Сигналы экспрессии обнаруживались уже через сутки после инъекции. Экспрессия длилась около 5 дней и охватывала около 55% канальцев.
Чтобы избежать потенциально неблагоприятной экспрессии Pdha2 в клетках Сертоли, авторы ввели в мРНК участок, распознаваемый микроРНК miR-471, высоко экспрессируемой в этих клетках, но не в сперматогониях. Это обеспечило сайленсинг мРНК в клетках Сертоли.
У самцов мышей с дефицитом Pdha2, которым ввели терапевтические наночастицы с МРНК, восстанавливалась продукция сперматозоидов. Через две недели в их тестикулах появились сперматиды, через три недели — сперматозоиды. От самцов после инъекции исследователи получили с помощью ИКСИ жизнеспособное плодовитое потомство (117 двухклеточных эмбрионов, 26 детенышей). Все потомство нормально развивалось и было гетерозиготным по мутации в гене Pdha2. Секвенирование подтвердило отсутствие крупномасштабных делеций и вставок, в том числе вставки ДНК-копии мРНК после обратной транскрипции.
Доставка мРНК в липидных наночастицах открывает новую эру в лечении мужского бесплодия, отмечают авторы статьи. Модификация состава ЛНЧ может дополнительно повысить эффективность терапии в будущем. Другие возможные направления работы — повышение специфичности доставки в определенные типы клеток, подавление экспрессии белка в нецелевых клетках или его быстрая деградация. Также возможна комбинация этого подхода с культивированием семенных канальцев in vitro, что избавит пациента от повторных хирургических вмешательств.
В PNAS опубликована другая работа при участии тех же японских исследователей под руководством Масахито Икава. В ней сообщается о восстановлении in vitro подвижности сперматозоидов при мужском бесплодии, вызванном дефицитом белка TMEM217 в семенниках. Эксперименты, также проведенные на мышах, привели к рождению здорового потомства.
В семьях мужчин, имеющих проблемы с фертильностью, может быть повышен риск онкозаболеваний
Источники
Daisuke Mashiko, et al. Sperm and offspring production in a nonobstructive azoospermia mouse model via testicular mRNA delivery using lipid nanoparticles // Proceedings of the National Academy of Sciences. October 13, 2025. 122 (42) e2516573122. DOI: 10.1073/pnas.251657312
Rie Iida-Norita, et al. Formation of a complex between TMEM217 and the sodium-proton exchanger SLC9C1 is crucial for mouse sperm motility and male fertility // Proceedings of the National Academy of Sciences. October 15, 2025. 122 (42) e2513924122. DOI: 10.1073/pnas.2513924122


 Меню
Меню





 Все темы
Все темы




 0
0