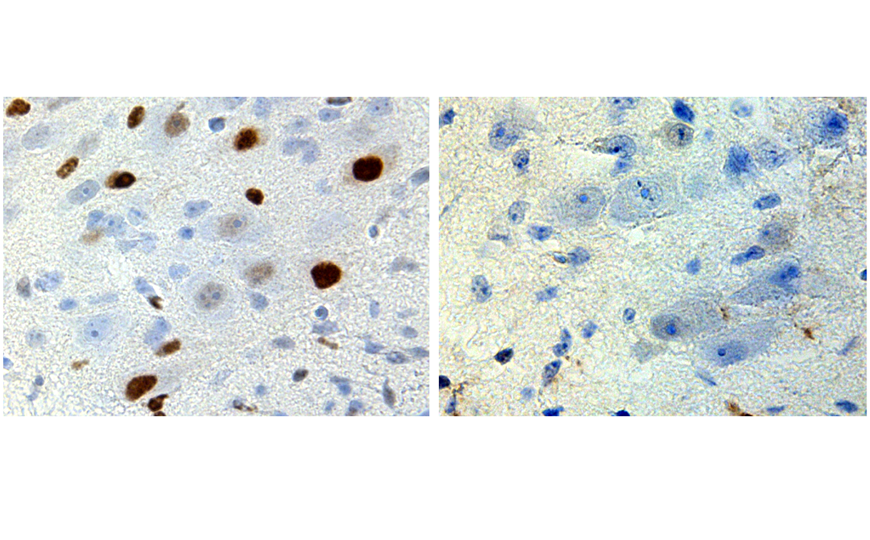
Мутационный статус генов BRCA предскажет ответ на химиотерапию
Трижды негативный рак молочной железы и рак яичника хорошо отвечают на терапию платиносодержащими препаратами, если в генах BRCA 1/2 присутствуют мутации. Для опухолей без мутаций предиктором ответа служит активность макрофагов.
Credit: moovstock | 123rf.com
Потеря активности генов BRCA1 и BRCA2, вовлеченных в систему репарации генома путем гомологичной рекомбинации, ассоциирована с чувствительностью опухолей к некоторым видам химиотерапии. Ранее предпринималось несколько попыток связать типы мутаций в BRCA с прогнозом ответа на лечение при трижды негативном раке молочной железы (ТНРМЖ) и раком яичника (РЯ), однако результаты были противоречивы. В новой работе ученые из США предположили, что функциональная роль генов BRCA определяется не только геномными мутациями, но и эпигенетическим статусом.
Они проанализировали геномы опухолей в нескольких когортах пациентов с ТНРМЖ и РЯ, прошедших химиотерапию с применением платиносодержащих препаратов и таксанов. Для работы использовались образцы от пациентов, а также мышиные модели ксенотрансплантации и клеточные линии. Их анализировали с помощью геномного и транскриптомного секвенирования, цифровой капельной ПЦР и других методов.
Ученые выявили три группы опухолей, по-разному реагирующих на терапию: с мутациями в одном из генов BRCA, без мутаций в обоих генах и опухоли с метилированным промотором BRCA1 (BRCA1meth). И метилирование, и мутации приводили к снижению активности гена, однако пациенты с BRCA1meth отвечали на терапию так же плохо, чем пациенты без мутаций. При этом мутации в BRCA ассоциировались с хорошими результатами лечения.
Мутации в BRCA были связаны с реакцией именно на платиносодержащие препараты. Ученые сравнили in vivo скорость роста ТНРМЖ с различными комбинациями мутаций после одного цикла лечения платиной. Опухоль без мутаций демонстрировала ответ на терапию только в 31,3% случаев. Мутации в BRCA1 и BRCA2 снижали скорость роста в 90,9% случаев. Опухоли с BRCA1meth отвечали на препараты чуть лучше, чем опухоли без мутаций, однако эта разница была статистически не значимой.
В следующем эксперименте на ксенографтных моделях ученые обнаружили, что статус метилирования промотора BRCA1 влияет на успех терапии: полное метилирование улучшает ответ, частичное — ухудшает. Они заметили, что ксенографты с полным метилированием были получены от пациентов перед началом приема платиносодержащих препаратов, а с частичным — от пациентов, которые уже начали терапию. Ученые сделали вывод, что в процессе лечения происходит деметилирование промотора BRCA1, увеличение экспрессии гена и, следовательно, развитие резистентности опухоли. При этом потеря метилирования обусловлена не экспансией клонов с активным промотором, а активным деметилированием одного аллеля промотора BRCA1 в большинстве клеток.
Дополнительно ученые показали, что чувствительность к комбинации платиносодержащих препаратов и таксанов у пациентов с ТНРМЖ и РЯ без мутаций в BRCA зависит от иммунной сигнатуры опухоли. Так, повышенная активность макрофагов воспалительного фенотипа ассоциирована с хорошим ответом на лечение. Авторы считают, что оценка мутаций в генах BRCA в комбинации с анализом иммунологического статуса опухоли позволит точно предсказывать исход химиотерапии.
Ранее другая команда выделила четыре подтипа ТНРМЖ, различающихся по активности метаболических путей и потенциальным мишеням для терапии.
Источник
Mehghi, F., et al. Genomic and epigenomic BRCA alterations predict adaptive resistance and response to platinum-based therapy in patients with triple-negative breast and ovarian carcinomas. // Science Translation Medicine, published online 06 July 2022. DOI: 10.1126/scitranslmed.abn19


 Меню
Меню





 Все темы
Все темы




 0
0