Негенетическое наследование фенотипа помогает патогенным бактериям адаптироваться к хозяевам
Одну из трудностей в лечении бактериальных инфекций представляет фенотипическая гетерогенность патогена. Например, у энтеропатогенной кишечной палочки (EPEC) описано два характерных фенотипа. Ученые из Израиля разработали методику анализа Microcolony-seq, с помощью которой показали, что фенотипы EPEC наследуются в течение многих поколений, причем генетически популяция бактерий остается однородной. Они также выявили механизм «сброса» этой фенотипической памяти и охарактеризовали такое явление у золотистого стафилококка. Подобная наследуемая гетерогенность фенотипов служит одним из механизмов адаптации патогена к хозяину.
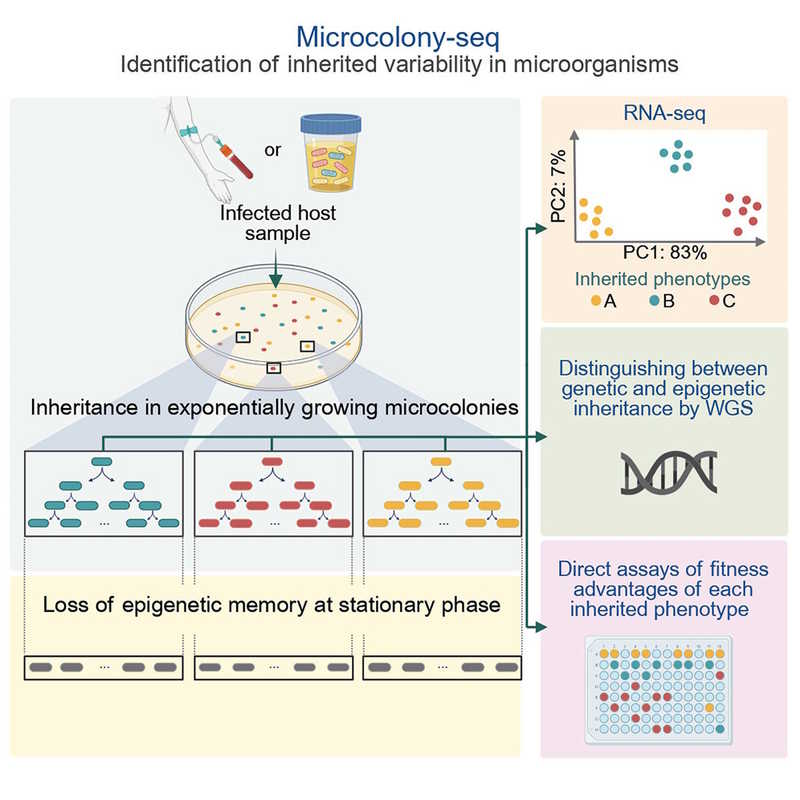
Наследственная фенотипическая гетерогенность в популяции бактерий — один из механизмов адаптации патогенов. Она способствует уклонению от иммунитета хозяина, разделению труда и колонизации поверхностей. Стабильно наследуемая фенотипическая гетерогенность наблюдается, в частности, у энтеропатогенной кишечной палочки — специфичного человеческого патогена. Однако ее затруднительно изучать — хотя последние достижения методов секвенирования РНК единичных клеток (scRNA-seq) позволяют выявить гетерогенность, анализируя транскриптомы отдельных бактерий, у таких технологий сохраняется ряд ограничений. Эти ограничения побудили ученых из Израиля разработать Microcolony-seq — метод выявления наследственной изменчивости в бактериальных популяциях. Объединяя секвенирование РНК, полногеномное секвенирование и характеризацию фенотипа, Microcolony-seq позволяет различить генетическое и фенотипическое наследование.
У энтеропатогенной Escherichia coli (EPEC) описано два выраженных фенотипа, обозначенных как SMALL и BIG — их легко отличить по размерам колоний. Исследователи проверили, можно ли выявить эту фенотипическую разницу, не зная размеров колонии. Для этого бактерии выращивали в жидкой среде (DMEM) при 37°C — такие условия имитируют нахождение в организме хозяина и обычно используются для активации вирулентности EPEC.
Сначала с помощью Microcolony-seq авторы выявили наиболее изменчивые гены среди микроколоний. По экспрессии этих генов микроколонии кластеризовали — это позволило выделить две популяции, которые, как затем выяснилось, на 100% соответствовали морфотипам SMALL и BIG. Интересно, что бактерии из этих субпопуляций сохраняли фенотип, даже если росли на одной чашке.
Для более детального исследования различий авторы провели анализ дифференциальной экспрессии. В субпопуляции морфотипа SMALL уровень экспрессии известного набора генов вирулентности был значительно выше, поэтому ее обозначили как VirEPEC, а вторую, с крупными колониями и низким уровнем генов вирулентности — AvirEPEC. Активно экспрессируемые гены VirEPEC относились преимущественно к аннотированным генам вирулентности (59 из 60, в том числе компоненты системы секреции III типа), а уровень генов, связанных с подвижностью и хемотаксисов, напротив, был снижен.
Вдохновившись таким результатом, авторы проанализировали с помощью Microcolony-seq и неаннотированные области генома. Они выявили открытую рамку считывания длиной 192 кодона — она находилась на плазмиде, экспрессия которой значительно повышена в субпопуляции VirEPEC. Кодируемый ей предполагаемый ген назвали pilW из-за его сходства с PilW, белком сборки пилей IV типа, у других E. coli.
Дальнейший анализ проводили, выращивая микроколонии VirEPEC и AvirEPEC на твердой среде с различными добавками. Ученые рассмотрели три фактора, с которыми бактерии могут столкнуться в организме хозяина: наличие бутирата (известного модулятора вирулентности), метаболиты стула младенцев — EPEC патогенна преимущественно для них, — и анаэробные условия, характерные для тонкого кишечника как для естественной ниши EPEC. Скорость роста и физиология микроколоний различалась в зависимости от условий, но разделение на субпопуляции сохранялось. При этом, как и в предыдущих экспериментах, они сохраняли генетическую идентичность, менялись только уровни экспрессии генов.
В целом анализ показал, что вирулентные микроколонии VirEPEC имеют явное преимущество в организме хозяина. Однако зачем бактериям поддерживать еще и второй фенотип? Проанализировав различные условия, авторы пришли к выводу, что преимущества AvirEPEC — это высокая подвижность и способность расти при высоком содержании соли. В этой субпопуляции была повышена экспрессия генов, участвующих в формировании бактериальной капсулы. Это подтверждалось и морфологически — при повышении концентрации соли в среде бактерии AvirEPEC формировали биопленки с большим количеством внеклеточных полимеров, тогда как бактерии VirEPEC либо переходили в состояние AvirEPEC, либо не выживали.
Обнаруженное переключение между фенотипами при избытке соли напомнило авторам «сброс» гетерогенности популяции при достижении стационарной фазы. Они проанализировали работу оперона per — одного из наиболее отличающихся по уровню экспрессии между VirEPEC и AvirEPEC. В качестве показателя экспрессии perABC они отслеживали меченый PerB. Уровень этого белка значительно снижался в стационарной фазе роста, а его оверэкспрессия нарушала сброс фенотипической памяти. Иными словами, для ее поддержания бактериям достаточно высокого уровня экспрессии PerABC.
Дальнейший анализ выявил еще три варианта наследуемых бимодальных фенотипов — два у E. coli и один у золотистого стафилококка Staphylococcus aureus. У микроколоний E. coli, выделенных из мочи пациентов, наблюдалось два фенотипа — VirUTI и AvirUTI — различавшихся метаболизмом железа.
В целом авторы заключают, что наблюдаемая гетерогенность фенотипов патогенных бактерий (в том числе в пределах одной инфекции) — это адаптивная стратегия. В ее основе, вероятно, лежит механизм положительной обратной связи через белки Per, которые поддерживают память бактерии на эпигенетическом уровне. При достижении стационарной фазы роста или при резкой смене условий происходит глобальное транскрипционное программирование, которое стирает память. Выявленную особенность «наследуемой фенотипической памяти» можно использовать при подборе терапии бактериальных инфекций или при разработке новых средств лечения, однако детали этого молекулярного механизма еще предстоит изучить.
Клостридия жертвует патогенностью ради приобретения устойчивости к антибиотику
Метаболизм азота важен для адаптации золотистого стафилококка к обитанию на человеке
Источник
Raya Faigenbaum-Romm, et al. Uncovering phenotypic inheritance from single cells with Microcolony-seq. // Cell (2025). DOI: 10.1016/j.cell.2025.08.001


 Меню
Меню





 Все темы
Все темы
 Credit:
Credit:



 0
0