Новый подход к генной терапии серповидноклеточной анемии испытали на макаках
Команда исследователей из США при участии Дэвида Лю опубликовала статью о редактировании у макак-резусов гена HBB, мутации в котором вызывают серповидноклеточную анемию (СКА). От существующих генотерапевтических препаратов против СКА этот подход отличает использование редакторов оснований — систем на основе CRISPR-Cas, которые изменяют одну «букву» в ДНК, а не целые участки. Такое редактирование может заменить ассоциированный с болезнью кодон GTG в гене HBB на GСG — так называемый вариант Масакар, который встречается в человеческих популяциях и не приводит к заболеванию.
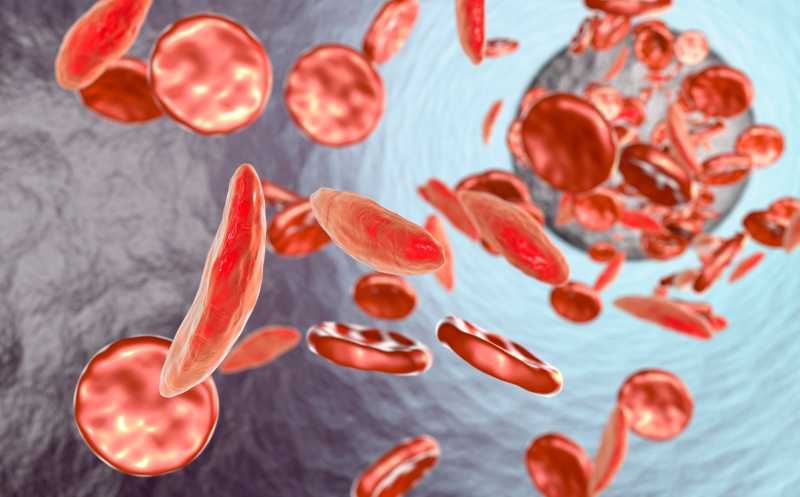
Авторы статьи в Science Translational Medicine отредактировали ген β-цепи глобина, мутации в котором вызывают серповидноклеточную анемию, в гемопоэтических стволовых клетках трех макак-резусов, а затем наблюдали их в течение 200 дней, исследуя клетки крови и образцы костного мозга.
Генотерапевтические препараты для лечения серповидноклеточной анемии (СКА) регулярно появляются в заголовках PCR.NEWS. Разрешенные к применению препараты, Касгеви и Лифгениа, — своего рода альтернатива трансплантации донорских гемопоэтических стволовых клеток (ГСК). Собственные ГСК пациента модифицируют вне организма таким образом, чтобы они производили функциональный гемоглобин (Касгеви с помощью CRISPR-Cas редактирования отменяет подавление синтеза фетального гемоглобина, Лифгениа доставляет в клетку с помощью лентивирусного вектора ген функционального гемоглобина). Обсуждаются подходы к редактированию in vivo , то есть прямо в организме. Однако остаются опасения, связанные с повышенным риском онкозаболеваний при терапии отредактированными клетками (предупреждение о таких рисках есть в инструкции Лифгениа).
Есть мнение, что более безопасной стратегией может быть использование редакторов оснований (base editor, BE), которые заменяют единичные нуклеотиды в определенных участках ДНК, не внося двунитевых разрывов. Например, цитозиновые редакторы вызывают замену C на T, адениновые — замену A на G. Первые редакторы оснований были созданы под руководством Дэвида Лю (Институт Бродов, МТИ, Гарвардский университет), и его лаборатория продолжает работу в этом направлении. Одна из целей — создание генной терапии СКА на основе редактора оснований.
Причина СКА — замена нуклеотида в гене HBB, который кодирует β-цепь глобина. Кодон GAG превращается в GTG, в результате происходит замена аминокислоты в β-глобине: вместо гидрофильной глутаминовой кислоты появляется гидрофобный валин. Гидрофобное пятно на поверхности белка ведет к слипанию молекул дефектного гемоглобина и появлению серповидных эритроцитов, закупоривающих капилляры.
В 2021 году команда Дэвида Лю представила свой подход к терапии СКА. Существующие редакторы оснований не позволяли исправить Т на А (кодон GTG на GAG). Но замена Т на С (то есть А на G в комплементарной цепи) создает известный непатогенный вариант HBB, впервые обнаруженный в индонезийском городе Макасар. Он приводит к замене глутаминовой кислоты на аланин в β-цепи глобина, и такой гемоглобин не полимеризуется.
В статье 2021 года авторы описали создание редактора оснований, превращающего патогенный аллель в аллель Макасар, отредактировали ГСК пациентов и мышей, моделирующих СКА. В новой работе оценивалась долгосрочная эффективность отредактированных клеток и объем нецелевого редактирования в экспериментах на трех макаках-резусах. Это существенный шаг к испытаниям технологии на людях, отмечают авторы.
У нечеловекообразных обезьян неизвестна мутация, вызывающая СКА, поэтому авторы редактировали гены в гемопоэтических стволовых клетках здоровых макак. Они вносили синонимичные замены нуклеотидов в ген HBB (то есть замены, не приводящую к заменам аминокислот, но позволяющие наблюдать за эффективностью редактирования) в том же локусе, где находится кодон-мишень.
Эффективность редактирования ГСК в клетках макак превысила 60%. Оно не повлияло на свойства клеток, важные с точки зрения безопасности, такие как созревание в эритроидные или миелоидные клетки. Исправления в локусе сохранялись при культивировании клеток.
Отредактированные клетки снова ввели животным, которые перед этим были облучены, чтобы уничтожить ГСК, остававшиеся в организме (это стандартная процедура при генной терапии ГСК ex vivo). Последующее наблюдение продолжалось до 200-го дня, у животнгых брали образцы периферической крови и костного мозга.
После трансплантации у всех трех макак быстро восстановились уровни нейтрофилов, эритроцитов и тромбоцитов. Средний уровень отредактированных клеток крови, имеющих ядро, составлял 25,6%. Более 20% стволовых клеток костного мозга имели моно- или биаллельные модификации, вызванные редактированием.
Более 900 участков генома были проверены на нецелевые замены A->G, и такие замены действительно произошли в восьми сайтах (в работе 2021 года их было 12). Какого-либо влияния этих модификаций (например, их преимущественный отбор в организме) не было обнаружено.
Эти данные подтверждают, что редактирование оснований в аутологичных ГСК может найти применение в терапии СКА. Однако до перехода к клиническим исследованиям необходимо провести дополнительные эксперименты по оценке безопасности.
Источник
Stefan Radtke, et al. Engraftment and persistence of HBB base-edited hematopoietic stem cells in nonhuman primates // Science Translational Medicine. 13 Aug 2025. Vol 17, Issue 811. DOI: 10.1126/scitranslmed.adn2601


 Меню
Меню





 Все темы
Все темы




 0
0











