Описан механизм высвобождения «зависших» рибосом у бактерий
Ученые из США и Германии на примере кишечной палочки E. coli описали неизвестный ранее механизм высвобождения рибосом, которые остановились на мРНК и не могут продолжать синтез белка. Они показали, что эндонуклеаза SmrB вносит разрыв в мРНК с 5’-конца от остановившейся рибосомы. После этого в рибосомный туннель может войти транспортно-матричная РНК, «снимающая» рибосому с транскрипта.
gritsalak | 123rf.com
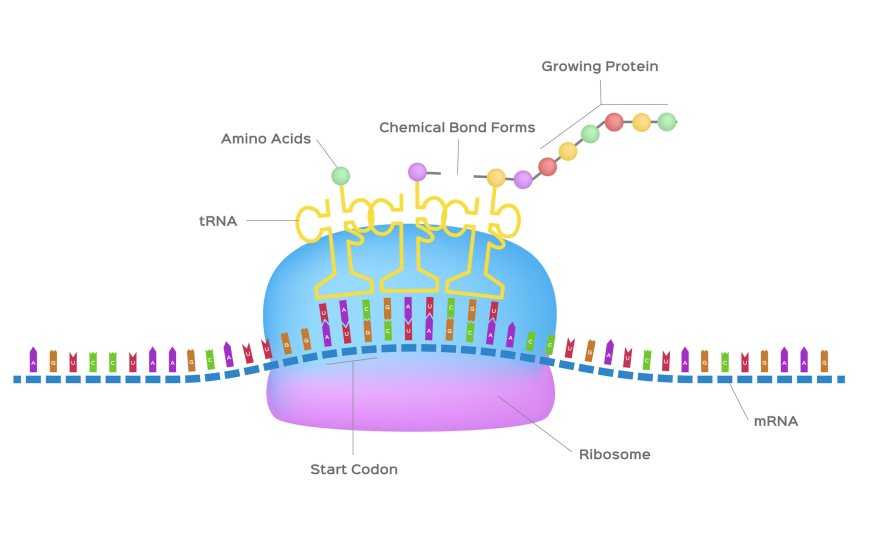
У бактерии Escherichia coli примерно в одном случае из 250 рибосома «зависает» на мРНК и, остановившись, не может продолжать синтез белка. Остановка рибосомы во время синтеза белковой цепочки может происходить по разным причинам, например, из-за химических повреждений мРНК или медленно считываемых кодонов, а иногда трансляции препятствует сам синтезируемый пептид. «Зависшие» рибосомы у бактерий высвобождаются транспортно-матричными РНК (тмРНК). Молекула тмРНК внедряется в туннель для мРНК в рибосоме и забирает ее на себя. Трансляция тмРНК завершается на стоп-кодоне, после чего субъединицы рибосомы становятся свободными.
Долгое время был неизвестен механизм внесения разрыва в мРНК, который необходим для привлечения тмРНК. В новой статье, опубликованной в Nature, охарактеризована эндонуклеаза SmrB, которая вносит разрыв в мРНК с 5’-конца от рибосомы и делает возможным взаимодействие рибосомы с тмРНК.
Авторы исследования провели скрининг мутаций E. coli, которые позволяют ей успешно транслировать очень сложный мотив в составе мРНК. Этот мотив разделял ген, кодирующий люциферазу NanoLuc, и ген, кодирующий белок устойчивости к антибиотику блеомицину. Если рибосомы в мутантной клетке «зависают» на трансляции сложного участка и высвобождаются, то бактерии лишаются устойчивости к антибиотику. Если же высвобождения рибосомы не происходит, то она доходит до синтеза белка устойчивости, поэтому таких мутантов можно отобрать на среде с антибиотиком.
Ученые создали библиотеку нокаутных штаммов из пяти миллионов мутантов E. coli, в которых различные гены были инактивированы за счет случайного внедрения транспозазы Tn5. Анализ мутантов, выживающих на среде с антибиотиком, показал, что у них вставка Tn5 обнаруживается в гене smrB более чем в 3 000 раз чаще, чем в среднем по геному. Этот ген кодирует эндонуклеазу. Мутанты, лишенные функционального гена smrB, способны к трансляции мРНК, содержащих сложные для считывания мотивы. При этом они сверхчувствительны к условиям, способствующим повсеместной задержке рибосом на различных эндогенных транскриптах.
Дальнейшие эксперименты показали, что эндонуклеаза SmrB действительно вносит разрыв в мРНК с 5’-стороны от «зависшей» рибосомы. Благодаря этому рибосома может взаимодействовать с тмРНК. Привлечение SmrB к «зависшей» рибосоме происходит при ее столкновении с следующей за ней рибосомой, транслирующей тот же транскрипт. Чтобы детально изучить взаимодействие SmrB с рибосомой, исследователи получили структуру комплекса из двух столкнувшихся рибосом (дисомы), а также дисомы с SmrB. Они показали, что SmrB действительно распознает столкнувшиеся рибосомы без участия дополнительных факторов.
Источник
Saito, K., Kratzat, H., Campbell, A. et al. Ribosome collisions induce mRNA cleavage and ribosome rescue in bacteria. // Nature, 2022, DOI: 10.1038/s41586-022-04416-7


 Меню
Меню





 Все темы
Все темы



 0
0











