Опухоль мозга приобретает резистентность к лечению, но становится чувствительной к дефициту серина
Глиобластома — самая агрессивная форма опухоли головного мозга, характеризующаяся быстрым ростом и устойчивостью к лечению. Исследователи из США сравнили пути метаболизма глюкозы в нормальной коре мозга и опухолевой ткани у людей и мышей. В коре глюкоза утилизируется в цикле Кребса и поддерживает синтез нейромедиаторов, тогда как в тканях глиобластомы она используется для синтеза нуклеотидов и NAD/NADH, необходимых для пролиферации и резистентности к терапии. Но при этом клетки опухоли теряют способность к синтезу аминокислоты серина и становятся зависимыми от его внешних источников. Ограничение серина в рационе мышей замедляло рост опухоли и усиливало действие химиолучевой терапии.
Глюкоза — главный источник энергии для работы мозга. В нормальных условиях она утилизируется в цикле Кребса, обеспечивая продукцию высокоэнергетических молекул, а также используется для синтеза нейромедиаторных аминокислот, которые поддерживают когнитивные и физиологические функции. Однако у злокачественных опухолей мозга, в частности у глиобластомы, эта картина радикально меняется.
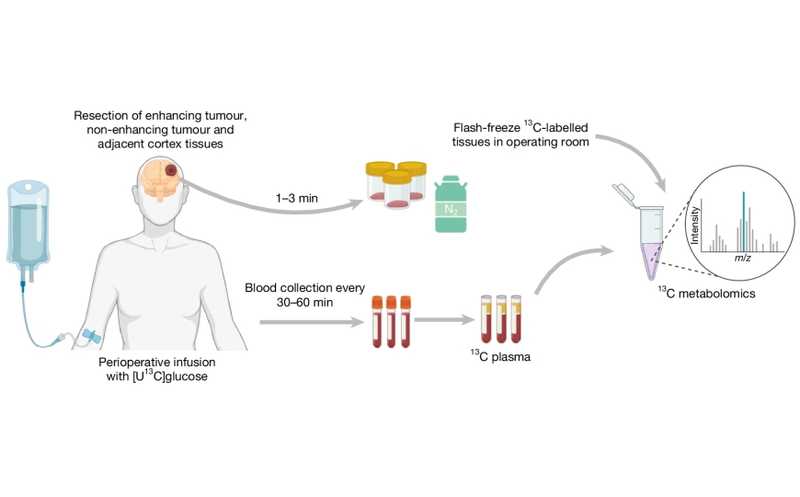
Глиобластома известна своей агрессивностью, быстрым ростом, устойчивостью к терапии и крайне неблагоприятным прогнозом. Несмотря на комплексное лечение, включающее операцию, лучевую и химиотерапию, большинство пациентов умирают в течение 1–2 лет после постановки диагноза. Молекулярная гетерогенность опухоли затрудняет поиск эффективной терапии, но есть альтернативная возможность: обнаружение уязвимых точек в измененном метаболизме опухоли, способствующем ее резистентности. Чтобы понять, как изменен метаболизм глюкозы в глиобластоме, исследователи из США использовали глюкозу, в молекулах которой все шесть атомов углерода были заменены на стабильный тяжелый изотоп 13C. Пациентам делали инфузии меченой глюкозы во время удаления опухоли, а также ее вводили мышиным моделям глиобластомы, которым трансплантировали клетки человеческой опухоли. Затем исследователи анализировали с помощью жидкостной хроматографии и масс-спектрометрии распределение меченого углерода в образцах опухоли и окружающих тканей мозга.
В нормальной коре мозга глюкоза преимущественно направлялась в цикл Кребса, а также использовалась для образования глутамата, аспартата и ГАМК — ключевых нейромедиаторов. В опухолевой ткани этот процесс был подавлен: резко снижалась активность цикла Кребса и синтез нейромедиаторов. Вместо этого глюкоза перенаправлялась на синтез нуклеотидов и молекул NAD/NADH, необходимых для строительства новых клеток и обеспечивающих устойчивость к повреждениям. Таким образом, глиобластома перестраивает нормальный метаболизм глюкозы ради собственных нужд.
Поскольку исследования во время операции представляют, по сути, одну временную точку, авторы статьи дополнили эти данные экспериментами на мышах. Для этого они разработали особый подход — анализ метаболических потоков (metabolic flux analysis, MFA). После того, как мышам с опухолями вводили 13C-глюкозу, образцы тканей собирали в нескольких временных точках на протяжении часов, и таким образом получили данные о динамике метаболитов. Эти данные подтвердили, что в опухоли усилена продукция всех четырех нуклеотидов из глюкозы.
Интересно, что после лучевой терапии опухоль у мыши перестраивала продукцию нуклеозидмонофосфатов, повышая продукцию ГМФ и снижая продукцию АМФ. Повышенное производство гуанилатов, которые необходимы для быстрого восстановления ДНК, объясняет, почему стандартная лучевая терапия часто оказывается недостаточно эффективной.
Особое внимание исследователи уделили роли серина. В нормальной ткани мозга значительная его часть синтезируется из глюкозы. Ткань глиомы вместо самостоятельного производства серина активно захватывала его из внешней среды — это позволяло экономить глюкозные углероды и направлять их на синтез нуклеотидов. (В нормальной ткани мозга быстрее нарастало количество молекул серина, содержащих три атома 13C, — такой серин образуется de novo в результате гликолиза. В глиоме присутствовал преимущественно серин с одним меченым атомом, очевидно, полученным через другие пути.)
Таким образом, серин может играть роль «топливного переключателем», определяющим, будет ли глюкоза использоваться для поддержания нормальной функции мозга или для опухолевого роста.
Здесь же обнаружилась потенциальная уязвимость. Когда мыши получали корм с ограниченным содержанием серина, а также глицина (который может быть источником серина), это резко снизило уровень нуклеотидов в опухоли, замедлило ее рост и усиливало действие стандартной химиолучевой терапии. При этом метаболизм здоровой коры почти не страдал, так как нормальные клетки продолжали синтезировать серин самостоятельно.
Авторы исследования установили, что глиобластома коренным образом перестраивает метаболизм глюкозы, подавляя нормальные нейрофизиологические процессы и направляя ресурсы на синтез нуклеотидов и поддержание устойчивости к терапии. Однако при этом у опухоли возникает зависимость от серина из внешних источников, что создает потенциальную терапевтическую уязвимость. Ограничение количества серина в пище может замедлять рост опухоли и повышать эффективность стандартного лечения. Таким образом, понимание специфической метаболической адаптации глиом открывает перспективы для новых терапевтических стратегий.
Как заморить голодом раковую клетку, воздействуя на метаболизм глутамина
Комбинация аргининового голодания и сенолитиков уменьшает опухоль у мышей
При дефиците аминокислот раковые клетки поглощают внеклеточный матрикс
Опухолевые клетки помогают друг другу добыть аминокислоты, чтобы выживать и растиИсточник
Scott A.J., et. al. Rewiring of cortical glucose metabolism fuels human brain cancer growth // Nature (2025), published online 3 September 2025. DOI: 10.1038/s41586-025-09460-7


 Меню
Меню





 Все темы
Все темы




 0
0










