PARADISCO — новый метод обнаружения ингибиторов транспортных белков, ассоциированных с раком
Австрийские ученые разработали метод поиска ингибиторов транспортных белков семейства SLC. Для структурно и функционально сходных белков сложно подобрать селективные ингибиторы. Чтобы решить эту проблему, авторы создали клеточные линии, каждая из которых экспрессирует лишь один из таких белков. Высокоселективный ингибитор подавляет рост только одной из линий и не влияет на другие.
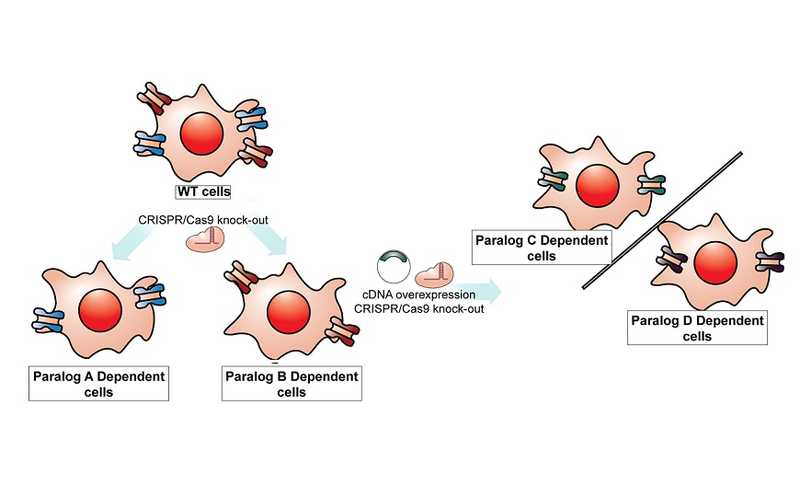
Схема получения клеток для скрининга. Пояснения в тексте
Credit:
Cell Chem Biol, 2023, DOI: 10.1016/j.chembiol.2023.06.029 | CC BY 4.0
Переносчики растворенных веществ (SLC) — большая группа мембранных белков, отвечающих за транспорт аминокислот, сахаров и других соединений в клетку и выведение их наружу. С помощью таких белков транспортируется в том числе лактат — конечный продукт гликолиза, который продуцируют в большом количестве раковые опухоли. Лактат способен подавлять иммунные клетки и вызывать резистентность к лечению. Транспортеры лактата (всего их описано четыре) играют в этом ключевую роль, однако эти белки еще недостаточно изучены. В Центре молекулярной медицины Академии наук Австрии (CeMM) разработали новый метод изучения белков-переносчиков и с помощью этого метода нашли новый селективный ингибитор.
Лактат преимущественно переносится через мембрану белками семейства SLC16. Главная сложность при изучении белков SLC заключается в их функциональной избыточности — одну и ту же функцию выполняют несколько паралогов. Они различаются по характеру экспрессии в клетках и тканях, так, SLC16A1 экспрессируется повсеместно, а SLC16A8 — исключительно в ткани сетчатки. Большое структурное сходство между ними затрудняет разработку селективных ингибиторов.
Авторы обратили внимание на синтетическую летальность между переносчиками лактата SLC16A1 и SLC16A3 (жизнеспособность клеток снижает лишь потеря функции обоих транспортеров из-за ингибирования или мутации, но не какого-то одного из них). Используя этот принцип, они создали скрининговую систему, которую назвали паралогозависимым изогенным клеточным анализом (PARADISO). Система включает пять изогенных клеточных линий, причем выживание и приспособленность каждой из них зависит от разных паралогов. Четыре линии экспрессируют по одному индивидуальному переносчику, пятая, контрольная, — все четыре.
Исследование проводилось на гаплоидной линии клеток человека HAP1. Клетки, не экспрессирующие SLC16A3, становятся чувствительными к ингибированию SLC16A1, в то время как в клетках, экспрессирующих SLC16A3, этот белок берет на себя функцию ингибированного SLC16A1, и такие клетки выживают. Авторы решили создать клеточные линии, каждая из которых зависит от одного из переносчиков лактата. Так, клеточная линия, экспрессирующая только SLC16A1, будет чувствительна к ингибиторам SLC16A1, но не к селективным ингибиторам SLC16A3, SLC16A7 или SLC16A8.
На первом этапе были созданы две клеточные линии: одна не экспрессировала SLC16A1, другая не экспрессировала SLC16A3. На них и контрольной линии дикого типа тестировали различные ингибиторы белков-переносчиков лактата, например сиросингопсин — ингибитор с высоким сродством к SLC16A3. Полученные данные о сродстве ингибиторов к переносчикам соответствовали предыдущим исследованиям.
Как показало РНК-секвенирование, клетки HAP1 изначально не экспрессируют ни SLC16A7, ни SLC16A8. Чтобы создать еще двае изогенные клеточные линии, зависимые от от этих двух паралогов, авторы сначала добились сверхэкспрессии каждого из них в клетках, которые экспрессировали только SLC16A1, а затем нокаутировали в них ген SLC16A1. В результате были получены четыре линии, в каждой из которых работал только один транспортер.
Авторы провели скрининг библиотеки, содержащей примерно 90 тысяч соединений, чтобы найти селективные ингибиторы SLC16A3. Из 1410 соединений, снижающих жизнеспособность клеток на 50% по сравнению с ДМСО, отобрали вещества, способные уничтожать клетки, зависимые от функции SLC16A3, но не клетки дикого типа и не зависимые от SLC16A1; таких веществ оказалось 34. Дальнейший скрининг на других клеточных линиях позволил выбрать 13 веществ с еще более высокой селективностью к SLC16A3. При обработке клеток этими соединениями в них накапливался лактат.
Затем авторы проверили метаболическую стабильность соединений в микросомах печени. Было отобрано одно из них, названное slCeMM1, которое ингибировало рост клеток, зависящих от SLC16A3 (но не клеток, зависящих от SLC16A1), и вызывало накопление внутриклеточного лактата. Протеомный анализ методом масс-спектрометрии подтвердил высокую селективность соединения.
Подобный подход может быть применен и к другим белкам-мишеням, имеющим паралоги, отмечают авторы.
Источник
Vojtech Dvorak, et al. Paralog-dependent isogenic cell assay cascade generates highly selective SLC16A3 inhibitors // Cell Chemical Biology, July 28, 2023, DOI: 10.1016/j.chembiol.2023.06.029


 Меню
Меню





 Все темы
Все темы




 0
0