Пересадка стволовых клеток из здорового глаза, выращенных в культуре, предотвращает помутнение роговицы
Вызванный травмой или другими причинами дефицит лимбальных эпителиальных стволовых клеток (ЛЭСК), которые обеспечивают регенерацию роговицы, может привести к потере зрения. Существуют методы трансплантации собственных ЛЭСК пациента из здорового глаза, но они не одобрены в США. Американские ученые разработали новый метод культивирования ЛЭСК, соответствующий стандартам FDA, и доказали его эффективность и безопасность в клиническом исследовании.

Статья в Nature Communications представляет результаты фазы 1/2 клинического исследования, в котором оценивались безопасность и эффективность трансплантации культивированных аутологичных лимбальных эпителиальных клеток, предотвращающей нарушение регенерации роговицы глаза.
Прозрачность роговицы зависит от ее регенеративной способности, которую обеспечивают лимбальные эпителиальные стволовые клетки (ЛЭСК), находящиеся в лимбе роговицы (месте ее сочленения со склерой). Помимо регенерации роговичного эпителия, ЛЭСК служат барьером, препятствующим инвазии эпителия конъюнктивы на поверхность роговицы. Недостаток этих клеток, вызванный травмой глаза, инфекцией или другими причинами, ведет к дискомфорту (боль, светобоязнь, слезотечение) и снижению зрения, возможно, к полной потере прозрачности роговицы. Хирургическое лечение дефицита ЛЭСК чаще всего проводится при помощи трансплантации аутологичных лимбальных стволовых клеток, то есть собственных клеток пациента, взятых из непораженного глаза. Аутологичные клетки предпочтительней аллогенных (донорских), так как не требуют пожизненной иммуносупрессии для предотвращения отторжения.
Существует несколько стратегий трансплантации ЛЭСК, как прямой, так и с культивированием клеток перед пересадкой. Культивирование клеток ex vivo увеличивает их количество, таким образом, можно брать меньше клеток из здорового глаза. Продукты, содержащие культивированные ЛЭСК для трансплантации, доступны в Евросоюзе (Holoclar) и Японии (Nepic). Однако они не могут быть разрешены в США, так как культивируются в среде с сывороткой, антибиотиками и мышиными фибробластами 3T3 в качестве питающих клеток, а это не соответствует стандартам FDA.
Исследователи из Гарвардской медицинской школы, Института рака Даны—Фарбера, Бостонской детской больницы и других научных и медицинских центров разработали удовлетворяющий требованиям FDA метод лечения дефицита ЛЭСК, который не требует применения компонентов животного происхождения, антибиотиков и сыворотки. Полученные клетки назвали CALEC (cultivated autologous limbal epithelial cells ). В новой статье опубликованы результаты клинического исследования.
Метод выращивания CALEC авторы разработали несколько лет назад и проверили его безопасность на четырех пациентах. (Подробнее на PCR.news.)
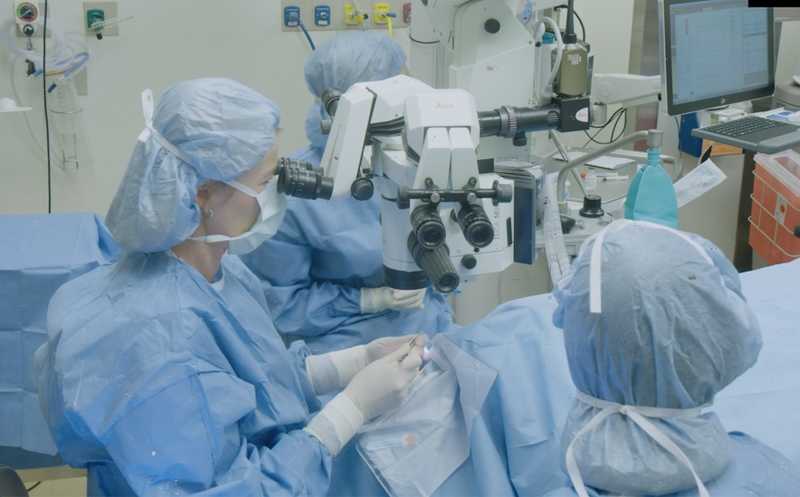 Ведущий автор статьи Ула Юркунас проводит первую трансплантацию стволовых клеток CALEC в 2018 году в клинике Mass Eye and Ear в Бостоне пациенту, получившему сильный химический ожог глаза. Credit: Mass Eye and Ear |
Пресс-релиз
Ведущий автор статьи Ула Юркунас проводит первую трансплантацию стволовых клеток CALEC в 2018 году в клинике Mass Eye and Ear в Бостоне пациенту, получившему сильный химический ожог глаза. Credit: Mass Eye and Ear |
Пресс-релиз
Свободные ЛЭСК получают из здорового глаза пациента с помощью биопсии и ферментативной обработки полученного фрагмента ткани. Культивирование перед трансплантацией происходит в два этапа. На первом этапе ЛЭСК выращивают в лунках пластикового планшета до тех пор, пока не станут конфлюэнтными (готовыми прикрепиться к субстрату). На втором этапе клетки переносият на лишенную эпителия амниотическую мембрану, на которой происходит дальнейший рост и формирование трансплантата. (Амниотическая мембрана широко используется в хирургическом лечении дефектов роговицы.) По окончании культивирования оценивается количество и жизнеспособность клеток, контролируется стерильность.
В новое исследование включили 15 участников в возрасте от 24 до 78 лет, с односторонним дефицитом ЛЭСК, вызванным химическим ожогом глазной поверхности или другими причинами. Из них 14 человек (13 мужчин и одна женщина) завершили 18-месячное наблюдение после трансплантации.
Ни у одного из пациентов не наблюдалось серьезных нежелательных явлений и осложнений, связанных с донорским или реципиентным глазом (острота зрения первого у всех оставалась на исходном уровне). Только у одного участника была обнаружена бактериальная инфекция, связная с постоянным ношением контактных линз.
При первом наблюдении, через три месяца после трансплантации, CALEC полностью восстановил роговицу у 50% участников. Через 12 и 18 месяцев полный успех был отмечен у 11 и 10 человек соответственно (79% и 77%; один из участников к 18 месяцев получил повторную трансплантацию). Еще у двух участников в этих временных точках наблюдался частичный успех (улучшение васкуляризации роговицы и/или симптоматики). Таким образом, общий успех CALEC составил 86% через три месяца, 93% и 92% через 12 и 18 месяцев.
В общей сложности трем участникам трансплантировали CALEC повторно, и один из них также достиг полного успеха к заключительному визиту.
Таким образом, CALEC продемонстрировал высокие показатели эффективности и безопасности. Тем не менее терапия остается экспериментальной и в настоящее время не применяется в американских клиниках. Авторы надеются, что это исследование станет основой для создания и внедрения одобренной клеточной терапии дефицита ЛЭСК.
Недостаток сна уменьшил число стволовых клеток роговицы у мышей
Источник
Jurkunas U.V. Cultivated autologous limbal epithelial cell (CALEC) transplantation for limbal tem cell deficiency: a phase I/II clinical trial of the first xenobiotic-free, serum-free, antibiotic-free manufacturing protocol developed in the US // Nature Communication 16, 1-12 (2025), published online 04 March 2025. DOI: 10.1038/s41467-025-56461-1


 Меню
Меню





 Все темы
Все темы




 0
0











