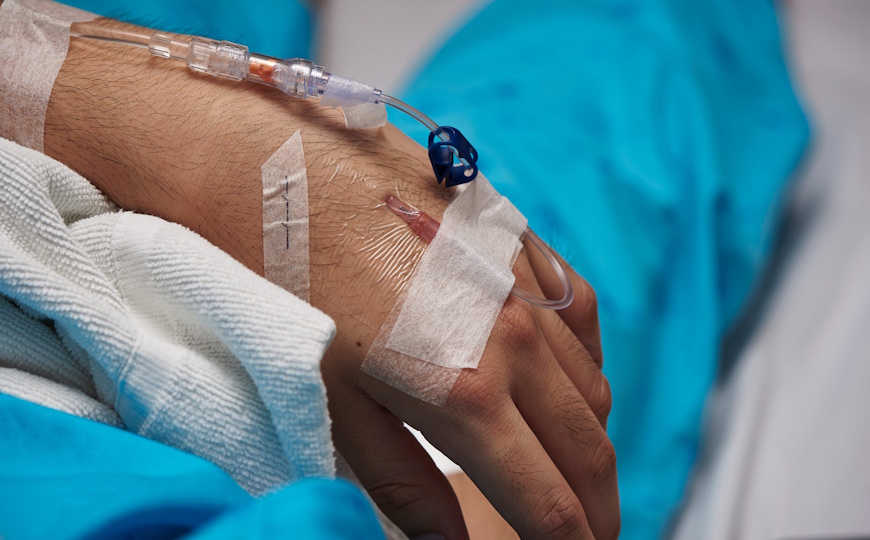
Персонализированный тест на чувствительность к терапии пембролизумабом завершил вторую фазу клинических исследований
Проспективное клиническое исследование показывает возможности технологии тестирования Signatera (производитель — компания Natera) в сопроводительной диагностике при иммунотерапии опухолей. Технология позволяет сделать вывод о том, эффективна ли терапия пембролизумабом, раньше, чем исследование других биомаркеров, и она применима к разным типам опухолей.
Credit:
Kateryna Kon | 123rf.com
Терапия онкозаболеваний при помощи ингибиторов контрольных точек (чекпойнт-ингибиторов) во многих случаях обеспечивает более высокую выживаемость больных и меньшую частоту нежелательных эффектов в сравнении с химиотерапией. Однако некоторые пациенты оказываются нечувствительны к иммунотерапии рака, и для них требуется подбор иных схем лечения. Фаза II клинического исследования INSPIRE (Study of the Effects of Pembrolizumab in Patients With Advanced Solid Tumors) показала высокую предиктивную эффективность персонализированного теста Signatera. Технология основана на определении ctDNA в плазме крови.
Исследование проводили в Канаде, в онкологическом центре Принцессы Маргарет (Торонто). Больных с распространенными солидными опухолями разделили на 5 когорт в зависимости от типа рака (плоскоклеточный рак головы и шеи, трижды негативный рак молочной железы, серозный рак яичников высокой степени злокачественности, злокачественная меланома; пятая группа включала пациентов с другими типами солидных опухолей). Пациентам была назначена терапия пембролизумабом (Китруда, Мерк). У всех участников взяли образцы опухолей и провели их полноэкзомное секвенирование. На основе полученных данных для каждого из 94 пациентов разработали персонализированный тест, включающий в себя определение до 16 соматических мутаций ctDNA. Первый тест провели до начала терапии и у 92 участников (98%) в плазме обнаружили ctDNA. У 73 пациентов образцы отбирали и в дальнейшем, на каждом из трех циклов лечения (начиная с 6–7-й недели иммунотерапии).
Исходная концентрация опухолевой ДНК в плазме коррелировала с выживаемостью без прогрессирования заболевания, общей выживаемостью, клиническим ответом. Дополнительную информацию давала динамика содержания ctDNA в плазме Так, у 30 из 73 больных уже после первого измерения было зафиксировано увеличение размера опухоли и концентрации ctDNA в плазме крове, и впоследствии все эти 30 пациентов оказались невосприимчивыми к терапии пембролизумабом. Двенадцать пациентов, у которых наблюдалось исчезновение ctDNA в образцах на том или ином этапе лечения (хотя бы один тест был отрицательным), прожили дольше. У этих пациентов медиана общей выживаемости, то есть срок, который пережила половина пациентов, достигла 25,4 месяца, тогда как у пациентов с ростом уровня ctDNA на любом этапе лечения — 13,7 месяца.
Авторы статьи отмечают, что уменьшение концентрации ctDNA — самый ранний предиктивный маркер положительного ответа на терапию. Так, у одного пациента ctDNA перестала определяться в образце уже через 4 месяца от начала терапии пербролизумабом, тогда как рентгенография опухоли показала положительный клинический ответ только спустя 8 месяцев. Отсутствие положительной динамики в концентрации ctDNA уже на 6-7 неделе лечения позволяет сделать вывод о целесообразности прекращения иммунотерапии и поиска иного лекарственного подхода для данного пациента. Кроме того, ctDNA может использоваться в качестве вспомогательного критерия для дифференциации истинной прогрессии опухоли от псевдопрогрессии.
Выгодное отличие ctDNA от других биомаркеров, таких как мутационная нагрузка опухоли или экспрессия опухолевой тканью лиганда к PD-1, — отсутствие зависимости между типом опухоли и прогностической значимостью маркера. Снижение уровня ctDNA коррелировало с положительным клиническим прогнозом у пациентов со всеми типами опухолей независимо от экспрессии PD-L1, микросателлитной нестабильности и мутационной нагрузки опухоли.
Авторы работы надеются, что технология Signatera найдет широкое применение для определения целесообразности терапии распространенных солидных опухолей ингибиторами контрольных точек.
Источник
Scott Bratman, et al. // Personalized circulating tumor DNA analysis as a predictive biomarker in solid tumor patients treated with pembrolizumab. // Nature Cancer, 2020; DOI: 10.1038/s43018-020-0096-5


 Меню
Меню





 Все темы
Все темы





 0
0