Плавательный пузырь рыбы помог восстановить сердце крысы после инфаркта
Инъекционные гидрогели из альгината — перспективный метод терапии ишемической сердечной недостаточности. Однако клинические испытания или не показали эффективности, или выявили высокие риски. Исследователи из Китая добавили к гидрогелю внеклеточный матрикс, полученный из плавательного пузыря рыб. По составу и микроструктуре плавательный пузырь похож на миокард, а его внеклеточный матрикс имеет низкую антигенность и богат белками, способствующими регенерации. У крысиной модели инфаркта миокарда такой гидрогель повысил фракцию выброса, улучшил ангиогенез и снизил количество воспалительных макрофагов в зоне поражения.
По данным ВОЗ, в 2019 году 56 млн людей страдали от сердечной недостаточности, с тех пор эта цифра только возросла. Примерно в 70% случаев речь идет об ишемической сердечной недостаточности, часто развивающейся после инфаркта миокарда; этот тип сердечной недостаточности имеет низкую пятилетнюю выживаемость. Установка стента может восстановить кровоток после инфаркта, но воссоздать отмершие ткани таким способом не получится. Из-за низкой способности взрослого сердца к регенерации поврежденный миокард заменяется фибробластами, что нарушает работу органа. После этого возможна только трансплантация, которая осложнена недостатком доноров и высокой стоимостью. Инъекционные гидрогели потенциально способны поддержать функции сердца, стимулировать регенерацию и уменьшить воспаление. Однако клинические испытания гидрогелей из альгината или не показали улучшений, или были ассоциированы с повышенными рисками для пациента. Специалисты связывают это с недостатками биоматериала и способа введения (в одном случае гидрогель вводили напрямую в миокард при открытой операции на сердце).
В исследовании, опубликованном в Advanced Science, группа ученых из Китая предложила новый тип биосовместимого гидрогеля, в состав которого входит внеклеточный матрикс (ECM), выделенный из плавательного пузыря рыбы. Этот материал обладает рядом преимуществ по сравнению с ECM, получаемым из тканей млекопитающих: имеет низкую антигенность и богат белками, способствующими регенерации. К тому же плавательный пузырь состоит из коллагена, гликозаминогликанов и эластина, по составу и микроструктуре он очень похож на миокард.
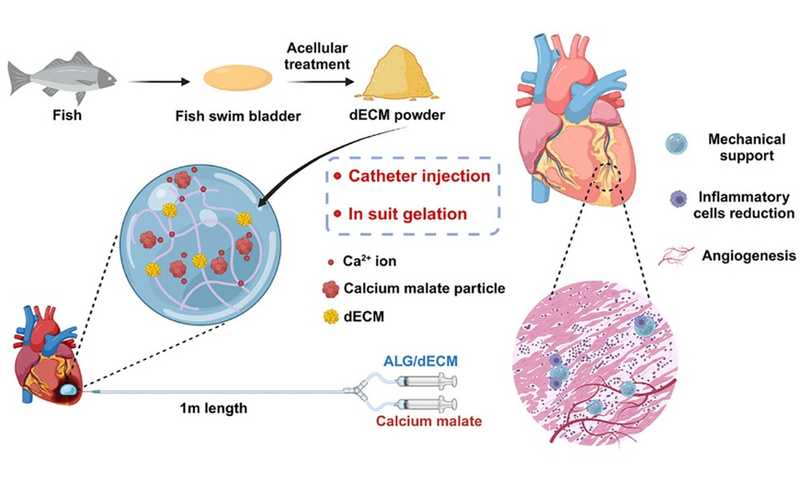
Процесс создания гидрогеля включал децеллюляризацию рыбьего плавательного пузыря с последующим измельчением ECM в порошок, который смешивали с раствором альгината. Малат кальция обеспечивал гелеобразование. Такой состав позволил достичь нужной вязкости, инъекционной способности и гелеобразования в пределах 5–6 минут, что является критически важным для транскатетерной доставки: материал должен оставаться жидким при прохождении через катетер, но быстро формировать гель после попадания в ткань сердца.
Авторы подтвердили устойчивость, стабильную структуру, биосовместимость и механическую прочность гидрогеля. В экспериментах in vitro ECM-гидрогель способствовал адгезии и выживанию кардиомиоцитов, стимулировал миграцию эндотелиальных клеток, образование капилляров, а также приобретение макрофагами противовоспалительного M2-фенотипа. Эти свойства особенно важны для восстановления поврежденной сердечной ткани, поскольку способствуют снижению воспаления и формированию новых сосудов в зоне ишемии. Гидрогель также обладал антиоксидантными свойствами и снижал уровни активных форм кислорода.
У крыс с инфарктом миокарда терапия с использованием гидрогеля значительно улучшила функции сердца. Через 28 дней после введения гидрогеля наблюдалось повышение фракции выброса на 9,3% по сравнению с контрольной группой, утолщение передней стенки левого желудочка, уменьшение зоны инфаркта (на 13,5%) и степени гипертрофии миокарда. Эти морфологические и функциональные изменения сопровождались улучшением ангиогенеза и снижением количества воспалительных макрофагов в зоне поражения.
С помощью РНК-секвенирования тканей миокарда исследователи обнаружили, что ECM-гидрогель влияет на экспрессию генов, связанных регенерацией, иммуномодуляцией и метаболизмом. В группе, получившей ECM, была значительно повышена экспрессия белка ANGPTL4, участвующего в регуляции липидного обмена, уменьшении окислительного стресса и защите кардиомиоцитов от липотоксичности, что может играть важную роль в восстановлении функции сердца.
Таким образом, гидрогель, в состав которого входит ECM из плавательного пузыря рыбы, обладает хорошими механическими и биологическими характеристиками, способствует иммуномодуляции и ангиогенезу, а также улучшает восстановление сердца после инфаркта у крыс. Также гидрогель можно использовать для менее инвазивной транскатетерной доставки в сердце, более удобной для клинического применения.
Инъецируемый гидрогелевый электрод восстановил проводимость поврежденного сердца у свиней
Источник:
Fu Y., et. al. Fish Swim Bladder-Derived ECM Hydrogels Effectively Treat Myocardial Ischemic Injury through Immunomodulation and Angiogenesis. // Advanced Science, 1-15 (2025), published online 9 April 2025. DOI: 10.1002/advs.202500036


 Меню
Меню





 Все темы
Все темы




 0
0











