«Побеление» жира вокруг сосудов повышает риск гипертензии
Известно, что ожирение — фактор риска гипертонии, однако точная связь между жировыми клетками и артериальным давлением пока не установлена. Авторы статьи в Science проанализировали периваскулярные жировые депо — естественные скопления адипоцитов вокруг сосудов. У человека в них присутствует бурый жир (отвечающий за термогенез), у мышей они во многом представлены бежевыми адипоцитами, которые имеют свойства как белого, так и бурого жира. Ученые показали на мышиной модели, что перепрограммирование жира в белый ассоциировано с ремоделированием сосудов, возникновением фиброза и гиперконтрактильностью, то есть факторами, способствующими повышению давления. Важную роль в этом играет секретируемый фермент QSOX1, экспрессия которого повышается в «побелевших» адипоцитах.
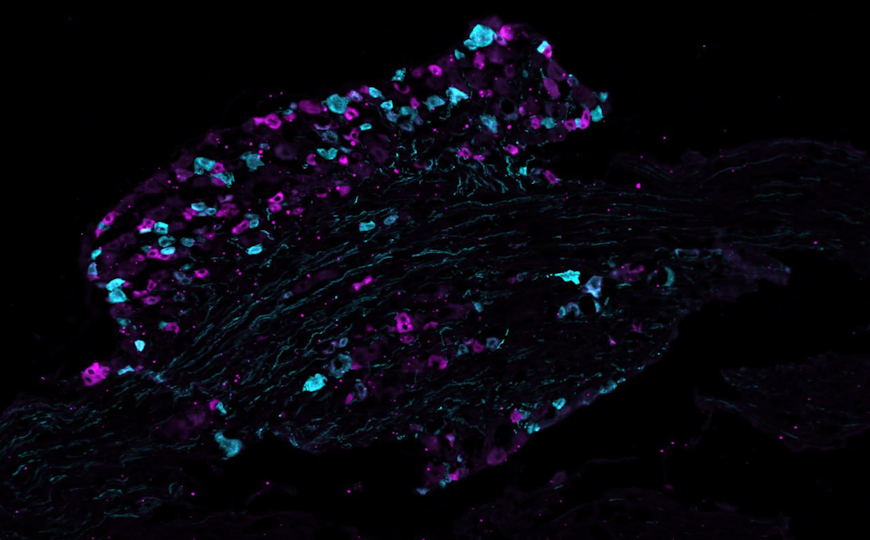
Иммунофлуоресцентное окрашивание аорты мыши и прилегающего к ней жира.
Credit:
Weslie R. and William H. Janeway Laboratory of Molecular Metabolism at The Rockefeller University |
пресс-релиз
Ожирение — фактор риска гипертонии и сердечно-сосудистых заболеваний, которые являются одной из ведущих причин смертности во всем мире. Однако биологическая основа связи между жировой тканью и кровяным давлением оставалась неуточненной. Интерес в этом контексте представляет, в частности, периваскулярная жировая ткань. По некоторым данным, она может обладать кардиопротекторными свойствами. Авторы статьи в Science углубились в этот вопрос и описали связь между фенотипом адипоцитов — белым, бурым или бежевым, — и влиянием периваскулярного жира на сосуды.
Жировая ткань, окружающая аорту, состоит из различных типов адипоцитов, в том числе бурых и бежевых. При этом периваскулярный бурый жир человека сильнее всего похож на бежевый жир у мышей, и авторы моделировали перестройки жировой ткани именно на этом ее подтипе. Уже было показано, что нокаут гена PRDM16 в бежевых адипоцитах приводит к потере идентичности — они снижают экспрессию разобщающего белка UCP1, необходимого для термогенеза, и приобретают черты белого жира. Ученые получили мышей с условным нокаутом Prdm16 в периваскулярном бежевом жире, чтобы выяснить, как ремоделирование адипоцитов влияет на состояние сосудов.
Брыжеечные артерии и сопротивление их стенок играют важную роль в регуляции артериального давления. Миография этих сосудов показала, что у мышей с нокаутом Prdm16 усиливалось их сокращение, опосредованное ангиотензином II. Миогенный тонус сосудов, их реакция на фенилэфрин или ацетилхолин не изменялись.
Секвенирование РНК единичных ядер (snRNA-seq) брыжеечных артерий и окружающей жировой ткани выявило 15 типов клеток. В их числе иммунные клетки (макрофаги, дендритные клетки, моноциты, Т- и В-лимфоциты), клетки сосудов (эндотелиальные, гладкомышечные и перициты) и прогениторные клетки, в том числе предшественники жировых, а также семь подтипов зрелых адипоцитов. Четыре из этих семи разновидностей существенно различались у нокаутных и контрольных мышей. Анализ транскриптов также показал, что при нокауте Prdm16 нарушается межклеточная коммуникация.
Ученые также выявили в транскриптоме признаки фиброза сосудов — одного из факторов риска гипертензии. В соответствии с этим, у мышей с нокаутом Prdm16 было повышено артериальное давление (как систолическое, так и диастолическое).
Чтобы выяснить, за счет чего адипоциты с дефицитом Prdm16 могут ремоделировать сосуды, авторы провели опыты в культуре клеток. Они обработали первичные гладкомышечные клетки аорты средой, в которой культивировали адипоциты. Культуральной жидкости от адипоцитов с нокаутом Prdm16 было достаточно, чтобы индуцировать экспрессию генов внеклеточного матрикса. Дальнейший анализ сигнальных пептидов выявил 12 генов-кандидатов, предположительно регулируемых Prdm16, которые могут секретироваться адипоцитами. Ключевым оказался Qsox1 — фермент, катализирующий образование дисульфидных мостиков во внеклеточном матриксе.
QSOX1 регулирует сборку внеклеточного матрикса, в том числе при раке, а полиморфизмы в его гене у человека ассоциированы с артериальным давлением. Кроме того, было показано, что у мышей с нокаутом Qsox1 давление снижено. Ученые решили проверить его роль в этом контексте и получили мышей с условным нокаутом Qsox1 в адипоцитах.
Сама по себе делеция Qsox1 в адипоцитах не повлияла на массу тела или жировой ткани, инсулинорезистентность или термогенез при стандартной диете, а также на работу сосудов. Однако при двойном нокауте — Prdm16 и Qsox1 — происходило «побеление» периваскулярного жира, аналогичное эффекту нокаута Prdm16. Оно сопровождалось снижением уровня UCP1 и усилением экспрессии маркеров белой жировой ткани.
Миография брыжеечных артерий не выявила различий между мышами с двойным нокаутом и контролем. Их сосуды не демонстрировали усиленных сокращений в ответ на ангиотензин II, в отличие от артерий животных с нокаутом только Prdm16. Кроме того, ученые убедились, что одновременная делеция Prdm16 и Qsox1 в адипоцитах предотвращала фиброз сосудов.
Исследователи предполагают, что, поскольку QSOX1 катализирует образование дисульфидных связей внутри и вне клетки, этот фермент может напрямую модулировать активность рецептора ангиотензина. Однако эта гипотеза требует экспериментальной проверки.
В целом работа показала, что секретируемый фермент QSOX1 начинает усиленно экспрессироваться бежевыми адипоцитами с дефицитом Prdm16 — то есть теми, которые перепрограммируются в белые жировые клетки. Это, в свою очередь, способствует гиперреактивности сосудов и их фиброзу, что нарушает регуляцию артериального давления и может приводить к гипертензии.
Источник
Mascha Koenen et al. Ablation of Prdm16 and beige fat identity causes vascular remodeling and elevated blood pressure. // Science 391, 306-313 (2026). DOI:
10.1126/science.ady8644


 Меню
Меню





 Все темы
Все темы




 0
0