Потенциальные мишени для борьбы со спастической параплегией 15 связаны с нейровоспалением
Спастическая параплегия 15 (SPG15) — одна из форм наследственных спастических параплегий, вызываемая мутациями в гене ZFYVE26 (SPG15), кодирующем белок спастизин. Исследование, опубликованное в Journal of Experimental Medicine, показало на мышиной модели, что при SPG15 происходит ранняя активация микроглии в центральной нервной системе (ЦНС) еще до заметной потери нейронов. Также идет экспансия, а затем и инфильтрация CD8+ T-клеток в ЦНС. Микроглия мыши приобретает фенотип, схожий с болезнь-ассоциированной микроглией, и начинает взаимодействовать с CD8+ T-клетками. Авторы наметили возможные пути для терапевтического вмешательства — восстановление гомеостаза микроглии, блокирование взаимодействия между микроглией и CD8+ T-клетками или истощение CD8+ T-клеток в мозге.
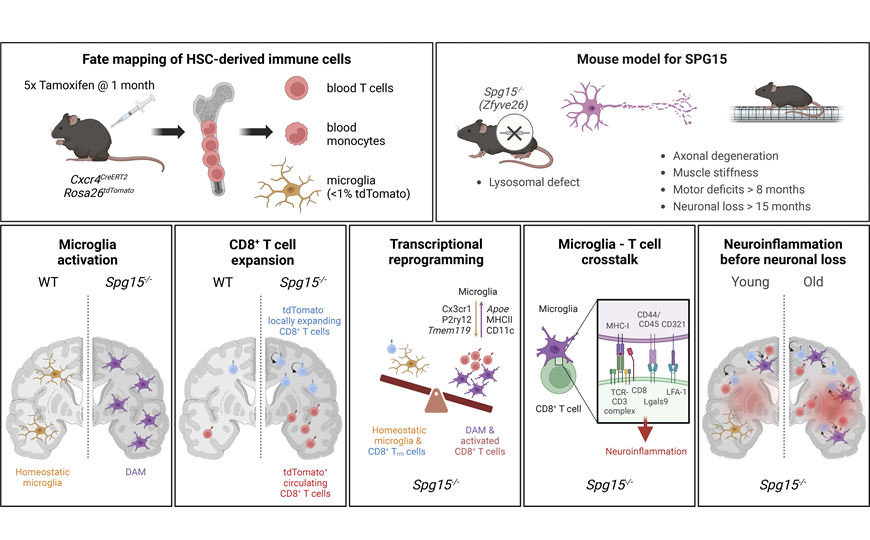
Frolov A., et al. // J Exp Med (2025), DOI: 10.1084/jem.20232357 | Creative Commons Attribution 4.0 International License
Наследственные спастические параплегии (НСП) представляют собой группу генетических заболеваний, поражающих двигательные нейроны и приводящих к прогрессирующей слабости и спастичности нижних конечностей. Несмотря на множество идентифицированных генетических причин, механизмы развития этих заболеваний остаются во многом неясными, что затрудняет разработку эффективных методов лечения. Исследование, опубликованное в Journal of Experimental Medicine, проливает свет на ранние патологические процессы, происходящие в центральной нервной системе (ЦНС) при одной из форм НСП, известной как спастическая параплегия 15 (SPG15).
SPG15 вызывают мутации в гене ZFYVE26 (SPG15), кодирующем белок спастизин. Они нарушают эндосомальный транспорт, биогенез лизосом и аутофагию — важные клеточные процессы, необходимые для нормальной работы нейронов. Исследователи использовали мышиную модель SPG15 (Spg15−/−), которая воспроизводит прогрессирующие двигательные нарушения и нейродегенерацию, наблюдаемые у людей.
Предыдущие исследования выявили признаки нейровоспаления при других типах НСП, включая SPG11. Чтобы выяснить, вовлечены ли иммунные клетки в патогенез SPG15, и если да, то на каких этапах заболевания, авторы провели детальный анализ клеточного состава ЦНС мышей Spg15−/− на разных стадиях жизни. Особое внимание уделялось микроглии — резидентным иммунным клеткам мозга — и T-лимфоцитам, играющим ключевую роль в иммунных реакциях.
В возрасте 12–15 месяцев у мышей еще не выявляется потеря нейронов в спинном и головном мозге, но она становится заметной в 15–18 месяцев. Интересно, что нарушения походки наблюдаются уже в 8–10 месяцев. Используя методы иммунофлуоресцентного окрашивания и проточной цитометрии, исследователи обнаружили раннюю активацию микроглии в спинном мозге и коре головного мозга мышей Spg15−/− еще до заметной потери нейронов. Активированная микроглия экспрессировала MHC-II, указывающий на ее вовлеченность в презентацию антигенов. Чтобы определить происхождение активированных клеток, ученые использовали генетический подход, позволяющий отслеживать клетки, происходящие из гемопоэтических стволовых клеток (HSC). Они показали, что активированная MHC-II+ микроглия была резидентными клетками мозга, а не мигрировала из периферической крови.
Дальнейший анализ с использованием РНК-секвенирования единичных клеток (scRNA-seq) выявил, что микроглия мышей Spg15−/− претерпевает трансформацию в состояние, напоминающее болезнь-ассоциированную микроглию (DAM). DAM характеризуется экспрессией специфических генов (Apoe, C1qb, Fth1) и потерей гомеостатических маркеров (P2ry12, Tmem119). Примечательно, что даже на ранних стадиях заболевания наблюдалась тенденция микроглии к переходу в DAM-подобное состояние.
Параллельно с активацией микроглии исследователи обнаружили увеличение количества CD3+ T-лимфоцитов в ЦНС мышей Spg15−/−. Дальнейший анализ показал, что среди инфильтрирующих T-клеток преобладали CD8+ T-лимфоциты, обладающие эффекторным фенотипом. Интересно, что fate-mapping эксперименты (отслеживания происхождения клеток) выявили, что ранний рост числа T-клеток в ЦНС происходит за счет рекрутирования и экспансии клеток, не происходящих из HSC, в то время как более поздняя инфильтрация включает происходящие из HSC клетки.
Используя методы визуализации и проточной цитометрии, ученые продемонстрировали возросшее взаимодействие между микроглией и CD8+ T-лимфоцитами в ЦНС мышей Spg15−/−. Анализ межклеточных взаимодействий с помощью программы CellChat позволил выявить потенциальные сигнальные пути, опосредующие коммуникацию между DAM-подобной микроглией и эффекторными CD8+ T-клетками.
Важно отметить, что, в отличие от некоторых других нейродегенеративных заболеваний и травм головного мозга, прогрессирование SPG15 у мышей не связано с инфильтрацией миелоидных клеток из периферической крови. То есть нейровоспаление при SPG15 в значительной степени обусловлено активацией резидентных иммунных клеток ЦНС и локальной экспансией T-клеток.
Авторы подчеркивают ключевую роль раннего нейровоспаления, опосредованного взаимодействием микроглии и CD8+ T-лимфоцитов, в патогенезе SPG15. Это открытие важно для понимания механизмов развития SPG15 и других сложных форм НСП. Авторы предполагают, что нарушение гомеостатических функций микроглии и взаимодействие с активированными CD8+ T-лимфоцитами могут лежать в основе сенсорных, когнитивных и двигательных нарушений, наблюдаемых при SPG15.
Также исследователи выявили потенциальную терапевтическую мишень — сеть коммуникаций между микроглией и CD8+ T-лимфоцитами. Будущие исследования, направленные на восстановление гомеостаза микроглии, блокирование взаимодействия между микроглией и CD8+ T-клетками или истощение CD8+ T-клеток в мозге, могут открыть новые пути для разработки противовоспалительных методов лечения, способных замедлить прогрессирование этого тяжелого наследственного заболевания. Дальнейшая валидация полученных результатов на человеческих образцах тканей мозга SPG15 и пациент-специфичных iPSC-моделях будет иметь решающее значение.
Найден новый ген, связанный с дегенерацией мотонейронов у человека
Источник:
Frolov A., et al. Microglia and CD8+ T cell activation precede neuronal loss in a murine model of spastic paraplegia 15. // J Exp Med 222 (7), e202323577 (2025), published online 23 April 2025. DOI: 10.1084/jem.20232357


 Меню
Меню





 Все темы
Все темы




 0
0









