Секвенирование длинных прочтений РНК выявило новые изоформы белков в клетках рака
Ученые из США разработали метод изучения альтернативного сплайсинга в клетках рака, основанный на секвенировании длинных РНК-ридов. С помощью нового метода они выявили новые сплайс-формы известных онкогенов и показали специфичность профилей альтернативного сплайсинга для разных подтипов рака молочной железы.
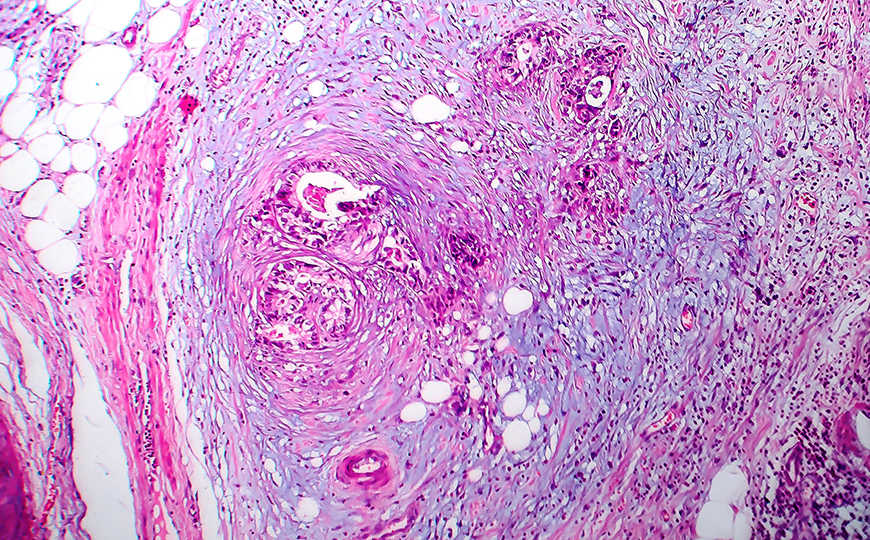
Секвенирование длинных РНК-ридов позволяет изучать альтернативный сплайсинг в опухолевых клетках. Метод разработали ученые из Джексоновской лаборатории геномной медицины (США) и рассказали о нем в Science Advances.
Репертуар белковых изоформ в человеческих опухолях отличается от такового в нормальных клетках. Это связано как с соматическими мутациями, так и с нарушениями регуляции альтернативного сплайсинга (AS). Изоформы белков могут способствовать онкогенезу, поэтому так важно иметь представление об AS-профилях в опухолевых клетках. Существующие каталоги AS-профилей составлены на основе данных секвенирования коротких фрагментов РНК, однако этот метод имеет ограничения. С его помощью можно собрать только 20–40% человеческого транскриптома.
Авторы новой работы создали метод анализа AS-профилей, основанный на секвенировании длинных фрагментов РНК, и проверили его на четырех образцах клеток нормальной молочной железы человека и 26 образцах опухолей молочной железы различных подтипов. Образцы включали как первичные ткани, так и клеточные линии. Секвенирование длинных РНК-ридов проводили на платформе PacBio. Полученные данные обрабатывали с помощью алгоритма ToFU.
Изоформы РНК определяли как известные или новые, накладывая их на референсный транскриптом GENCODE v.30. Доля новых изоформ в транскриптах каждого образца составила 17–55%. При этом изоформы, полученные из опухолевых образцов, кластеризовались отдельно от изоформ образцов нормальных клеток.
Изоформы происходили от 16 772 аннотированных генов и 905 неизвестных локусов. Две трети изоформ в опухолевых образцах были новыми, и 81% этих новых образцов детектировался в биопсийных тканях пациентов, что говорит о потенциальной клинической значимости таких исследований. Ученые показали, что 5’-области новых изоформ перекрываются с сайтами начала транскрипции, выявленные в независимых исследованиях методом CAGE, а также с областями открытого хроматина, указанными в The Cancer Genome Atlas. Это говорит о надежности нового метода.
Дальнейший анализ показал, что новые изоформы в основном ассоциированы с ключевыми молекулярными путями образования опухоли молочной железы: эстрогеновым и андрогеновым сигналингом, интерфероновым ответом, сигнальным путем mTORC1 и регуляцией веретена деления. Ученые выявили множество новых сплайс-форм NCOR1, GATA3, SPEN, PTEN и других генов, для которых характерны множественные мутации при раке молочной железы. Новые сплайс-формы соответствовали неизвестным ранее изоформам белков с предположительно измененной функцией и клеточной локализацией.
Наконец, ученые разработали смешанную гауссовскую модель (GMM) для кластеризации AS-профилей и применили его к транскриптомным данным по 1 135 образцам опухоли молочной железы и 1 443 образцам нормальной ткани из баз The Cancer Genome Atlas и Genotype-Tissue Expression. Они искали изоформы, выявленные в предыдущем эксперименте с помощью секвенирования длинных РНК-ридов. Было выделено 3 059 событий альтернативного сплайсинга, специфичных для опухоли. Из них 35 событий AS для 30 генов были ассоциированы с выживаемостью пациентов. Наиболее сильные ассоциации выявлены для альтернативного первого экзона CYB561, выпадающего экзона CEACAM1 и потери удерживаемого интрона в E2F4. Десять событий AS часто встречались в определенных подтипах рака молочной железы. Так, события, затрагивающие CYB561 и CEACAM1 характерны для HER2-положительного рака. При этом 21 событие из 35 AS отсутствовало в GENCODE v.30.
Таким образом, секвенирование длинных РНК-ридов выявило сложность и специфичность событие альтернативного сплайсинга при раке груди и подтвердило клиническую значимость новых изоформ. По мнению авторов, с помощью этого метода можно искать новые мишени для терапии рака.
Источник
Diogo F. T. Veiga, et al. A comprehensive long-read isoform analysis platform and sequencing resource for breast cancer. // Science Advances, 19 Jan 2022, Vol 8, Issue 3; DOI: 10.1126/sciadv.abg6711


 Меню
Меню





 Все темы
Все темы




 0
0











