Система OptoAAV доставляет генетический материал в единичные клетки
Система OptoAAV, основанная на аденоассоциированном векторе, селективно доставляет генетический материал в клетки при освещении красным светом. Такая система позволяет модифицировать определенный участок культуры клеток и производить генно-инженерные манипуляции с единичными клетками.
Аденоассоциированные векторы (AAV) — удобный инструмент для генетической инженерии эукариотических клеток. При этом возможности проводить с их помощью селективную модификацию определенных клеток или участков тканей ограничены. Коллаборация ученых из Германии и Китая разработала систему доставки генетической информации в клетки, активируемую красным светом, и назвали ее OptoAAV.
Системы доставки AAV при освещении пытались создать и раньше, но все они имели существенные недостатки, затрудняющие их использование. Некоторые из них требовали для активации ультрафиолет, опасный для клеток, другие — предварительную генетическую модификацию клеток для экспрессии фоторецептора.
OptoAAV лишена недостатков своих предшественников. Вектор модифицировали таким образом, чтобы он экспрессировал фитохром-связывающий фактор 6 (PIF6) из Arabidopsis thaliana, способный к распознаванию фитохрома B (PhyB). При воздействии красного света PhyB меняет свою конформацию и связывается с PIF6. Исходный поверхностный белок AAV изменили так, чтобы он потерял способность связываться с клеточным рецептором HSPG и заякориваться таким образом на клетке.
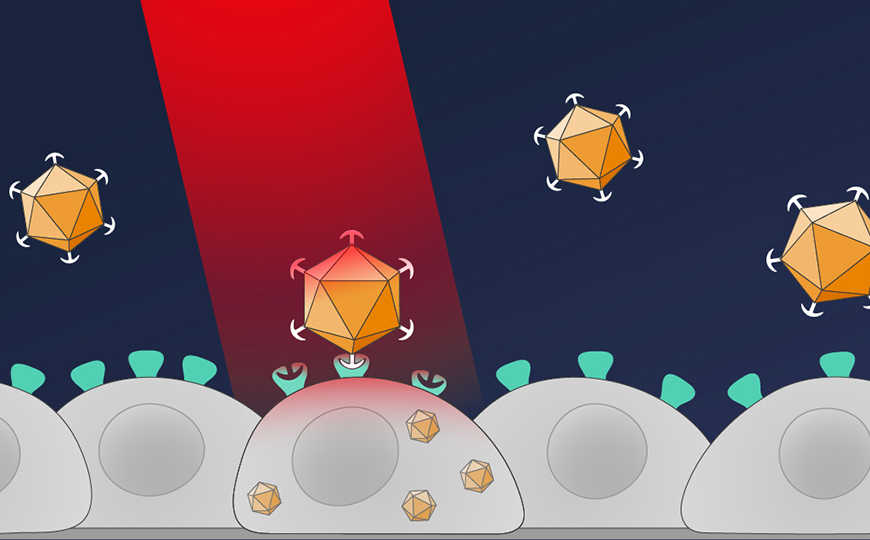
Для доставки OptoAAV в клетки требуется предварительный шаг — инкубация клеток с гибридным белком PhyB-DARPin. Во время инкубации DARPin связывается с рецептором эпидермального фактора роста EGFR, который экспрессируется во многих раковых клетках. В частности, его несут клетки линии эпидермоидного рака A-431, на которой исследователи опробовали свою систему. В результате на поверхности клеток закрепляется PhyB. AAV селективно связывается с клеткой за счет взаимодействия PIF6 с PhyB при освещении и эффективно трансдуцирует ее.
С использованием OptoAAV, несущей репортерный флуоресцентный белок, исследователи произвели последовательно две генно-инженерные манипуляции на одной и той же культуре клеток, закрывая от света разные участки культуры. Помимо этого, с использованием конфокальной микроскопии удалось модифицировать единственную клетку в культуре. Эффективность целевой трансдукции флуоресцентным белком в этом эксперименте составила 60%. Около 1% нецелевых клеток также флуоресцировали, но с меньшей интенсивностью.
OptoAAV можно адаптировать для использования с другими типами клеток, экспрессирующими иные, чем EGFR, рецепторы.
Модификация на уровне единственной клетки может быть использована, например, для изучения влияния гетерогенности клеток на биологические процессы. Для регенеративной медицины может представлять интерес введение факторов дифференцировки в различные участки ткани. Если систему удастся протестировать in vivo, область ее применения включит нейронауки и разработку генной терапии рака.
Источник
Hörner, M., et al. // Spatiotemporally confined red light-controlled gene delivery at single-cell resolution using adeno-associated viral vectors. // Science Advances, 7, 25, 16 Jun 2021; DOI: 10.1126/sciadv.abf0797


 Меню
Меню





 Все темы
Все темы




 0
0











