T-клетки, нацеленные на неоантигены, прошли фазу 2 КИ при метастатическом колоректальном раке
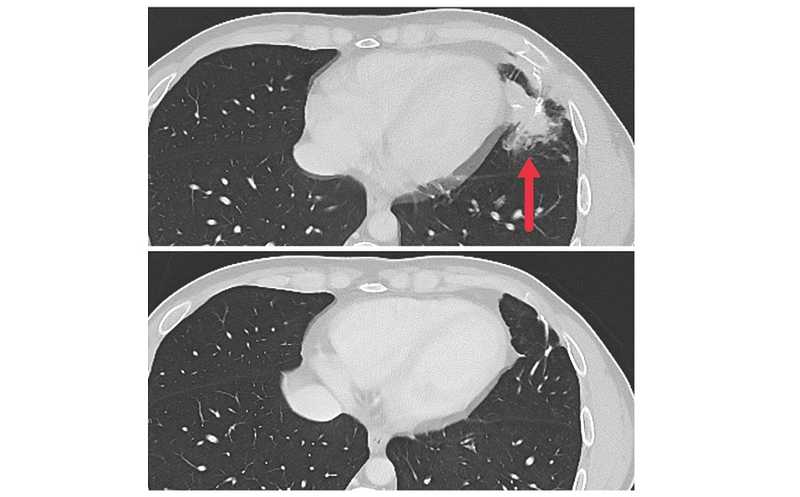
Группа исследователей из США представила данные фазы 2 клинических испытаний T-клеток для терапии метастатического колоректального рака. Эти T-клетки экспрессировали неоантиген-реактивные Т-клеточные рецепторы инфильтрирующих опухоль лимфоцитов. В исследование было включено семь пациентов; у трех значительно уменьшились метастатические очаги в печени, легких и лимфатических узлах на срок от четырех до семи месяцев.
Credit:
National Cancer Institute | Пресс-релиз
Неоантигены, возникающие в опухоли при накоплении генетических аномалий, — идеальная мишень для терапии, так как они не встречаются в здоровых тканях. Примерно у 80% пациентов с раками желудочно-кишечного тракта в опухолях выявляются неоантиген-реактивные T-лимфоциты (TIL, tumor-infiltrating lymphocytes). Терапия с помощью TIL показала обнадеживающие результаты при некоторых типах рака. Однако TIL представляют собой высоко дифференцированные клетки, и достижение необходимого для инфузии количества клеток является трудной задачей, сопряженной с их истощением. В новой статье, опубликованной в Nature Medicine, авторы представили результаты фазы 2 КИ аутологичных T-клеток, экспрессирующих неоантиген-реактивные Т-клеточные рецепторы (TCR), для терапии метастатического колоректального рака.
«Взяв естественные Т-клеточные рецепторы, которые присутствуют в очень небольшом количестве клеток, и поместив их в нормальные лимфоциты, которых у нас огромное количество, […] мы можем генерировать столько клеток, борющихся с раком, сколько захотим», — объясняет Стивен Розенберг из Национального института онкологии в Бетесде, один из руководителей исследования.
Для выявления неоантиген-реактивных TCR сначала проводилась резекция метастатического очага. Затем авторы изолировали лимфоциты из опухоли и провели полноэкзомное и транскриптомное секвенирование клеток периферической крови и опухоли для определения соматических мутаций. Затем TIL культивировали вместе с дендритными клетками, содержащими РНК тандемных минигенов или синтетические пептиды с обнаруженными мутациями, и с помощью флуоресцентно-активированного сортинга отбирали те Т-клетки, которые экспрессировали маркеры активации. Последовательности α- и β-цепей TCR отобранных Т-клеток вставляли в ретровирусные векторы, после чего проводили трансдукцию Т-клеток.
В клиническое испытание были включены семь пациентов с метастатическим колоректальным раком. Всем пациентам перед началом терапии проводилась лимфодеплетирующая химиотерапия с помощью циклофосфамида и флударабина. После инфузии T-клеток пациенты получали четыре дозы пембролизумаба каждые три недели и алдеслейкин — препарат рекомбинантного IL-2.
Трое пациентов достигли непродолжительного частичного ответа на терапию, выраженного в регрессии очагов метастазирования в печени, легких и лимфатических узлах. Медиана выживаемости без прогрессирования составила 4,6 месяца. Ответ на терапию зависел от источника неоантиген-реактивных TCR. Пять из семи пациентов получили TCR, выделенные из CD4+ T-клеток, только один из которых достиг частичного ответа на терапию. Оба пациента, получавших TCR, выделенные из CD8+ Т-клеток, достигли частичного ответа на терапию.
У одного пациента возник синдром высвобождения цитокинов. У всех пациентов развились цитопении, вызванные лимфодеплецией. У одного пациента развился диатез с кровотечением.
После инфузии T-клеток авторы проанализировали персистенцию клеток в крови пациентов. У двух пациентов, опухоли которых не ответили на терапию, не было обнаружено TCR-трансдуцированных клеток на 41 день после инфузии.
В будущем авторы планируют разработать протокол, который позволит получать T-клетки, нацеленные на десять неоантигенов, что сделает этот метод терапии более практичным и потенциально позволит преодолеть гетерогенность опухоли и иммунную резистентность.
Противоопухолевую активность CAR NK-клеток усиливает добавление к рецептору домена CD28
Источники:
Parkhurst M., et al. Adoptive transfer of personalized neoantigen-reactive TCR-transduced T cells in metastatic colorectal cancer: phase 2 trial interim results // Nat Med. 2024. DOI: 10.1038/s41591-024-03109-0
Цитата по пресс-релизу

 Меню
Меню





 Все темы
Все темы




 0
0









