Т-клетки, вызывающие аутоиммунное заболевание, могут быть трансформированы в терапевтические клетки
Терапевтическое применение регуляторных Т-клеток, за открытие которых присуждена Нобелевская премия 2025 года, затруднено тем, что их сложно получить в больших количествах. Журнал Science Translational Medicine опубликовал статьи одного из лауреатов — Симона Сакагути с соавторами, в которых описано получение регуляторных Т-клеток из обычных CD4+ T клеток разных подтипов. Наивные и эффекторные CD4+ Т-лимфоциты проще выделить, они лучше размножаются in vivo. Если они получены от пациента, то могут обладать специфичностью к интересующему антигену, то есть причина болезни превращается в терапевтическое средство. Индуцированные регуляторные Т-клетки, полученные по предложенному авторами протоколу, не теряли защитные свойства в течение долгого времени.
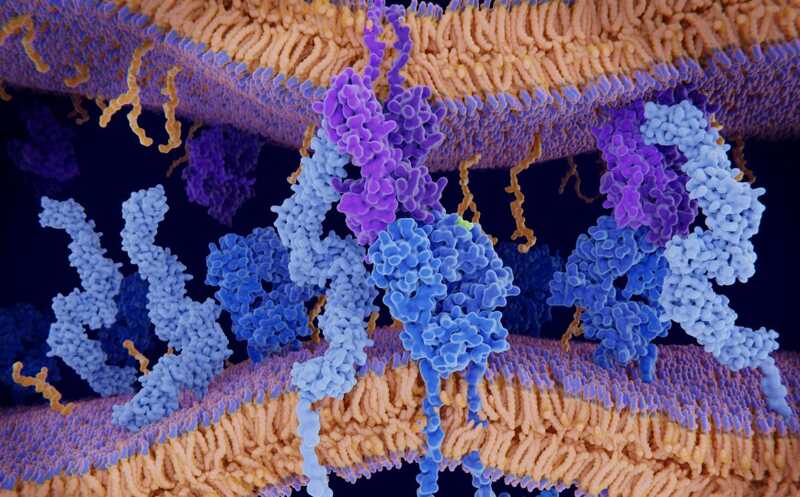
Презентация антигена (светло-зеленый) CD4+ Т-клетке
Credit:
123rf.com
Нобелевская премия по физиологии и медицине 2025 года была присуждена за открытие регуляторных Т-клеток (Treg), подавляющих аутоиммунные реакции. Один из лауреатов, Симон Сакагути из Университета Осаки, продемонстрировал существование регуляторных CD4+CD25+ Т- клеток в экспериментах на мышах. В свежем номере Science Translational Medicine опубликованы две статьи Симона Сакагути с коллегами, посвященные получению регуляторных Т-клеток in vitro для терапии аутоиммунных заболеваний. Это может стать важным шагом к их клиническому применению.
CD4+ и CD8+ Т-клетки атакуют молекулы и клетки, которые содержат антигены, распознаваемые их рецепторами, а регуляторные Т-клетки предотвращают атаку на антигены, которые распознают они (например, на эндогенные белки организма). Эта их способность предотвращать нападение иммунной системы на собственные органы и ткани перспективна для применения в терапии аутоиммунных заболеваний. Как и при получении других клеточных терапевтических препаратов, для этого можно взять клетки пациента или донора, нарастить их вне организма и вернуть в кровоток. Однако Treg встречаются в крови в небольших количествах и плохо растут in vitro.
Сакагути с коллегами пошли по другому пути: они получили регуляторные Т-клетки из других типов Т-клеток, тех, что вызывают иммунный ответ. Их проще культивировать, и кроме того, если получать их от пациента, они уже будут обладать специфичностью к тому самому антигену, иммунная атака на которой вызывает болезнь.
Если усилить в Т-клетке экспрессию гена Foxp3, за открытие которого присуждена Нобелевская премия другим лауреатам 2025 года, Мэри Брункоу и Фредерику Рамсделлу, то она превратится в индуцированную Т-регуляторную клетку (iTreg), способную подавлять иммунную реакцию. К сожалению, ненадолго: «Потеря экспрессии Foxp3 [происходит] за пару дней», — говорит соавтор второй из статей Масаюки Амагаи.
Японские исследователи предложили способ получения клеток, которые дольше сохраняют свойства iTreg. Этот способ описан в первой статье. Трансформацию успешно прошли различные типы Т-лимфоцитов — наивные и эффекторные/клетки памяти CD4+ T, в том числе TH1, TH2 и TH17.
Клетки стимулировали антигеном, TGF-бета, интерлейкином-2 (IL-2), а также добавляли ингибитор циклинзависимых киназ CDK8/19, усиливающий экспрессию Foxp3. Белок, кодируемый этим геном, подавляет выработку IL-2 и других противовоспалительных цитокинов и стимулирует экспрессию генной сигнатуры Treg — самого Foxp3, а также Il2ra и Ctla4. Замечательно, что ингибирование CDK8/19 одновременно блокирует дифференцировку Т-клеток в эффекторные, которая должна была бы произойти в присутствии провоспалительных цитокинов.
Кроме того, авторы индуцировали эпигенетические изменения в ДНК клетки (гипометилирование, модификации гистонов и ремоделирование хроматина, охватывающее энхансеры соответствующих генов), чтобы сделать трансформацию более продолжительной. Для этого отменяли костимуляцию рецептора CD28 моноклональными антителами во время индукции Treg.
Полученные клетки авторы ввели мышам, чувствительным к аутоиммунному воспалительному заболеванию кишечника, и подтвердили их защитные свойства, которые сохранялись даже шесть недель спустя — намного дольше, чем у клеток, полученных по более ранним протоколам. Эти клетки также подавляли реакцию «трансплантат против хозяина» у мышей. Наконец, авторы получили iTreg из человеческих Т-клеток, причем уровень конверсии составлял в среднем около 80%, а дополнительные модификации протокола подняли его до 90%.
Во второй статье Сакагути и Амагаи с коллегами исследовали потенциальные терапевтические свойства iTreg. Обыкновенная пузырчатка — редкое аутоиммунное заболевание, при котором на слизистой оболочке и кожи образуются заполненные жидкостью пузыри и эрозии, как при ожогах. При прогрессировании они распространяются по всему телу. До появления современных методов лечения кортикостероидами смертность от этого заболевания приближалась к 90%. Причина болезни — аутоиммунная реакция на эпидермальный белок клеточной адгезии десмоглеин 3 (Dsg3). Важно, что это единственный аутоантиген, вызывающий реакцию при данном заболевании.
Чтобы создать мышиную модель обыкновенной пузырчатки, авторы получили Т-клетки, таргетирующие Dsg3, от мышей, дефицитных по Dsg3 (Dsg3−/−), которых иммунизировали этим белком. Собранные клетки вводили мышам Rag2−/−, у которых нет собственных зрелых Т- и В-лимфоцитов.
Ранее авторы получили мышей Dsg3H1, которые экспрессировали Т-клеточный рецептор к Dsg3, полученный от патогенного клона CD4+ Т-клеток. От этих мышей можно было выделять большое количество Т-клеток, нацеленных на Dsg3 (по сути, именно такие клетки вызывают аутоиммунные реакции, приводящие к развитию обыкновенной пузырчатки). Эти клетки трансформировали в iTreg, вводили их мышам, моделирующим заболевание, и наблюдали подавление продукции аутоантител и развития повреждений кожи. Примечательно, что Т-клетки, полученные от обычных мышей и не нацеленные на Dsg3, оказались менее эффективными.
Исследователи также получили iTreg из клеток пациентов с обыкновенной пузырчаткой и показали, что добавление дексаметазона и цАМФ усиливает их иммуносупрессивное действие. По словам Амагаи, они уже начали адаптировать этот подход для клинических исследований, в которых прежде всего будет проверена его безопасность.
Этот подход можно использовать даже при идиопатических заболеваниях, когда неизвестно, какой антиген вызывает иммунную реакцию, подчеркивают авторы. В крови людей с аутоиммунным заболеванием всегда много Т-клеток, распознающих этот антиген, соответственно, полученные из них iTreg будут подавлять иммунную реакцию именно на него.
Источники
Norihisa Mikami, et al. Generating functionally stable and antigen-specific Treg cells from effector T cells for cell therapy of inflammatory diseases // Science Translational Medicine. 22 Oct 2025. Vol 17, Issue 821. DOI: 10.1126/scitranslmed.adr6049
Miho Mukai, et al. Conversion of pathogenic T cells into functionally stabilized Treg cells for antigen-specific immunosuppression in pemphigus vulgaris // Science Translational Medicine. 22 Oct 2025. Vol 17, Issue 821. DOI: 10.1126/scitranslmed.adq9913


 Меню
Меню





 Все темы
Все темы




 0
0