Трансплантат из смеси гепатоцитов с гелевыми микросферами может помочь при печеночной недостаточности
Исследователи из Массачусетсткого технологического института (США) предложили новый способ формирования трансплантата, содержащего гепатоциты, — инъекцию смеси донорских гепатоцитов, фибробластов и микросфер из гидрогеля. Клетки в таком трансплантате, введенные в жировую ткань мышей, сохраняли жизнеспособность и активность не менее двух месяцев. Авторы исследования допускают, что подобная «инъекция печени» не только позволит пациенту дождаться донорского органа, но, возможно, заменит трансплантацию.
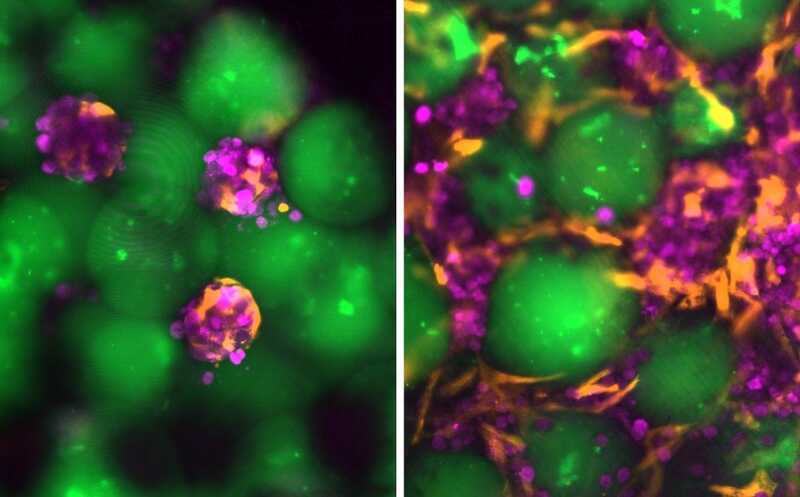
Гелевые микросферы (зеленые), гепатоциты (малиновые) и фибробласты (оранжевые) формируют мини-печень. Слева — нулевой день культивирования in vitro, справа 14-й.
Credit:
Bhatia Lab | Пресс-релиз
Пациентам с хроническими заболеваниями печени может помочь трансплантация, однако донорских органов не хватает, кроме того, операция по пересадке печени достаточно тяжелая, и не каждый пациент может ее перенести. В качестве решения рассматривается трансплантация донорских гепатоцитов, которая, если и не заменит полностью функцию печени, может позволить человеку с печеночной недостаточностью дождаться очереди на трансплантацию.
Исследователи из Массачусетского технологического института разработали «мини-печени», которые можно вводить в организм инъекционно. В экспериментах на мышах они показали, что введенные в организм гепатоциты, смешанные с микрошариками из модифицированного желатина и фибробластами, могут оставаться жизнеспособными по меньшей мере два месяца и при этом вырабатывают ферменты и другие белки, которые производит печень. Результаты исследования опубликованы в журнале Cell Biomaterials.
В последнее десятилетие сотрудники лаборатории Сангиты Бхатии из МТИ работают над способами восстановления функции печени без трансплантации донорского органа. Инъекции гепатоцитов — перспективный подход, однако выживаемость в организме клеток, не имеющих определенной ниши, как правило, низкая, поэтому рассматриваются варианты, связанные с инкапсулированием клеток в гель.
В новой статье исследователи предлагают вводить клетки печени в смеси с микросферами гидрогеля, которые бы удерживали их вместе и способствовали васкуляризации (прорастанию сосудов). Гранулированные гидрогели при инъекции ведут себя как жидкость, но в тканях образуют включение с фиксированной формой — каркас, который обеспечивает клеткам механическую поддержку и в то же время не препятствует интеграции с организмом.
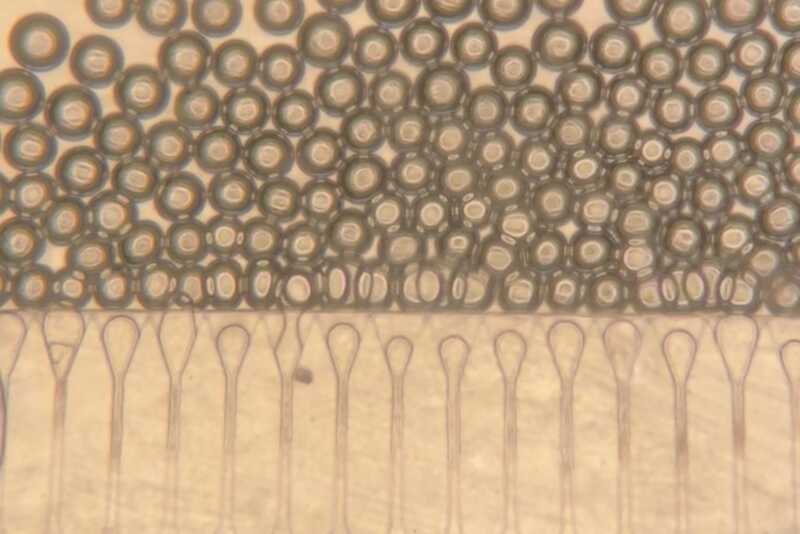 Гидрогелевые микросферы для мини-печеней получали в микрофлюидном устройстве эмульгированием водных капель в масляной фазе с последующим воздействием УФ. Credit: Bhatia Lab
| Пресс-релиз
Гидрогелевые микросферы для мини-печеней получали в микрофлюидном устройстве эмульгированием водных капель в масляной фазе с последующим воздействием УФ. Credit: Bhatia Lab
| Пресс-релиз
Изучается использование таких гидрогелевых имплантов для ускорения заживления ран: клетки хозяина мигрируют между сферами и формируют новую ткань. В новом исследовании гранулированный гель аналогичным образом «заселялся» донорскими гепатоцитами. В состав смеси также входили человеческие фибробласты, которые способствовали образованию стабильной структуры, выживанию гепатоцитов и росту кровеносных сосудов.
«Если клетки вводить без этих микросфер, они не будут эффективно интегрироваться в организм хозяина, но эти микросферы обеспечивают гепатоцитам нишу, в которой они могут оставаться локализованными и гораздо быстрее подключаться к кровообращению», — говорит первый автор статьи Вардхман Кумар.
Микросферы состояли из химически модифицированного желатина — желатинметакрилоила (GelMA), применяемого в 3D-биопечати. Смесь клеток и микросфер вводили мышам иммунодефицитной линии в жировую ткань живота: ранее авторы установили, что в жировой ткани клетки выживают лучше, чем при подкожном введении. Для контроля инъекции и последующего мониторинга использовали УЗ-визуализацию. Авторы отмечают, что трансплантат не обязательно должен находиться рядом с печенью, локализации могут быть различными.
Клетки образовали стабильную компактную структуру, со временем в ней сформировались сосуды (в то же время при использовании негранулированного геля того же состава васкуляризации не происходило). После инъекции гепатоциты как минимум восемь недель оставались жизнеспособными и выделяли специализированные белки в кровоток. Авторы также отмечают, что степень биоразлагаемости желатиновых микросфер можно регулировать; ее повышение может улучшить функции трансплантата.
Продолжительная жизнеспособность гепатоцитов говорит о том, что подобный малоинвазивный подход может не только применяться во время ожидания трансплантации, но, возможно, и станет альтернативой трансплантации, утверждают исследователи.
Получение гепатоцитов из индуцированных плюрипотентных стволовых клеток самого пациента пока сопряжено с проблемами, хотя некоторые успехи в этом направлении достигнуты. Если же гепатоциты будут донорскими, то пациентам придется принимать иммуносупрессивные препараты. Однако исследователи изучают возможность разработки «незаметных» гепатоцитов, не вызывающих атак иммунной системы, или использования тех же гидрогелевых микросфер для локальной доставки иммуносупрессантов.
Авторы отмечают, что предложенную ими технологию, которую они назвали INSITE (injected, self-assembled, image-guided tissue ensembles), можно распространить на другие клеточные терапии, включая трансплантацию островковых клеток поджелудочной железы для лечения диабета.
Женщина с диабетом не нуждается в инсулине после трансплантации островков из ее собственных клеток
Гепатоциты для лечения печеночной недостаточности можно получать из химерных животных
Источники
Vardhman Kumar, et al. Image-guided injectable niche for hepatocyte transplantation // Cell Biomaterials. Published online March 3, 2026. DOI: 10.1016/j.celbio.2026.100378
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0











