В диффузных крупноклеточных B-клеточных лимфомах идентифицировали семь различных микросред
Составлено наиболее подробное на сегодня описание пространственной организации клеток в диффузных крупноклеточных В-клеточных лимфомах — одном из самых распространенных видов лимфом. Исследование, выполненная с применением методов пространственной транскриптомики и протеомики, показала, что опухолевая ткань состоит из клеточных ниш — микроскопических сообществ, в которых соседствуют и взаимодействуют различные типы клеток иммунной системы и опухолевые В-клетки. Эти ниши отличаются по составу и характеру межклеточных связей и могут определять некоторые особенности ответа опухолей на иммунотерапию.
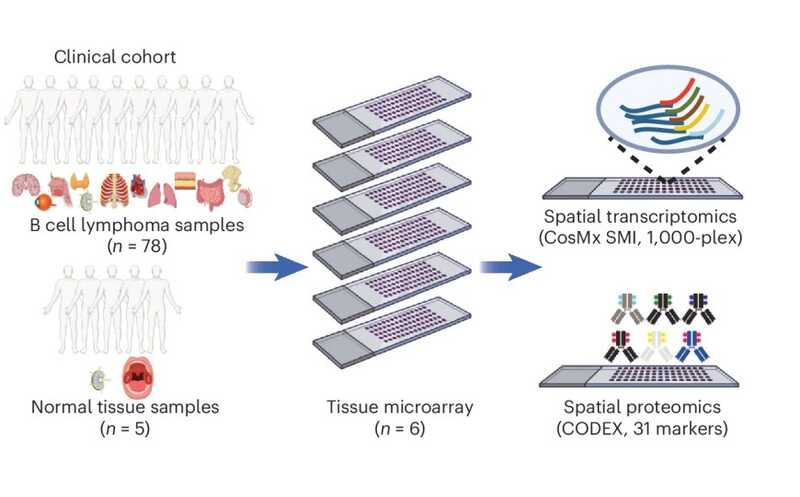
Nat Genet (2025). DOI: 10.1038/s41588-025-02353-5 | CC BY NC ND 4.0
Исследователи из Онкологического центра М.Д. Андерсона и компании BostonGene, которая занимается молекулярным и иммунным профилированием опухолей, изучили структуру микроокружения диффузных крупноклеточных В-клеточных лимфом на уровне отдельных клеток и выявили ассоциации этой структуры с клиническими параметрами.
Диффузные крупноклеточные B-клеточные лимфомы (ДКВКЛ) представляют собой гетерогенную группу агрессивных опухолей из зрелых B-лимфоцитов. Хотя химиоиммунотерапия первой линии эффективна для большей части пациентов, примерно у 40% имеет место рефрактерное или рецидивирующее течение заболевания. В последние годы благодаря использованию CAR-T-терапии и биспецифических антител удалось достичь улучшения прогноза у таких пациентов, однако в некоторых случаях лечение все еще оказывается неэффективным.
Одной из причин значительной вариабельности в течении заболевания могут быть различия в микроокружении опухолей — качественном и количественном составе нормальных клеток организма и характере их локального взаимодействия со злокачественными клетками. ДКВКЛ, как правило, развиваются в лимфатических узлах — органах, архитектура которых ориентирована на поддержание связей между лимфоцитами, антиген-презентирующими клетками и другими миелоидными клетками, соединительной тканью и кровеносными сосудами. При возникновении лимфомы нормальная архитектура лимфатического узла разрушается, однако в ткани сохраняются многие типы клеток, влияющих на развитие опухоли.
Более ранние исследования показали, что ДКВКЛ у разных пациентов характеризуются различными паттернами организации микроокружения. Свойства микроокружения зависят от происхождения и мутационного профиля клеток опухоли — они также могут быть ассоциированы с исходом заболевания.
Чтобы понять, как формируется реактивное микроокружение ДКВКЛ, авторы статьи в Nature Genetics применили технологии пространственной транскриптомики (NanoString CosMx) в совокупности с протеомными (CODEX) и геномными методами исследования. В исследование включили образцы от 78 пациентов с различными формами ДКВКЛ, включая EBV-позитивные лимфомы (то есть с признаками инфицирования клеток вирусом Эпштейна — Барр).
Авторы идентифицировали 19 различных клеточных состояний, в том числе опухолевые В-клетки, разнообразные подтипы макрофагов и плазматических клеток, Т-лимфоциты, стромальные, эндотелиальные и другие клетки. Учитывая, что специализированные клетки в тканях группируются вместе, формируя функциональные единицы, ученые провели анализ соседства (neighborhood) клеток и выделили семь так называемых клеточных ниш (cellular niches, CN), каждая из которых характеризовалась преобладанием определенного типа клеток. Одни ниши были обогащены T-лимфоцитами, другие — миелоидными клетками, стромальными клетками, плазматическими клетками; некоторые ниши состояли преимущественно из опухолевых клеток. Также авторы выделили те ниши, в которых множественные диффузно расположенные опухолевые клетки были перемешаны с разнообразными иммунными клетками, и те, в которых среди гетерогенных скоплений неопухолевых клеток встречались единичные опухолевые.
Интересно, что результаты этого этапа имели мало общего с выводами более ранних исследований, где применялись «старые» методы РНК-секвенирования без учета взаиморасположения клеток в пространстве. Это подчеркивает, что пространственная транскриптомика является более точным методом исследования клеточных ниш в опухолях.
Особое внимание исследователи уделили тому, как внутри разных ниш ведут себя Т-лимфоциты. В зонах, богатых Т-клетками, они сохраняли признаки активных и «здоровых» наивных клеток и клеток памяти, демонстрировали высокий уровень цитотоксических молекул и слабую экспрессию маркеров истощения. В нишах, где преобладали миелоидные клетки (в частности, макрофаги) или опухолевые В-клетки, Т-клетки, напротив, проявляли признаки дисфункции и истощения. Такие различия отражали неравномерное распределение сигнальных молекул: в богатых T-лимфоцитами «здоровых» были выявлены признаки активного хемокинового сигналинга, привлекающего Т-клетки, а в обогащенных опухолевыми клетками преобладали супрессорные взаимодействия (в том числе PD-1—PD-L1).Отдельные типы ДКВКЛ демонстрировали специфические паттерны организации клеточных ниш. Так, EBV-ассоциированные лимфомы содержали меньше опухолевых В-клеток и больше Т-клеток и состояли преимущественно из богатых T-лимфоцитами и смешанных ниш. Несмотря на высокий уровень экспрессии цитотоксических молекул, эти Т-клетки (в отличие от T-лимфоцитах, которые присутствовали в таких нишах в EBV-негативных лимфомах) одновременно экспрессировали маркеры хронического истощения — признак того, что они постоянно активированы вирусными антигенами и осуществляют «надзор» за зараженными B-лимфоцитами, но неспособны полностью уничтожить опухоль. Это указывает на возможную чувствительность EBV-положительных ДКВКЛ, имеющих плохой прогноз, к иммунотерапии.
Не менее интересные результаты были получены для лимфом так называемых иммунопривилегированных зон — головного мозга, яичек и глаз, куда обычно ограничен приток иммунных клеток. Несмотря на это, такие опухоли демонстрировали значительную инфильтрацию Т-лимфоцитами. Эти клетки активно делились и экспрессировали цитотоксические маркеры, но кроме того, экспрессировали так называемые ингибирующие рецепторы (LAG3, HAVCR2, PDCD1, ENTPD1), являющиеся маркерами T-клеточной дисфункции. Исследователи предполагают, что такие опухоли тоже могут хорошо реагировать на иммунотерапию.
«Идентификация “карманов” в ткани опухоли, где T-лимфоциты уже активированы, дает нам понятные мишени для разработки терапии, стимулирующей собственную иммунную систему пациента, наряду с препаратами, нацеленными на уничтожение клеток опухоли», — комментирует Линхуа Ван, одна из руководительниц исследования.
Будущие исследования в этом направлении должны использовать более крупные и «информативные» фрагменты опухолевой ткани вместо тканевых микроматриц и связать влияние микроокружения с клиническим исходом заболевания.
B-клеточная лимфома ускоряет старение иммунных клеток, особенно в молодом организме
Источник
Dai, Y., et al. Multi-modal spatial characterization of tumor immune microenvironments identifies targetable inflammatory niches in diffuse large B cell lymphoma. // Nature Genetics (2025). DOI: 10.1038/s41588-025-02353-5


 Меню
Меню





 Все темы
Все темы




 0
0