В повышении риска тяжелого COVID-19 при ожирении и диабете обвинили бактерии
В журнале eLife опубликована статья, в которой разбираются механизмы взаимодействия коронавируса SARS-CoV-2 и бактерий человеческого микробиома, объясняющие тяжелое протекание COVID-19 при диабете и ожирении.
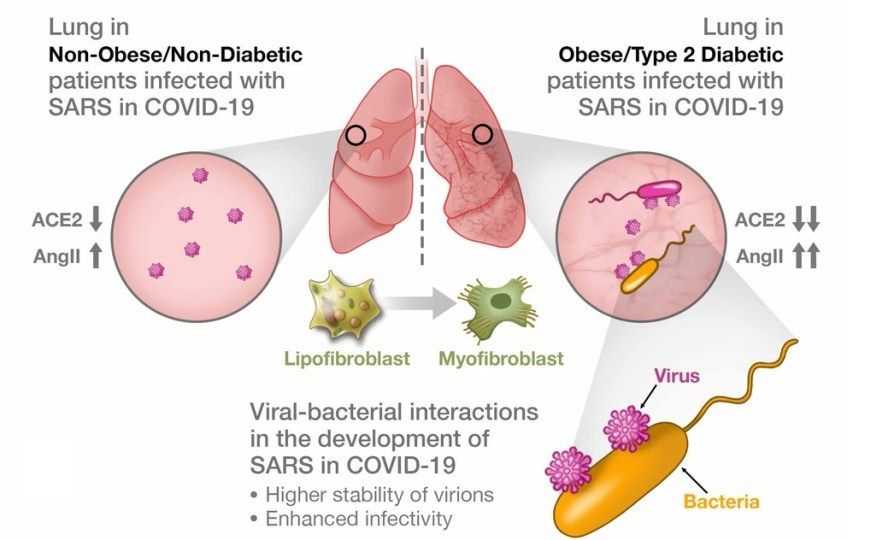
Kruglikov, et al., 2020; DOI: 10.7554/eLife.61330 | CC BY 4.0
Известно, что люди с ожирением и сахарным диабетом 2 типа намного более склонны к тяжелому течению COVID-19 и развитию различных осложнений. Ученые из Германии и США считают, что причина этого кроется во взаимовлиянии коронавируса SARS-CoV-2 и кишечных бактерий.
Известно, что в жировой ткани активно экспрессируется ангиотензинпревращающий фермент 2 (ACE2), с помощью которого вирус проникает в клетку. Это значит, что адипоциты могут быть резервуаром SARS-CoV-2, увеличивая локальную вирусную нагрузку. Также показано, что коронавирус может активировать гены, связанные с метаболизмом липидов в эпителии легких. Кроме того, интенсивное связывание SARS-CoV-2 с ACE2 приводит к дефициту последнего и разбалансировке ренин-ангиотензиновой системы (РАС).
В новом обзоре исследователи выдвинули теорию, согласно которой бактерии человеческого мекробиома и продукты их жизнедеятельности при ожирении и сахарном диабете 2 типа синергетически усиливают действие коронавирусной инфекции. Как это происходит?
Экспрессия ACE2 влияет на транспорт аминокислот и выработку антимикробных пептидов, что уже в значительной мере определяет состав микробиоты. При ожирении и диабете 2 типа ухудшаются барьерные функции слизистой оболочки кишечника, в результате чего бактерии и продукты их жизнедеятельности (в том числе липополисахариды) попадают в кровоток. Распространяющиеся по кровеносной системе бактерии и их токсины попадают не только в легкие, но и в жировую ткань, что подтверждается сообщениями об обнаружении бактерий и бактериальной ДНК в различных жировых депо организма.
Увеличение циркулирующих в крови липополисахаридов приводит к накоплению эндотоксинов в тканях легких, это активирует воспалительные процессы и становится причиной повреждения сосудов. В то же время SARS-CoV-2 взаимодействует с липополисахаридами, что повышает эффективность его связывания с АСЕ2 и инфекционность. Развивается локальный дефицит ACE2 в тканях легких, дисбаланс между агентами РАС, вызывающими сужение и расширение сосудов, и как результат — усиления воспалительных процессов.
Одновременное действие коронавируса и бактерий вызывает гиперцитокинемию — патологический выброс провоспалительных цитокинов, по масштабам намного превышающий ответную реакцию организма на действие одного лишь вируса или только бактериальной инфекции.
Известно, что коронавирусы модифицируют адипоциты и адипоцитоподобные клетки, переводя их в состояние дифференцировки. Показано, что при тяжелых формах болезни сходные процессы протекают и в легких: происходит активизация трансдифференцировки липофибробластов в миофибробласты, что приводит к фиброзу.
«Хотя все эти потенциальные механизмы могут увеличивать тяжесть течения COVID-19, мы считаем, что преобладает только один из них, и этот механизм должен работать не только у пациентов с ожирением и диабетом, но и у людей из других групп повышенного риска, в том числе у пожилых, — пишут ученые. — Наша теория подтверждается экспериментами, показывающими, как сочетание бактериальной и вирусной инфекции приводит к так называемому цитокиновому шторму, характерному для COVID-19».
Исследователи подчеркивают, что хотя сами по себе перечисленные механизмы не являются специфичными только для SARS-CoV-2, тем не менее, из-за высокого сродства вируса к ACE2 они приводят к намного более тяжелым последствиям, чем при других инфекциях.
Источник
Kruglikov IL, Shah M, Scherer PE. // Obesity and diabetes as comorbidities for COVID-19: Underlying mechanisms and the role of viral-bacterial interactions. // Elife. 2020;9:e61330. Published 2020 Sep 15; DOI: 10.7554/eLife.61330


 Меню
Меню





 Все темы
Все темы




 0
0











