Вакцина против мутантного белка KRAS предотвращает рецидив при раке поджелудочной железы и колоректальном раке
Противораковая вакцина ELI-002 2P компании Elicio Therapeutics вызвала сильный иммунный ответ у пациентов с раком поджелудочной железы и колоректальным раком. Она нацелена на мутантные формы белка KRAS. Это стандартизированный, а не индивидуальный продукт, то есть вакцина может быть назначена разным пациентам с мутациями, затронувшими KRAS. В фазе 1 клинического исследования участвовали 25 пациентов, перенесших операцию по удалению опухоли. У шести человек опухолевые биомаркеры полностью исчезли, у 21 появились Т-клетки, специфичные к KRAS.
Вакцина, которая нацеливает клетки иммунной системы на мутантные формы белка KRAS, показала обнадеживающие результаты в исследовании, включающем 25 пациентов с раком поджелудочной железы или колоректальным раком.
При раке поджелудочной железы рецидив после стандартного лечения практически неизбежен, а лечение после рецидива в основном паллиативное; пятилетняя выживаемость составляет около 23%. Драйверные мутации KRAS, способствующие прогрессированию опухоли, встречаются примерно в 20–25% опухолей человека. При колоректальном раке и протоковой аденокарциноме поджелудочной железы их частоты еще выше (50% и 93%).
Мутации KRAS — привлекательные неоантигены для разработки противораковых вакцин: они не только широко распространены, но и распознаются различными аллелями HLA, что позволяет создать вакцину, подходящую для большого числа пациентов.
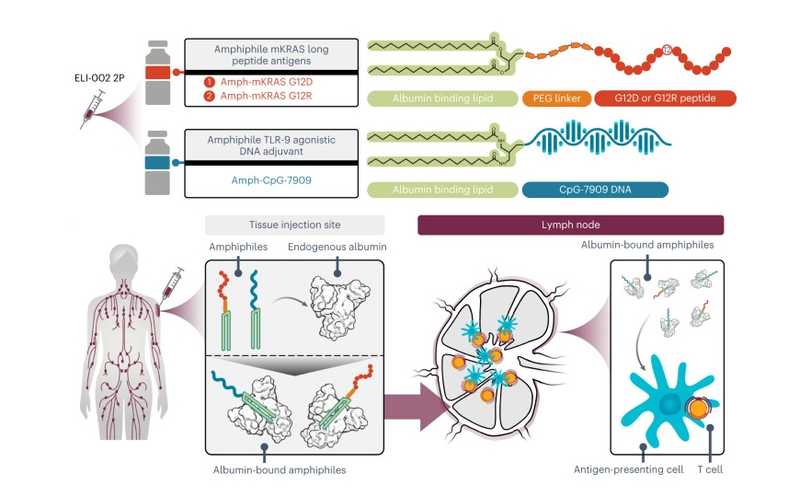
Обычные иммуногены в составе вакцин, включая пептидные антигены, плохо проникают в лимфатические узлы, где их поглощают антигенпрезентирующие клетки. В вакцине ELI-002 2P бостонской компании Elicio Therapeutics, используется платформа Amphiphile (AMP), разработанная в Массачусетском технологическом институте. К пептидам мутантного KRAS в составе вакцины ELI-002 2P ковалентно присоединены диацильные липиды, который, в свою очередь, связывается с эндогенным сывороточным альбумином. Присоединение к крупной белковой молекуле обеспечивает доставку в лимфоузлы. Также вакцина содержит ДНК агониста Toll-подобного рецептора 9 (TLR9), модифицированную аналогичным образом, в качестве адъюванта.
В январе 2024 года уже были представлены предварительные результаты фазы 1 клинического исследования AMPLIFY-201 с участием 25 пациентов. У 20 из них была протоковая аденокарцинома поджелудочной железы, у пяти — колоректальный рак; медианный возраст участников в начале исследования — 61 год. Все они перенесли операцию, и у всех появились признаки минимальной остаточной болезни, указывающие на рецидив (присутствие сывороточного опухолевого антигена или циркулирующей опухолевой ДНК). Каждому пациенту сделали серию инъекций препарата ELI-002 2P с постоянной дозой пептида и возрастающей дозой адъюванта. Новая публикация представляет обновленные данные после более продолжительного наблюдения за пациентами (медианное время 19,7 месяцев).
Как и в предыдущей работе, у 84% пациентов (21 из 25) присутствовали KRAS-специфические Т-лимфоциты; у 71% были как хелперные CD4+ клетки, так и цитотоксические CD8+ клетки. У многих эти клетки выявлялись в течение длительного времени.
В новой работе авторы отдельно рассматривали пациентов с высоким и низким Т-клеточным ответом (выше и ниже порогового значения). В группе пациентов с высоким Т-клеточным ответом у шести (три человека с раком поджелудочной железы и три с колоректальным раком) исчезли опухолевые биомаркеры в крови. В группу с низким Т-клеточным ответом попали 8 человек, у всех наблюдалось рентгенологическое прогрессирование, и выживаемость в этой группе была низкой. Также после вакцинации у многих участников появился клеточный иммунный ответ на другие опухолевые антигены, которых не было в вакцине.
Медиана безрецидивной выживаемости, рассчитанная для всех 25 пациентов, составила 16,33 месяца, а медиана общей выживаемости — 28,94 месяца. Тот и другой показатель выше, чем известные из литературы. У пациентов с более высоким Т-клеточным ответом медианы безрецидивной выживаемости и общей выживаемости не были достигнуты, то есть у очень многих пациентов рак все еще отсутствовал,
«Воздействие на KRAS долгое время считалось одной из сложных задач в терапии рака, — говорит первый автор исследования Зев Вайнберг из Калифорнийского университета в Лос-Анджелесе. — Это исследование показывает, что вакцина ELI-002 2P может безопасно и эффективно обучать иммунную систему распознавать мутации, способствующие развитию рака, и бороться с ними. Она предлагает многообещающий подход к созданию точного и устойчивого иммунного ответа, и не так сложна или затратна, как полностью персонализированные вакцины».
Исследовательская группа уже завершила набор во вторую фазу более масштабного исследования новой вакцины ELI-002 7P, которая нацелена на более широкий набор мутаций KRAS, сообщается в пресс-релизе.
Ингибитор активной формы мутантного KRAS эффективен против рака легких у мышей
Источники
Wainberg, Z.A., et al. Lymph node-targeted, mKRAS-specific amphiphile vaccine in pancreatic and colorectal cancer: phase 1 AMPLIFY-201 trial final results // Nature Medicine (2025). DOI: 10.1038/s41591-025-03876-4
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0











