Вакцины против кори и ветряной оспы безопасны для детей, перенесших трансплантацию органов
Живые вирусные вакцины против кори, краснухи, паротита и ветряной оспы безопасны для детей, перенесших трансплантацию печени и почек. В исследовании принял участие 281 ребенок с низким, средним или высоким уровнем иммуносупрессии. У большинства пациентов после одной-трех доз вакцин был достигнут уровень защитных антител. С учетом участившихся вспышек кори и паротита авторы предлагают смягчить критерии отвода от прививок для детей — реципиентов органов.
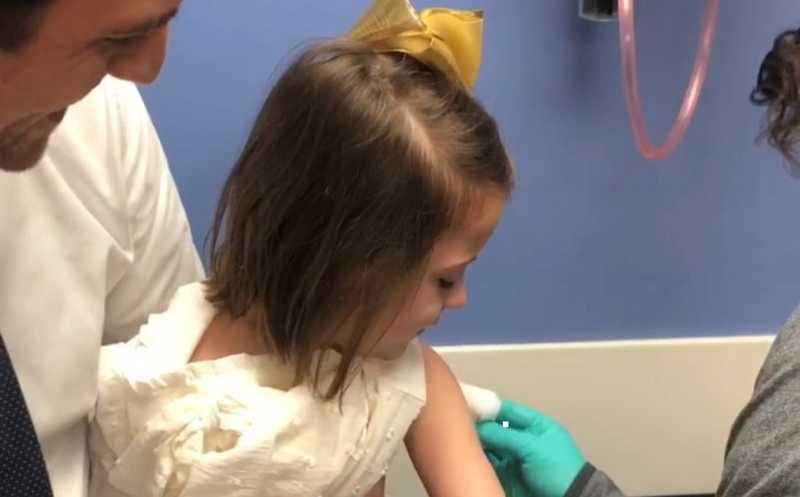
Девочка с трансплантированной печерью получает вакцину MMR в детской больнице Цинциннати.
Credit:
Cincinnati Children's, предоставлено родственниками | Пресс-релиз
Исследователи из США показали, что живые вакцины, которые вводятся детям согласно национальным календарям прививок, не вызывают серьезных побочных эффектов у детей, находящихся на иммуносупрессивной терапии после трансплантации органов.
В настоящее время введение живых вакцин MMR (корь, краснуха, паротит) и от одной до трех доз VZV (ветряная оспа) рекомендовано не ранее чем через год после трансплантации и только тем пациентам, кто получает низкие дозы иммуносупрессивных препаратов. В данном исследовании приняли участие пациенты, находящиеся на низком, среднем и высоком уровне иммуносупрессии, а некоторые из них были инфицированы вирусом Эпштейна–Барр. Отсутствие серьезных побочных эффектов говорит о том, что критерии отводов от вакцинации можно смягчить. Это особенно актуально с учетом вспышек кори и других инфекционных заболеваний в последние годы.
Во время пандемии SARS-CoV-19 миллионы пациентов не были вакцинированы согласно нацкалендарям, что привело к снижению коллективного иммунитета против ряда инфекций. На этом фоне вспышки кори, паротита и ветряной оспы создают значительный риск для пациентов, перенесших трансплантацию. Для предотвращения отторжения пересаженного органа применяют иммуносупрессивную терапию, которая подавляет активность иммунной системы. Препараты, их дозировка, а также длительность применения, которое может быть и пожизненным, определяются индивидуально. Как следствие, такие пациенты подвержены инфекциям.
Ведение живых вакцин не рекомендовано после пересадки органов, так как человек с ослабленным иммунитетом может заразиться вакцинным штаммом. Еще в начале 1990-х годов была показана эффективность живых вакцин у пациентов после трансплантации, и в 2019 году Американское общество трансплантологов опубликовало рекомендации применения живых вакцин против кори, краснухи, паротита (MMR) и ветряной оспы (VZV): эти вакцины могут получать пациенты на низких дозах иммуносупрессивных препаратов спустя год после операции. Однако исследования показали, что меньше трети центров детской трансплантологии регулярно предлагают живые вакцины.
В исследовании участвовал 281 ребенок, из которых 96% были реципиентами печени, 3% — реципиентами почек и 1% — печени и почек. Пациенты получили от одной до трех доз вакцин MMR (236 детей) и VZV (217 детей). Средний возраст на момент получения первой дозы вакцины после трансплантации составил 8,9 лет, а среднее время от трансплантации до включения в исследование — 6,3 года.
На момент вакцинации 94% детей, получивших вакцину против ветряной оспы, не имели к ней иммунитета, и 97% детей, которые получили вакцину MMR, не имели иммунитета к кори, эпидемическому паротиту и/или краснухе. В исследованной группе 73,4% детей находились на низком уровне иммуносупрессии, 14,2% и 12,4% получали средние и высокие дозы иммуносупрессивных препаратов, соответственно. Спустя 1–3 месяца после вакцинации у большинства пациентов был сформирован защитный уровень антител: у 72% от ветряной оспы, 86% от кори, 83% от эпидемического паротита, 99% от краснухи. Через год после вакцинации большинство детей, у которых выработались защитные антитела, сохранили эту защиту: у 77% от ветряной оспы, 92% от кори, 83% от эпидемического паротита и 94% от краснухи.
После вакцинации VZV у пятерых детей, получавших среднюю и высокую дозу иммуносупрессивных препаратов, развилась клиническая форма ветряной оспы, но все дети выздоровели в течение недели.
При средней иммуносупрессии антитела на защитном уровне сформировались у 77% детей, тогда как при низкой иммуносупресси защитный уровень сформировался у 92% детей. Не было зафиксировано серьезных нежелательных явлений, приведших к отторжению трансплантата.
У 7% детей была обнаружена ДНК вируса Эпштейна–Барр на момент вакцинации. По существующим рекомендациям, такие пациенты должны находиться под особым контролем. Однако не было установлено, что этот тем или иным образом факт влияет на формирование защитного иммунитета.
Среди ограничений исследования авторы отмечают неполноту историй пациентов о вакцинации до трансплантации. Кроме того, в нем участвовало мало реципиентов почки. Также не у всех детей были определены защитные титры антител через год после вакцинации.
«В современном мире заражение корью и ветряной оспой представляет собой реальный риск для детей с ослабленным иммунитетом. Эти инфекции могут быть смертельными для реципиентов трансплантата. Возможность вводить живые вакцины после трансплантации и обеспечивать иммунитет имеет решающее значение», — прокомментировала первый автор исследования доктор Эми Фельдман, директор программы трансплантации печени в детской больнице Колорадо.
Источники
Feldman A.G., et al. Safety and Immunogenicity of Live Viral Vaccines in a Multicenter Cohort of Pediatric Transplant Recipients // JAMA Network Open. 2023; 6(10): e2337602. DOI: 10.1001/jamanetworkopen.2023.37602
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0









