Вес могут снижать не только агонисты, но и антагонисты рецепторов GIP
Второе поколение препаратов для снижения веса — биспецифические агонисты рецепторов инкретинов GLP-1 и GIP (GLP-1R и GIPR) — эффективнее агонистов только рецептора GLP-1, к которым относится, например, семаглутид. Однако были получены парадоксальные результаты: в сочетании с агонистами GLP-1R потерю веса ускоряют не только агонисты GIPR, но и его антагонисты. В журнале Nature Metabolism опубликованы две статьи, авторы которых рассматривают, как действуют на мозг мышей агонисты GLP-1R, агонисты и антагонисты GIPR. По их данным, нейронные сигнальные пути антагонистов GIPR — общие с агонистами GLP-1R, но отличные от агонистов GIPR.
Семаглутид и другие стабилизированные аналоги глюкагоноподобного пептида-1 (GLP-1, ГПП-1) произвели революцию в лечении ожирения и диабета. Эти препараты являются агонистами рецептора GLP-1R, то есть оказывают такое же действие, как сам GLP-1: усиливает секрецию инсулина поджелудочной железой, снижает аппетит.
Следующим поколением препаратов для лечения ожирения стали многофункциональные лекарства, у которых есть и другие цели, помимо GLP-1R. Одна из таких целей — рецептор GIPR глюкозозависимого инсулинотропного полипептида (GIP); этот гормон, как и GLP-1, принадлежит к инкретинам — стимуляторам продукции инсулина, снижающим уровень глюкозы. К подобным препаратам двойного действия относится Зепбаунд (тирзепатид) от Eli Lilly — агонист обоих рецепторов. В прошлом году было показано его превосходство над семаглутидом при лечение ожирения в реальных условиях. Хорошие результаты в клинических исследованиях демонстрирует и другая разработка Eli Lilly — ретатрутид (LY3437943). Датская компания Novo Nordisk, в которой был разработан семаглутид, недавно приобрела права на экспериментальный препарат UBT251 китайской компании United Laboratories, который действует на три рецептора — GLP-1R, GIPR и рецептор гормона глюкагона.
Парадокс в том, что в сочетании с агонистами GLP-1R усиливают потерю веса и агонисты GIPR, и его антагонисты. В очередном номере журнала Nature Metabolism эффектам комбинации агонистов GLP-1R и антагонистов GIPR посвящены две статьи. В первой работе участвуют исследователи из Eli Lilly, во второй — из компании Amgen, которая разрабатывает свой биспецифический агонист GLP-1R и GIPR. Оба исследования выполнены на мышах с нокаутами инкретиновых рецепторов во всем организме или в определенных типах клеток, причем авторы методами транскриптомного анализы идентифицировали изменения в экспрессии генов при воздействии препаратов.
Авторы первой работы показали, что инактивация гена Gipr только в ГАМКергических нейронах или в нейронах периферической нервной системы не влияет на потерю веса, вызванную агонистом GLP-1R в сочетании с антагонистом GIPR. При этом ранее было показано, что действие двойных агонистов GIPR–GLP-1R зависит именно от функциональной сигнализации GIPR в ГАМКергических нейронах. Очевидно, в случае антагониста GIPR задействован другой путь.
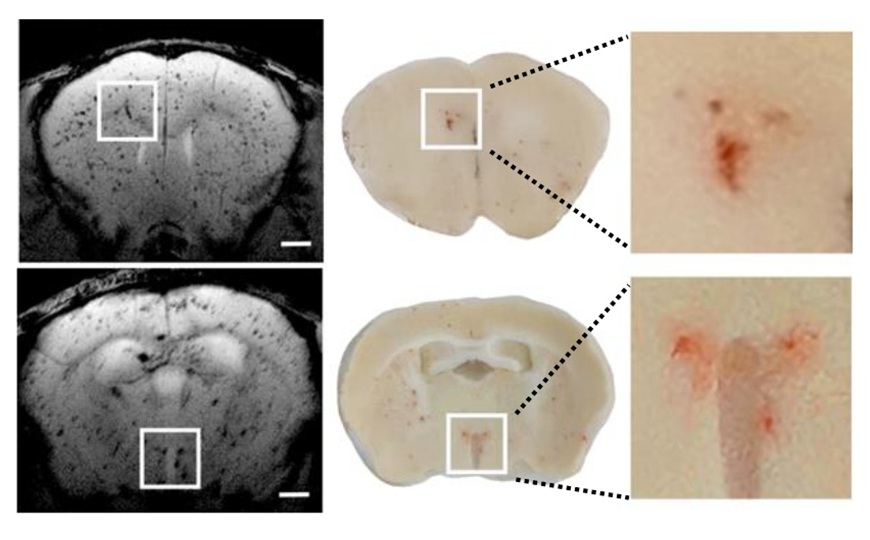
Чтобы определить, на какие нейронные пути действуют антагонисты и агонисты GIPR, авторы провели секвенирование РНК единичных ядер из мозговой ткани мышей с ожирением, которые получали ацил-GIP, ацил-GLP-1, ацилированный пептидный антагонист GIPR либо пептид MAR709 — двойной агонист GIPR–GLP1R. (Ацилирование улучшает фармакокинетику пептидов.) Оказалось, что в стволе мозга профиль экспрессии, связанный с антагонистом GIPR, положительно коррелирует с профилем GLP-1R, но отрицательно коррелирует с агонистом GIPR и двойным агонистом GIPR–GLP1R. Напротив, изменения экспрессии генов, вызванные агонистом GIPR, отрицательно коррелируют с назначением агониста GLP-1R и положительно — с двойным агонистом GIPR–GLP1R.
Дальнейший анализ показал, что три популяции нейронов, демонстрирующие наиболее сильные изменения экспрессии генов в ответ на антагонист GIPR, активно экспрессируют ген Glp1r и аналогичным образом регулируются агонистами GLP-1R. Иными словами, антагонизм GIPR задействует те же нейроны и сигнальные пути, что и агонизм GLP-1R, а нейронные пути агонизма GIPR от них отличаются.
Авторы также обнаружили, что подавление экспрессии Glp1r во всех клетках мыши (а не только в определенных популяциях нейронов) блокировало потерю веса, опосредованную антагонистом GIPR. При этом действие агонистов GIPR от экспрессии Glp1r не зависит.
Согласно данным, которые получили авторы второй статьи, для действия двойного агониста GLP-1R—GIPR необходима экспрессия в нейронах как Gipr, так и Glp1r. Это подтверждает, что подобные препараты взаимодействуют непосредственно с нейронами. И действительно, биспецифическая молекула — конъюгат пептида, активирующего GLP-1R, и антитела, блокирующего GIPR, — обнаруживалась в мозге мышей после введения в периферическую кровь, хотя размер ее достаточно велик (около 150 кДа).
Эти же исследователи показали, что генетическая блокада сигнализации GIPR в нейронах (копирование эффекта антагониста) усиливает действие агонистов GLP-1R на снижение массы тела. Они также описали метаболические преимущества блокады GIPR — воздействие антагониста сопровождалось появлением транскриптомных сигнатур ремоделирования тканей, улучшенного липидного метаболизма и уменьшения воспаления в жировой ткани и печени.
Таким образом, ЦНС — важная мишень как для агонистов, так и для антагонистов GIPR, но те и другие действуют на различные нейронные сигнальные пути, опосредующие потерю веса. Сигнальные пути ЦНС антагонистов GIPR — общие с агонистами GLP-1R, но отличные от агонистов GIPR.
Остается еще много вопросов. Например, как изменяется активность этих сигнальных путей при длительном лечении? (Авторы вводили мышам препараты кратковременно, чтобы исключить влияние потери веса на транскриптом.) Как именно антагонисты GIPR активируют сигнализацию GLP-1R в мозге? Картирование нейронных сетей GIPR и GLP-1R и их пересечений поможет понять, как влияет на потерю веса взаимодействие препаратов, отмечается в комментарии Nature Metabolism. Эти исследования крайне важны, учитывая стремительный темп гонки разработчиков новейших препаратов от ожирения.
Тирзепатид лучше семаглутида способствует снижению веса в клинике
Источники
Gutgesell, R.M., et al. GIPR agonism and antagonism decrease body weight and food intake via different mechanisms in male mice // Nature Metabolism (2025). DOI: 10.1038/s42255-025-01294-x
Liu, C.M., et al. GIPR-Ab/GLP-1 peptide–antibody conjugate requires brain GIPR and GLP-1R for additive weight loss in obese mice // Nature Metabolism (2025). DOI: 10.1038/s42255-025-01295-w


 Меню
Меню





 Все темы
Все темы



 0
0