Вирус гриппа инфицирует клетки сердца
Ученые из Университета штата Огайо обнаружили, что вирус гриппа А реплицируется в кардиомиоцитах. Ранее считалось, что нарушения сердечной функции при тяжелом гриппе обусловлено воспалением в легких. Исследование провели на мышиных моделях с использованием рекомбинантного вируса H1N1.
Вирус гриппа поражает легкие, но также может вызывать осложнения на сердце. Долгое время считалось, что системное кардиотоксическое воспаление обусловлено цитокиновым штормом, который вызывает инфекция, поражающая легкие.
Исследователи из Университета штата Огайо обнаружили, что нарушение работы сердца вызваны репликацией вируса гриппа А (H1N1) непосредственно в сердечно-мышечной ткани. Исследование провели на мышах.
Один из ведущих авторов статьи, Джейкоб Юнт, изучает грипп много лет. В частности, в его лаборатории разработали мышиную модель с нокаутом гена IFITM3, кодирующего одноименный белок врожденного иммунитета IFITM3. Он представляет собой трансмембранный белок, который в норме блокирует связывание вируса с мембраной.
Вариации в гене IFITM3 — единственный известный генетический фактор, предсказывающим увеличение риска развития тяжелых форм гриппа. Около 20% китайцев и 4% европейцев имеют генетические варианты, которые приводят к дефициту нормального IFITM3. Мышиная модель, разработанная авторами статьи, отражает развитие патологий у таких людей.
Ранее ученые обнаружили, что у нокаутных по IFITM3 мышей повышается вероятность возникновения нарушений работы сердца по сравнению с мышами дикого типа. Авторы поставили перед собой задачу выяснить, что именно влияет на развитие патологий сердца — достаточно ли для нарушения сердечной функции воспаления, возникающего в легких, или необходима репликация вируса в кардиомиоцитах.
Авторы создали рекомбинантный вирус штамма H1N1. Репликация такого вируса в кардиомиоцитах значительно ослаблена, в то время как в легких она остается на прежнем уровне. Далее ученые заразили мышей, нокаутных по IFITM3, и мышей дикого типа интактным и рекомбинантным вирусом.
Оба вируса реплицировались в легких и приводили к системному воспалению, но рекомбинантный вирус не обнаружили в сердечно-мышечной ткани мышей дикого типа, и его титр был значительно снижен в кардиомиоцитах генно-модифицированных мышей. Так, ученые создали модель, которая позволяет разделять влияние воспаления в легких и вирусной репликации в сердце на нарушение сердечной функции.
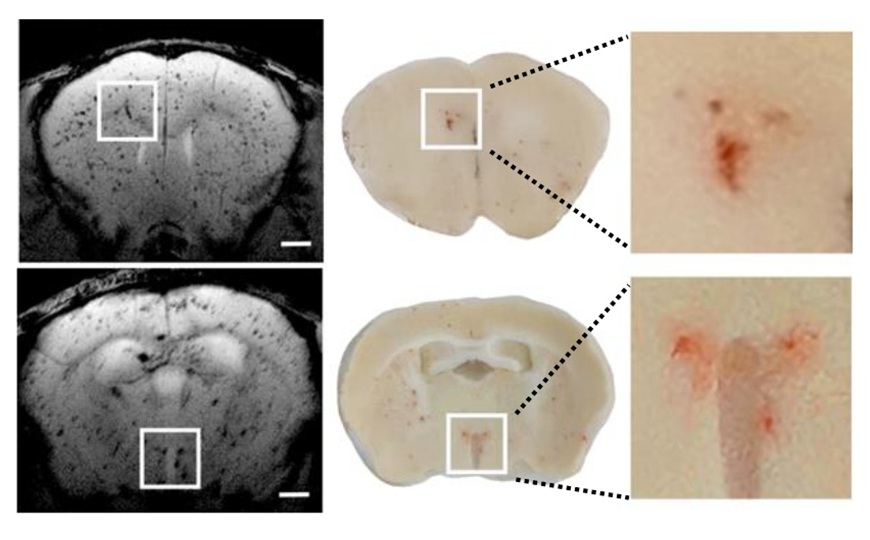
Авторы обнаружили, что у мышей, которым ввели рекомбинантный вирус, частота образования фиброзов и концентрация креатинкиназы (маркера сердечной недостаточности) была меньше по сравнению с мышами, зараженными интактным вирусом. У последних также была нарушена проводимость сердца, чего не обнаружили у мышей с генетически модифицированным вирусом.
«Теперь у нас есть мышиная модель и [модифицированный] вирус, которые позволили различить воспаление в легких и репликацию вируса в сердце. До сих пор у нас не получалось этого сделать», — говорит Юнт. «Если у вас нет вируса, который активно реплицируется в сердце, вы не увидите таких же нарушений проводимости сердца или фиброза».
Как отмечают сами авторы, предстоит еще большая работа. Пока не до конца ясно, следует ли как-то модифицировать терапию госпитализированных пациентов с гриппом и осложнениями на сердце, но проделанная работа определила вектор последующих экспериментов. В частности, ученые планируют исследовать, как вирус распространяется из первоначального очага инфекции в сердце и поддерживает свою жизнедеятельность в новых условиях.
Источник
Adam D. Kenney, et al. Influenza virus replication in cardiomyocytes drives heart dysfunction and fibrosis // Science Advances, 8, published online 2022, DOI: 10.1126/sciadv.abm5371
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы



 0
0