Внеклеточный матрикс помогает кластерам опухолевых клеток выживать в кровотоке
Для образования метастазов циркулирующие опухолевые клетки (ЦОК) должны выдержать механический стресс при перемещении в кровотоке. Лучше выживают кластеры ЦОК, для образования которых обычно нужны белки адгезивных контактов эпителия (такие как E-кадгерин). Но ЦОК трижды негативного рака молочной железы формирует кластеры за счет внеклеточного матрикса, в первую очередь гиалуронана. Он взаимодействует с рецептором CD44 соседней клетки при первоначальном контакте и помогает образовывать более прочные связи. Раковые клетки, вырабатывающие мало гиалуронана, образовывали меньше кластеров ЦОК и метастазов в организме мыши.
Циркулирующие опухолевые клетки (ЦОК) необходимы для метастазирования; они перемещаются по кровотоку в одиночку или в виде кластеров. Кластеры могут включать в себя как одни только опухолевые клетки, так и опухолевые клетки с лимфоцитами, тромбоцитами или ассоциированными с опухолью фибробластами. Кластеры ЦОК чаще дают начало метастазам, чем одиночные ЦОК. Ранее было показано, что для образования кластеров нужны белки адгезивных контактов эпителия (такие как E-кадгерин), но эти белки могут отсутствовать при агрессивном трижды негативном раке молочной железы (РМЖ), который активно метастазирует. Исследователи из США выяснили механизм соединения клеток в кластере ЦОК подобных опухолей.
В клетках трижды негативного РМЖ активнее экспрессируются компоненты внеклеточного матрикса и плазматической мембраны по сравнению с другими типами рака. Например, в них значительно выше уровень экспрессии HAS2, который кодирует гиалуронансинтазу 2. Авторы предположили, что внеклеточный матрикс повышает агрессивность трижды негативного РМЖ.
Гиалуронан (HA) — важный компонент внеклеточного матрикса, а HAS2 — основной продуцирующий HA фермент РМЖ. Ранее было показано, что повышение уровня HA и экспрессии HAS2 ассоциировано с худшей выживаемостью и метастазированием, но механизм не был выявлен.
На мышиной модели трижды негативного РМЖ авторы изучили локализацию HA в ЦОК. HA покрывал поверхность ЦОК и оставался на этих клетках, пока они перемещались по кровотоку. В кластерах HA локализовался в местах контакта отдельных ЦОК.
В опытах in vitro исследователи выяснили, не оторвутся ли отдельные ЦОК друг от друга при перемещении по артериям и венам. Оценивали число и размеры кластеров, а также число единичных ЦОК. ЦОК циркулируют от нескольких минут до нескольких часов; исследователи наблюдали за системой в течение часа, но кластеры, состоящие из клеток LM2, BT549, WHIM12 и MDA-MB-231, оставались стабильными. Напротив, клетки неметастатического РМЖ HMLE и MCF10A не образовывали кластеры.
Проанализированные клеточные линии, образующие метастазы, не вырабатывали E-кадгерин, но экспрессировали HAS2, и его уровень экспрессии положительно коррелировал с числом кластеров. Предположительно, HA опосредует образование кластеров.
Действительно, HA присутствовал на поверхности клеток, особенно много его было в местах контактов двух клеток. HA деградировали гиалуронидазой, в результате клетки утрачивали способность формировать стабильные кластеры. Схожие результаты были получены при нокдауне HAS2. Причем необходимы были именно HA с высоким молекулярным весом.
Рецептор HA — CD44 — был необходим для формирования кластера. Если экспрессировать в клетках 293FT одновременно HAS2 и CD44, то они тоже начинали формировать кластеры. Результаты подтвердили на клетках рака простаты, поджелудочной и глиобластомы.
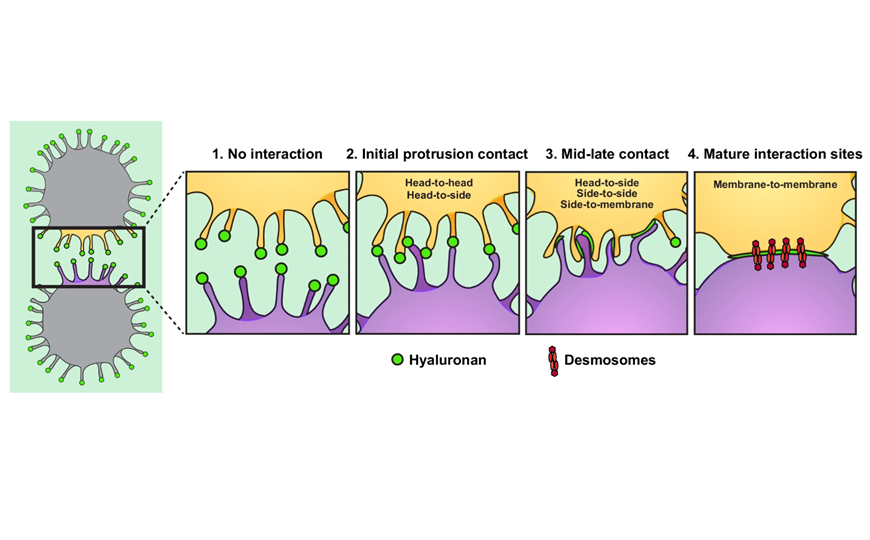
Раковые клетки также образовывали многочисленные CD44+ выпячивания. Они повышали площадь поверхности клеток и, вероятно, служили точкой первоначального контакта между соседними клетками. Для образования этих выпячиваний и кластеров в целом необходим актин. После формирования первоначального контакта клетки сближаются, пока не сформируют стабильную связь.
Контакты между клеток образуются и без HA, но такие агрегаты не выдерживают действия механического стресса, который неизбежен при перемещении по кровотоку. После образования плотных межклеточных контактов формируются также десмосомы, стабилизирующие кластеры. Снижение количества HA уменьшало выживаемость ЦОК под действием стресса (с 65% живых клеток до 20–25% через 24 часа).
Раковые клетки LM2 и клетки с нокдауном HAS2 вводили мышам системно, а через 24 часа изучали легкие. При нокдауне опухолей в легких было меньше. То же было показано при образовании метастазов в легкие на мышиной модели РМЖ. Если вводить мышам раковые клетки с нокдауном HAS2, то образуется в 75 раз меньше одиночных ЦОК и в 82 раза меньше кластеров. У некоторых мышей вовсе не обнаруживалось кластеров ЦОК. Но даже если только у некоторых ЦОК сохранялась способность вырабатывать HA, они могли рекрутировать ЦОК без HA в кластеры.
Таким образом, исследователи выявили механизм клеточной адгезии, обеспечивающий стабильные клеточные контакты по типу «клетка-внеклеточный матрикс-клетка». Этот механизм используется ЦОК при трижды негативном РМЖ, которые не имеют белков адгезивных контактов эпителия. Это позволяет им сочетать преимущества в миграции и инвазии с повышенным метастатическим потенциалом, обеспечиваемым кластерами ЦОК.
Гиалуронан во внеклеточном матриксе обеспечивает химиорезистентность раковых клеток
Источник:
Georg OM Bobkov, et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis // Nature Communications (2026), published 06 February 2026, DOI: 10.1038/s41467-026-69007-w


 Меню
Меню





 Все темы
Все темы




 0
0











