Восстановление активности cGAS в раковых клетках усиливает иммунный ответ на опухоль
Сигнальный путь cGAS-STING — один из естественных механизмов противоопухолевого иммунитета, однако его активация в раковых клетках зачастую подавлена. Ученые из США предложили восстановить работу этого сигнального пути с помощью липидных наночастиц, содержащих мРНК cGAS. Первые эксперименты на мышах с меланомой, которым вводили наночастицы в опухоли, дали обнадеживающий результат. Активация cGAS-STING усиливала противоопухолевый иммунный ответ и подавляла рост агрессивной формы меланомы, которая редко отвечает на иммунотерапию.
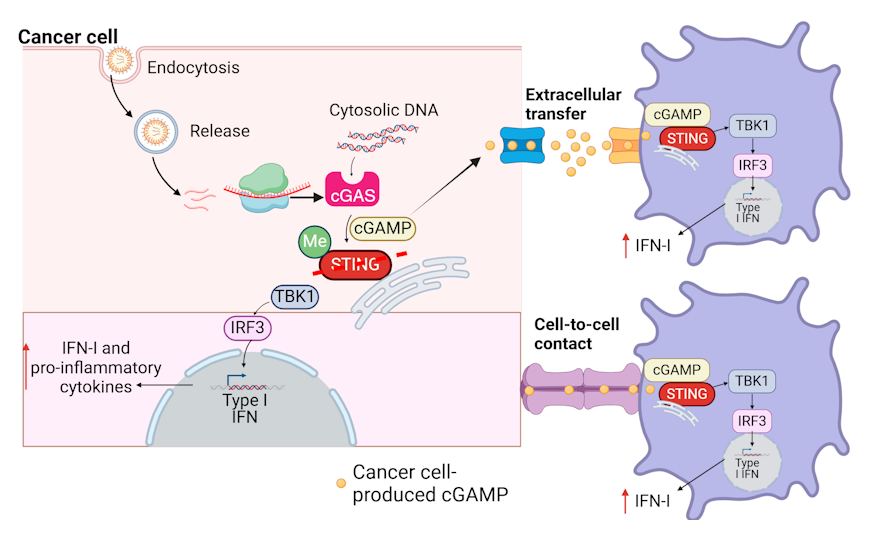
Credit:
PNAS (2025). DOI: 10.1073/pnas.2409556122 | CC BY-NC-ND
Одним из естественных механизмов, которыми обладает организм для борьбы с опухолевыми клетками, является сигнальный путь cGAS-STING. Это внутриклеточный «сенсор опасности», реагирующий на присутствие в клетке чужеродной двухцепочечной ДНК и запускающий выработку интерферонов I типа для борьбы с вирусами и подавления роста опухолей. В отличие от здоровых клеток, клетки опухолей могут содержать в своей цитоплазме свободную двухцепочечную ДНК, что делает активацию пути cGAS-STING перспективной стратегией противоопухолевой терапии. При этом в обычных условиях в опухолевых клетках эта система не активируется, что может быть связано, например, с эпигенетическим регулированием. Кроме того, циклический гуанозинмонофосфат-аденозинмонофосфат (2′3′-cGAMP) — гидрофильная и отрицательно заряженная молекула, что значительно осложняет его доставку в клетки, где он также может подвергаться деградации ферментом ENPP1.
Чтобы преодолеть эти ограничения, ученые из Массачусетского технологического института, Гарвардского университета и Гарвардской медицинской школы предложили искусственно усилить выработку 2′3′-cGAMP в опухолевых клетках. С помощью липидных наночастиц они доставили в них мРНК, кодирующую фермент cGAS — синтазу циклического GMP-AMP. Исследователи предположили, что синтезируемый таким образом cGAMP может не только действовать на сами раковые клетки, но и выделяться в межклеточное пространство, где будет захватываться иммунными клетками.
«Часть моей философии науки заключается в том, что мне очень нравится использовать эндогенные процессы, которые уже имеются в организме, и пытаться применять их в немного ином контексте. Эволюция уже проделала всю тяжелую работу. Нам нужно только понять, как подтолкнуть ее в другом направлении, — объясняет эту задумку Александр Крайер, первый автор статьи. — Когда я увидел, что раковые клетки производят эту молекулу, я подумал: может быть, есть способ использовать этот процесс и усилить его».
Эксперимент проводили на линии клеток мышиной меланомы. После доставки липидных наночастиц с мРНК опухолевые начинали активно синтезировать cGAMP и выделять его во внеклеточную среду. Этот процесс дополнительно усиливался после искусственного внесения в клетки двухцепочечной ДНК. Чтобы убедиться, что выделяемый cGAMP биологически активен, ученые использовали RAW-Lucia™-ISG-макрофаги, в которых при активации интерферонового сигналинга запускалась экспрессия люциферазы. Другими маркерами того, что выделяемая опухолевыми клетками сигнальная молекула активировала дендритные клетки и макрофаги, было повышение экспрессии CD80, CD86, CD40 и MHC-II. Эти эффекты наблюдались даже при отсутствии непосредственного контакта между клетками, что свидетельствует о передаче cGAMP через некие внеклеточные механизмы, например, везикулы.
Липидные наночастицы с мРНК также оказали противоопухолевый эффект в мышиной модели агрессивной меланомы. Введение наночастиц в опухоли значительно замедляло их рост и увеличивало общую выживаемость мышей. Наилучший результат был достигнут при сочетании такой терапии с антителами к PD-1, которые вводили спустя сутки после наночастиц: у 30% подопытных мышей опухоли полностью регрессировали и не рецидивировали в течение 60 дней. Особая значимость полученных результатов состоит в том, что использовавшаяся в эксперименте форма меланомы зачастую не отвечает на терапию ингибиторами иммунных контрольных точек.
Чтобы разобраться в механизмах противоопухолевой активности наночастиц, ученые проанализировали микроокружение опухолей. Они выявил повышение концентрации хемокина CXCL10 — молекулы, привлекающей Т-лимфоциты и NK-клетки в очаг воспаления. Через сутки после введения препарата в микроокружении опухоли увеличивалась доля активированных CD8+ Т-лимфоцитов, NK-клеток, макрофагов и дендритных клеток.
По мнению доктора Натали Арци, руководительницы исследования, использование внутриклеточных механизмов выработки сигнальных молекул — перспективное направление терапии рака, поскольку может не только повысить эффективность лечения, но и минимизировать системные токсические эффекты, характерные для современных методов.
В меланомах обнаружили «кратеры» — посадочные площадки для Т-клеток, разрушающих опухоль
мРНК-вакцины против коронавируса улучшают результаты иммунотерапии рака
Источник
Cryer, A.M., et al. Restoration of cGAS in cancer cells promotes antitumor immunity via transfer of cancer cell–generated cGAMP. // Proceedings of the National Academy of Sciences (2025). DOI: 10.1073/ pnas .2409556122
Цитаты по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0










