Антитело к биомаркеру рака яичника, конъюгированное с радиоактивным изотопом, подходит для диагностики или терапии
Гликопротеин муцин-16 высоко экспрессирован на клетках рака яичника. Научная группа из США показала, что huAR9.6 — антитело к муцину-16, — конъюгированное с радиоактивным изотопом циркония, обладает диагностическим потенциалом, а конъюгированное с радиоактивным изотопом лютеция — терапевтическим потенциалом. Терапевтический агент показал противораковый эффект и повышение общей выживаемости на мышиных моделях рака яичника.
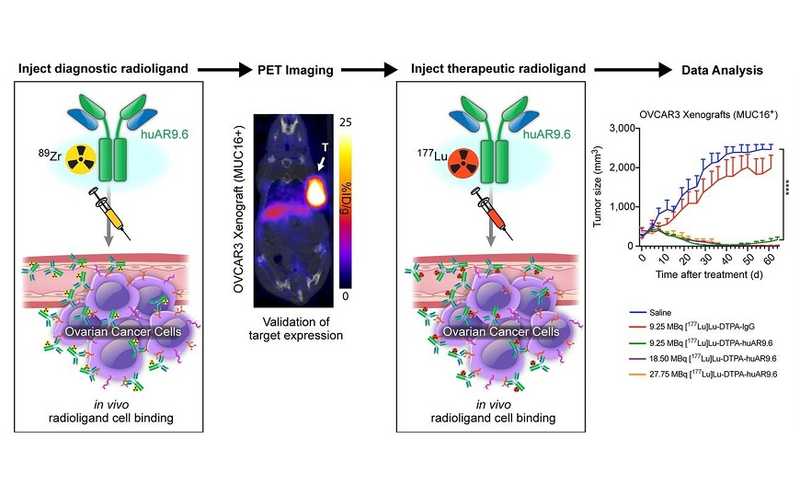
Антитело с тераностическим (диагностическим и терапевтическим) потенциалом при раке яичников: конъюгат с цирконием-89 обеспечивает визуализацию, а конъюгат с лютецием-177 подавляет рост опухоли у мышей.
Credit:
Journal of Nuclear Medicine. 2024. DOI: 10.2967/jnumed.123.266524 | Пресс-релиз
На данный момент стандартным подходом в терапии рака яичника остается химиотерапия препаратами платины. В качестве биомаркера для диагностики рака яичника часто используют опухолевый антиген 125 (CA125) — один из эпитопов муцина-16. Однако уровень CA125 в сыворотке крови не позволяет эффективно выявлять заболевание на ранней стадии. В новой статье, опубликованной в The Journal of Nuclear Medicine, авторы предложили диагностическую и терапевтическую системы, использующую гуманизированное антитело huAR9.6, нацеленное на гипогликозилированные остатки муцина-16 (MUC16). Антитело конъюгировали с радиоактивными изотопами циркония (препарат обозначили как [89Zr]Zr-DFO-huAR9.6) и лютеция ([177Lu]Lu-CHX-A″-DTPA-huAR9.6) для диагностики и терапии, соответственно.
Для in vivo экспериментов использовали мышей, которым ксенотрансплантировали опухоли рака яичника — с высокой экспрессией MUC16 (OVCAR3 и OVCAR4), с низкой экспрессией MUC16 (OVCAR5) и без экспрессии MUC16 (OVCAR8).
Диагностическое антитело [89Zr]Zr-DFO-huAR9.6 показало высокое и специфичное связывание с MUC16, а также стабильность в человеческой сыворотке. Оно хорошо связывалось с клетками линий OVCAR3 (76%) и OVCAR4 (75%), но не с OVCAR8. С помощью иммуно-ПЭТ визуализации было показано, что в экспериментах in vivo на мышиных моделях [89Zr]Zr-DFO-huAR9.6 накапливалось в опухолях OVCAR3 (35%) и OVCAR4 (30%) спустя 144 часа после инъекции; в гораздо меньшем количестве оно накапливалось в опухолях OVCAR5 (13%) и не накапливалось в OVCAR8 (1%).
Терапевтическое антитело [177Lu]Lu-CHX-A″-DTPA-huAR9.6 показало стабильность в человеческой сыворотке в течение более 7 дней. Для исследования терапевтического эффекта in vivo выбрали модель OVCAR3, причем использовали антитело с разной удельной активностью: 9,25 мегабеккерелей (МБк), 18,5 МБк и 27,75 МБк. В качестве мышам вводили физиологический раствор либо [177Lu]Lu-CHX-A″-DTPA-IgG. Все пять мышей в группе 18,5 МБк и две из пяти в группе 27,75 МБк показали полный ответ на терапию после однократного введения препарата. В группе 9,25 МБк девять из 15 мышей дали рецидив через 5–10 недель после терапии.
В исследованиях на моделях рака яичника с низкой экспрессией MUC16 (OVCAR5) или без экспрессии MUC16 (OVCAR8) использование терапевтического антитела в активности 9,25 МБк замедляло рост опухоли, но данный эффект был незначительным по сравнению с контролем. На моделях OVCAR8 не было обнаружено противоракового эффекта.
Побочным эффектом терапии была гематологическая токсичность. Снижение количества эритроцитов, тромбоцитов и лейкоцитов носило дозозависимый характер. Наиболее чувствительными к облучению оказались тромбоциты и лейкоциты, однако после начала терапии все показатели крови быстро возвращались к дотерапевтическому уровню.
«Эта тераностическая платформа может быть использована для стратификации и отбора пациентов, которым будет полезна целевая радиоиммунотерапия. Кроме того, она может сыграть важную роль в ранней диагностике рака яичника», — говорит Киара Мак, первый автор статьи.
Биспецифическое антитело уменьшило размеры резистентных опухолей в фазе 1 КИ
Источники
Kyeara N. Mack, et al. Interrogating the Theranostic Capacity of a MUC16-Targeted Antibody for Ovarian Cancer // Journal of Nuclear Medicine. 2024. DOI: 10.2967/jnumed.123.266524
Цитата по пресс-релизу

 Меню
Меню





 Все темы
Все темы




 0
0