Ближе к сердцу
Ученые из США разработали протокол получения эпикардиальных клеток-предшественников из индуцированных плюрипотентных стволовых клеток. При совместном культивировании эпикардиальных клеток-предшественников с кардиомиоцитами формируются агрегаты, способные к спонтанному сокращению.
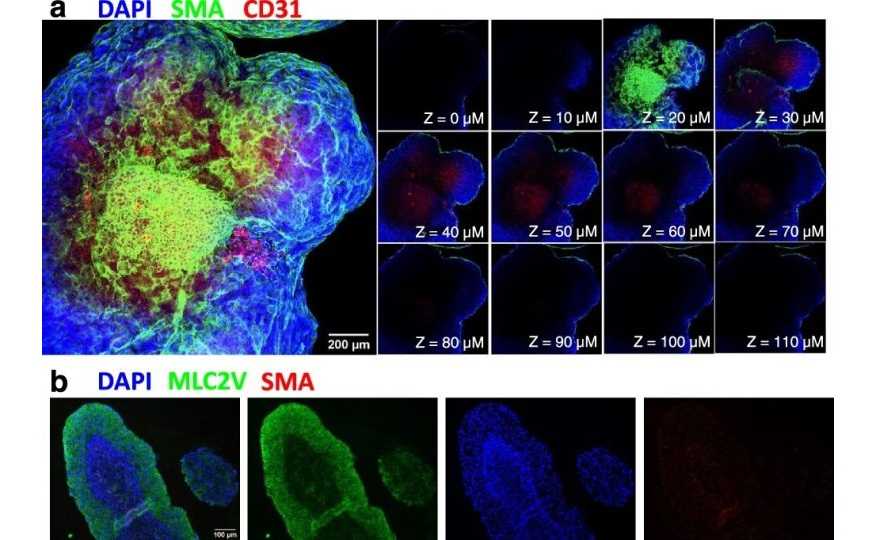
Credit: Tan, J.J., et al., 2021; DOI: 10.1038/s41467-021-24921-z | CC BY 4.0
Команда под руководством исследователей из Массачусетской больницы общего профиля получила культуру эпикардиальных клеток-предшественников (ЭКП), которые работают в период раннего развития сердца, но исчезают сразу после рождения. Они создали протокол, по которому можно запустить дифференцировку индуцированных плюрипотентных стволовых клеток человека (ИПСКч) в ЭКП, а также проверила их влияние на кардиомиоциты (КМЦ) при совместном выращивании в двумерных и трехмерных культурах.
ЭКП участвуют в формировании эпикарда — внешней оболочки сердца. В эпикарде присутствуют клетки разных типов, и все они необходимы для нормального развития сердца в пренатальный период. При контакте с КМЦ начинается дифференцировка ЭКП в непосредственно эпикардиальные клетки (ЭК), которые в ответ ускоряют развитие самих КМЦ. Ученые уже могут воспроизвести ранние стадии развития сердца и даже получить любое количество КМЦ всего лишь из одного образца крови, однко формирование структуры органа происходит на более позднем этапе. Повторение этого процесса в лабораторных условиях — сложная задача, так как множество разнообразных типов клеток участвуют в нем и создают уникальное микроокружение. Получение ЭКП приближает ученых к решению этой задачи.
Авторы новой работы создали протокол дифференцировки ИПСКч в ЭКП с помощью коктейля факторов эмбрионального развития BMP4, VEGF и RA. Всего через семь дней после его применения с помощью ОТ-ПЦР они детектировали повышение экспрессии маркеров, связанных с развитием сердца, и даунрегуляцию маркеров плюрипотентности. РНК-секвенирование подтвердило, что транскриптомный профиль полученных ЭКП близок к известному профилю ЭК.
Клетки на этом этапе имели эпителиальный фенотип, а иммуноцитохимия показала наличие ZO1 — белка, который участвует в образовании плотных контактов. При добавлении ростовых факторов TGFβ, bFGF или их сочетания происходил быстрый эпителиально-мезенхимальный переход с уменьшением экспрессии ZO1 и повышением маркера мезенхимальных клеток CD90.
Следующей частью эксперимента была проверка поведения ЭКП и КМЦ в условиях совместного культивирования. Иммуноцитохимический анализ показал, что непрямое сокультивирование ЭКП и КЦМ повышает миграцию ЭКП, а прямое вызывает формирование сети из агрегатов КЦМ, при этом к восьмому дню агрегаты становятся более плотными, а сама сеть к 21 дню ─ более выраженной. Кроме того, ЭКП благоприятно влияли на пролиферацию КМЦ.
Авторы исследования оценили и электромеханические свойства КМЦ, культивируемых отдельно, совместно с ЭКП, а также с линиями эндотелиальных клеток (HUVEC) и фибробластов (HCF). С помощью алгоритма высокоскоростной визуализации при электростимуляции было показано, что КМЦ, которые культивировались с ЭКП, сокращаются сильнее, чем в остальных трех случаях.
Последним этапом исследования стал анализ поведения ЭКП и КЦМ в трехмерных совместных культурах. Уже через день сфероиды ЭКП и КЦМ начинали соединяться между собой, при этом происходили спонтанные сокращения агрегатов, связанные с транспортом ионов кальция (эти сокращения зафиксированы на видео). Окрашивание гематоксилин-эозином показало, что образованные ЭКП и КЦМ совместные структуры высоко организованы, что особенно выражено в более плотных слоях клеток.
Описанное исследование ─ только часть большой работы группы, основной целью которой на данный момент является создание полностью функциональной и морфологически точной ткани сердца. Получение ЭПК — небходимый шаг на пути к воспроизведению полной трехмерной структуры органа.
Источник
Tan, J.J., et al. Human iPS-derived pre-epicardial cells direct cardiomyocyte aggregation expansion and organization in vitro. // Nature Communications 12, 4997 (2021), published online 17 August 21; DOI: 10.1038/s41467-021-24921-z


 Меню
Меню





 Все темы
Все темы




 0
0











