ДНК-наноприманка для мультиплексной идентификации вирусов
Быстрый и дешевый мультиплексный анализ, то есть одновременная идентификация разных биомолекул в образце (например, геномов различных вирусов), значительно облегчит диагностику респираторных заболеваний. Новая технология для мультиплексного анализа использует специальные конструкции на основе ДНК и нанопоровое зондирование.
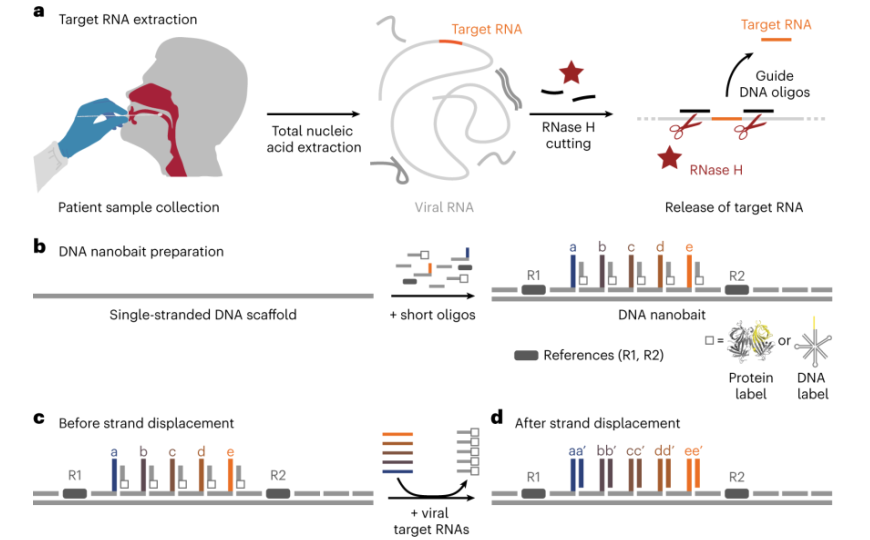
Nature Nanotechnology, 2023. DOI: 10.1038/s41565-022-01287-x | CC BY 4.0
В статистике смертей от инфекционных заболеваний во всем мире лидируют респираторные инфекции. Респираторные заболевания трудно диагностировать по симптомам, при этом подходы к терапии могут сильно различаться, поэтому необходимо развивать молекулярные методы диагностики. Во время пандемии впечатляющие результаты продемонстрировали ОТ-ПЦР и других методов амплификации. Однако проблемой остается мультиплексность, то есть возможность одновременно определять различных возбудителей в одном образце. Ученые из Великобритании создали самособирающуюся ДНК-наноприманку (DNA nanobait), способную одновременно идентифицировать несколько коротких РНК-мишеней. Для детекции используется нанопоровое зондирование.
Сначала в образец добавляют РНКазу Н и направляющие олигонуклеотиды (однонитевые молекулы ДНК длиной 20 нуклеотидов). Если в образце присутствует вирусный геном, олигонуклеотиды связываются с ним справа и слева от уникального участка-мишени. После этого РНКаза Н расщепляет гибридные участки ДНК:РНК и вырезает мишень. При выборе целевого сайта важно учитывать вторичную структуру вирусного генома, подчеркивают авторы; желательно, чтобы он находился в области с минимальным количеством спаренных оснований, иначе он останется связанным после вырезания.
ДНК-наноприманка имеет сложную структуру: от каркасной молекулы отходят «ветки», комплементарные мишеням. С «ветками» гибризизуются олигонуклеотиды, несущие метку (стрептавидин или «цветок» из шпилек ДНК); они оставляют свободным короткий однонитевой участок. Если в образце присутствует мишень, она вытесняет из дуплекса олигонуклеотид (toehold-mediated strand displacement), и с соответствующего сайта наноприманки исчезает метка.
Положение меток определяют с помощью нанопорового зондирования: отрицательно заряженная наноприманка в электрическом поле движется к положительному электроду и проходит через пору. Ток через пору резко уменьшается, когда через нее протискивается объемная метка, но если метка отсутствует — падения нет. (Принцип метода на рисунке.)
Авторы разработали наноприманку для мультиплексной идентификации SARS-CoV-2, респираторно-синцитиального вируса (универсальная для группы А), риновируса (универсальная), гриппа (универсальная для группы А) и парагриппа 1 и убедились, что эта платформа может одновременно идентифицировать несколько вирусов.
Наноприманку также можно настроить на распознавание вариантов вируса, различающихся единичными нуклеотидами. Авторы проверили это на штаммах SARS-CoV-2 (уханьский штамм, европейский штамм В.1, альфа, бета и дельта). Идентификация целей может происходить на фоне транскриптомов человека, без предварительной очистки и амплификации; тест успешно детектировал РНК SARS-CoV-2 в мазках из ротоглотки. Результаты исследования 13 образцов соответствовали результатам ПЦР-анализа
Предложенную технологию легко масштабировать и адаптировать к новым штаммам. Авторы считают, что она может стать альтернативой методам, основанным на амплификации.
Диагностическая система на основе CRISPR типа III выявляет РНК коронавируса
Источник
Bošković, F., et al. Simultaneous identification of viruses and viral variants with programmable DNA nanobait // Nature Nanotechnology (2023). DOI: 10.1038/s41565-022-01287-x


 Меню
Меню





 Все темы
Все темы




 0
0










