Инъекции гидрогеля с цитокинами вызвали у мышей формирование третичных лимфоидных структур
В опухолях могут образовываться третичные лимфоидные структуры (ТЛС) — агрегаты иммунных клеток, способствующие активации противоопухолевого ответа. Их наличие ассоциировано с лучшим прогнозом и лучшими результатами иммунотерапии. Авторы статьи в PNAS создали модель ТЛС для доклинических исследований. Мышам вводят подкожно хитозановый гидрогель, нагруженный липидными микрочастицами с хемокинами, и вокруг него образуется ТЛС-подобная структура, обогащенная лимфоцитами. У мышей после инъекций замедлился рост меланом, что подтверждает функциональную адекватность модели.
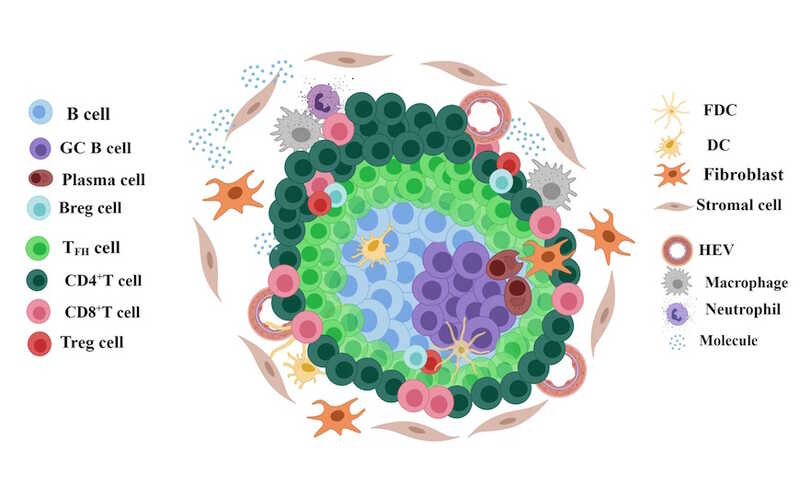
Вторичные лимфоидные органы (к ним относятся селезенка, лимфоузлы, миндалина) играют решающую роль в запуске адаптивного иммунного ответа на антигены. Так, именно в них наивные лимфоциты взаимодействуют с антигенпрезентирующими клетками. Существуют также третичные лимфоидные структуры (ТЛС, tertiary lymphoid structures) — агрегаты иммунных клеток, которые формируются в нелимфоидных тканях в процессе хронического воспаления, при аутоиммунных заболеваниях, хронические инфекциях и при некоторых видах рака. Ранее было доказано, что они ассоциированы с иммунным противоопухолевым ответом и их присутствие в опухолях повышает эффективность иммунотерапии.
ТЛС образуются не во всех опухолях, и опухоли, в которых их нет, без часто не поддаются иммунотерапии. Изучение свойств ТЛС и механизмов их формирования могло бы открыть новые терапевтические перспективы в иммуноонкологии. Однако для этого нужны адекватные модели, позволяющие проводить исследования на лабораторных животных. Двое исследователей из Онкоцентра и Исследовательского института Моффитта (США) предложили в качестве такой модели биоразлагаемый инъекционный гидрогель, содержащий лимфоидные хемокины и другие цитокины. Когда такой гидрогель ввести мышам подкожно, это обеспечивает высвобождение цитокинов в микроокружение ткани, что привлекает Т- и В-клетки и приводит к формированию ТЛС-подобных структур.
Для проверки гипотезы авторы выбрали гидрогель на основе хитозана. Важное свойство хитозановых гелей — термочувствительность: они переходят в гелевую фазу только при 37° С, что позволяет легко делать инъекции. Эксперименты с клетками, инкапсулированными в гель, подтвердили, что он не только биосовместим и не цитотоксичен (в отличие от некоторых других гелей на основе хитозана), но и повышает жизнеспособность и пролиферацию иммунных клеток.
Далее исследователи сконструировали специальные носители для цитокинов и хемокинов, обеспечивающие медленное и продолжительное высвобождение, — сферические микрочастицы силикагеля (SiO2) с мезопористой структурой. Их нагружали молекулами CCL19, CCL21 и CXCL13, а также лимфотоксином-α1β2, а затем покрывали липидной оболочкой.
Микрочастицы поместили в хитозановый гидрогель и протестировали данную конструкцию на мышах. Инъекция под кожу спины хорошо. переносилась. Через три недели вокруг остатков гидрогеля сформировались структуры, обогащенные иммунными клетками CD45+. В них также увеличилось число B-клеток (CD19+) и T-клеток (CD3+).
Чтобы проверить противоопухолевую активность данной модели ТЛС, исследователи вводили мышам через 27 дней после имплантации гидрогеля с цитокинами клетки меланомы. Рост опухоли у таких мышей был подавлен и выживаемость увеличилась по сравнению с контролем. Следовательно, индуцированные ТЛС- подобные структуры способны стимулировать специфический противоопухолевый Т-клеточный ответ.
«Изучая, как запускать формирование TLS, мы надеемся помочь иммунной системе лучше распознавать и атаковать такие опухоли, улучшая возможности терапии для пациентов, у которых в настоящее время наблюдается ограниченный ответ на иммунотерапию», — комментирует автор исследования Рана Фалахат.
Таким образом, созданы биополимерные скаффолды для инъекций, которые индуцируют образование ТЛС-подобных агрегатов in situ. Инъекционный способ введения, не требующий хирургического вмешательства, — важное преимущество данной модели. Авторы отмечают, что она может рассматриваться в качестве прототипа для новых терапевтических стратегий, направленных на преодоление резистентности к иммунотерапии за счет формирования ТЛС в опухолях. Однако она должна быть исследована на других видах опухолей.
В меланомах обнаружили «кратеры» — посадочные площадки для Т-клеток, разрушающих опухоль
Источники
Rana Falahat, James J. Mulé. Chemokine/cytokine-releasing biomaterials induce in situ tertiary lymphoid–like structures and enhance antitumor immunity // Proceedings of the National Academy of Sciences (2025), published online 3 November 2025. DOI: 10.1073/pnas.2409560122
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы
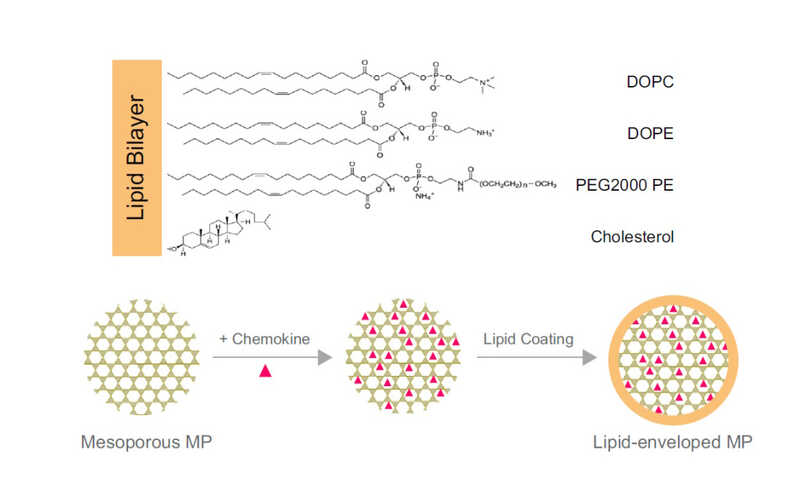 PNAS (2025), 2025. DOI:
PNAS (2025), 2025. DOI:




 0
0