NK клетки воруют PD-1 у раковых клеток и инактивируются
Естественные киллеры (NK) способны получать рецептор PD-1, который они в норме не экспрессируют, за счет трогоцитоза — захвата фрагмента клеточной мембраны раковой клетки. Процесс регулируется SLAM-рецепторами и приводит к инактивации NK.
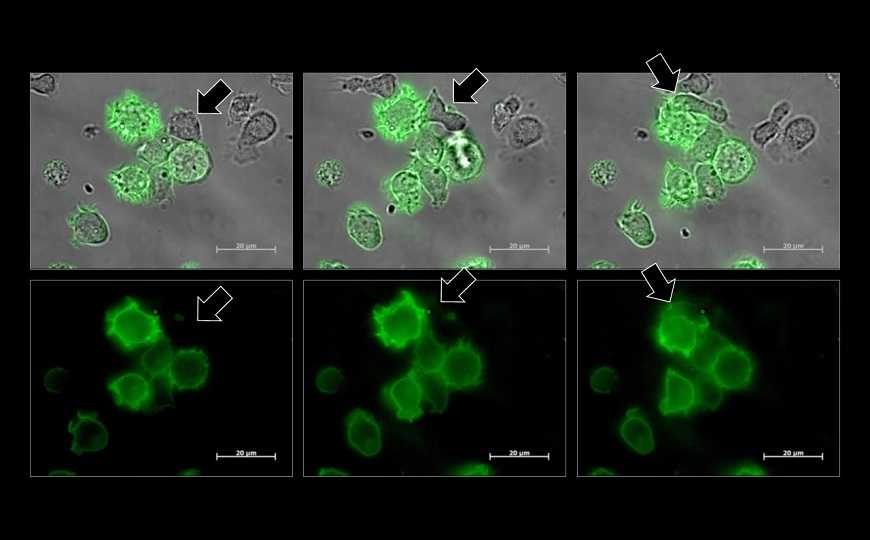
Зеленым обозначены раковые клетки, стрелка указывает на NK клетку.
Credit:
Hasim et al., Sci. Adv. 8, eabj3286 (2022) | Пресс-релиз
Ранее было показано, что рецептор PD-1 подавляет активность естественных киллеров (NK), так что эти клетки вносят вклад в эффективность терапии ингибиторами контрольных точек иммунитета у мышиной модели. Однако авторов смутило то, что в норме NK не экспрессируют PD-1. В новой работе эта же группа ученых показала, что NK получают рецептор PD-1 за счет трогоцитоза, «воруя» его у раковых клеток.
Трогоцитоз — процесс, при котором клетка захватывает фрагмент клеточной мембраны другой клетки и включает его в состав собственной. Так мембранные белки, которые несла клетка-жертва, оказываются на мембране клетки-охотника.
Первым делом авторы подтвердили, что NK получают PD-1 именно от раковых клеток. Для этого ученые использовали линию клеток лимфомы мышей RMA. Они получили рекомбинантную линию клеток RMA, экспрессирующих PD-1 и маркерный белок Thy-1.1, а также линию с нокаутом PD-1 (Pdcd-/-). При окрашивании клетки, несущие оба белка, становились синими, а клетки, несущие только Thy-1.1, — фиолетовыми. Далее ученые культивировали RMA клетки вместе с NK. Сами по себе NK не окрашивались ни по одному из белков. Но NK, культивируемые с Pdcd+/+ RMA клетками, окрашивались и по PD-1, и по Thy-1.1, а культивируемые с Pdcd-/- — только по Thy-1.1.
Ученые также подтвердили необходимость межклеточного контакта для передачи белков. Те NK, которые при культивировании были отделены от RMA клеток барьером, а также те, которые культивировали в супернатанте, в котором до этого находились RMA клетки, не окрашивались ни по одному из белков.
Так как специфичного способа ингибирования процесса трогоцитоза не существует, ученые нарушали синтез АТФ и полимеризацию актина. В обоих случаях NK не окрашивались ни по одному из белков, даже при совместном культивировании с RMA клетками. Ученые также подтвердили факт трогоцитоза несколькими дополнительными опытами с окрашиванием мембранных липидов и белков.
Далее авторы определили, какими рецепторами регулируется процесс трогоцитоза. Первым предположением ученых было взаимодействие PD-1 на раковых клетках и PD-L1 на NK. Однако насыщение культуры антителами, блокирующими PD-L1, не повлекло за собой остановку трогоцитоза, ровно как и нокаут PD-L1. Тогда ученые обратили внимание на SLAM-рецепторы — группу белков, экспрессируемых иммунными клетками и участвующих в межклеточных взаимодействиях, таких как презентация антигенов. SLAM-рецепторы в норме экспрессируются как NK, так и T- и B-лимфоцитами. Для проверки роли SLAM-рецепторов в трогоцитозе ученые провели нокаут локуса SLAM у иммунных клеток, которые затем культивировали с RMA клетками. В этом опыте ученые наблюдали нарушение трогоцитоза как у NK, так и у T- и B-лимфоцитов.
Также ученые решили проверить, проходит ли трогоцитоз in vivo. Для этого Pdcd+/+ и Pdcd-/- мышам вводили RMA или RMA-Pdcd-/- клетки. Когда размер опухоли достигал 300 мм3, ученые отбирали NK из тканей рака и окрашивали их. Во всех случаях NK из раковых тканей окрашивались по Thy-1.1. По PD-1 окрашивались только NK, полученные от животных, которым были введены Pdcd+/+ RMA клетки, вне зависимости от того, экспрессирует ли PD-1 само животное.
Авторы продемонстрировали, что захват PD-1 ингибирует активность NK in vivo — введение Pdcd-/- RMA-S-Pdl клеток из предыдущей работы Pdcd-/- мышам значительно замедляло рост опухоли. При этом in vitro рост Pdcd-/- RMA-S-Pdl клеток замедлен не был.
Наконец, ученые подтвердили факт трогоцитоза у человека на ряде клинических случаев, используя в качестве маркера белок CD138, экспрессируемый раковыми клетками, но не NK.
Источник
Mohamed S. Hasim, et al. When killers become thieves: Trogocytosed PD-1 inhibits NK cells in cancer // Science Advances Vol 8, Issue 15, published April 13, 2022. DOI: 10.1126/sciadv.abj3286


 Меню
Меню





 Все темы
Все темы




 0
0











