Оптогенетический подход вернул к норме уровень гормона паращитовидных желез
Избыточный синтез паратгормона приводит к нарушению метаболизма кальция и повреждению костных тканей. Ученые из Китая предложили использовать для лечения гиперпаратиреоза оптогенетику. Синтез гормона в клетках паращитовидной железы со светочувствительным белком в мембране регулируется синим светом, который может включаться избытком кальция. Модель проверили на мышах и крысах.
SIAT | Пресс-релиз
Гиперпаратиреоз — заболевание, при котором в крови больного повышен уровень паратиреоидного гормона, который производят паращитовидные железы. Оно приводит к нарушению гомеостаза кальция, фосфора и деминерализации костей. Секреция паратгормона контролируется концентрацией кальция в крови посредством отрицательной обратной связи, однако этот процесс подробно не изучен. Тем не менее известно, что ответ клеток сопровождается изменением мембранного потенциала и повышением концентрации внутриклеточного кальция.
Исследователи из Шэньчжэньского института передовых технологий показали, что клетки паращитовидных желез у больных гиперпаратиреозом не реагируют на повышенную концентрацию кальция. Они предложили исправить это, встроив в мембрану клеток специально сконструированный опсин ChETA — один из вариантов ченнелродопсина, — которой стимулирует деполяризацию мембраны в ответ на возбуждение светом синего спектра.
Сначала исследователи проверили свою гипотезу на культуре клеток паращитовидной железы человека. Они показали, что при освещении трансдуцированных клеток их мембрана деполяризовалась, а синтез паратгормона снижался. Последнее, как определили исследователи, было вызвано повышением внутриклеточной концентрации кальция и активации сигнальных путей PLA2-AA и PKA/цАМФ. Это приводило к ингибированию экспрессии генов GCM2, MAFB2 и PTH, которые тесно связаны с синтезом паратгормона. Более того, в освещаемых клетках нарушался везикулярный транспорт. Все наблюдаемые эффекты исчезали спустя час после светового стимула.
После этого ученые проверили работу генетической конструкции на ex vivo паращитовидной железе крыс. Они показали, что уровень гормона при освещении заметно снижался по сравнению с контролем, но возвращался к исходным значениям спустя 1-2 часа после выключения света. Также исследователи выяснили, что при увеличении времени освещения физиологический ответ клеток возрастает, однако уже после 30 минут воздействия он перестает меняться. В то же время частота мерцания возбуждающего света не влияет на физиологический ответ клетки. Свои результаты ученые подтвердили на модельных крысах с гиперпаратиреозом. Более того, они показали, что клетки без ChETA также могут менять свою физиологию под воздействием трансдуцированных соседей.
Затем исследователи решили сделать оптогенетическую систему автономной и приблизить ее к нативной регуляции в организме. Для этого они сконструировали синий светодиод, совмещенный с датчиком кальция. При повышенной концентрации Ca2+ светодиод включался и освещал клетки с ChETA на мембране. Свою идею они последовательно проверили на культуре клеток и на трансплантированной ткани щитовидной железы в иммуносупрессивных мышах. Повышение концентрации кальция во всех случаях приводило к снижению уровня паратгормона.
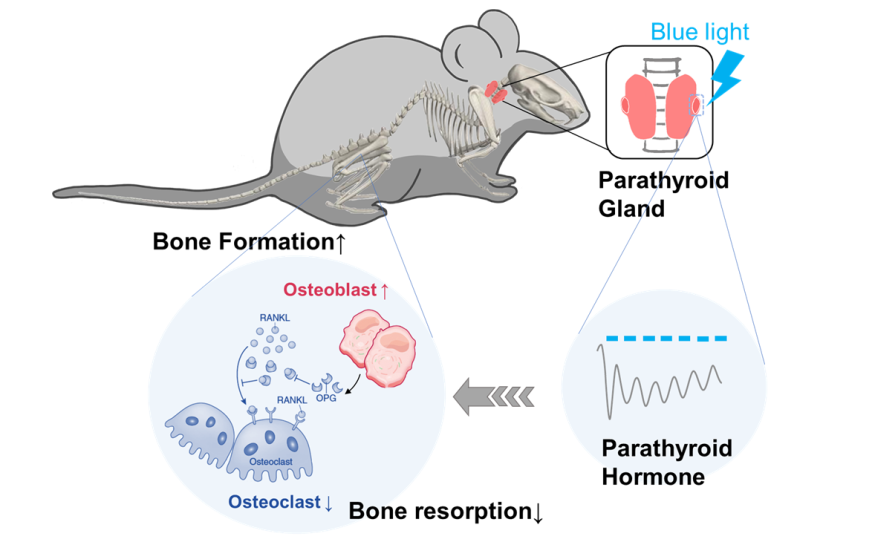
Также ученые выяснили, что их конструкция помогает устранить последствия гипертиреоза. Мышам трансплантировали в спину фрагменты человеческой паращитовидщной железы, клетки которой экспрессировали ChETA. Транплантат освещали синим светом по 30 минут один раз в два дня, в течение 28 дней. У этих мышей по сравнению с контрольной группой больных животных снизилась потеря костной массы, скорость формирования новой компактной костной ткани была выше, было больше клеток с маркерами остеобластов (клеток, из которых развивается костная ткань) и меньше остеокластов (клеток, которые отвечают за ее резорбцию), также вырос уровень экспрессии бета-катенина. В совокупности эти результаты говорят о ремоделировании костной ткани и снижение потери костной массы.
Исследование открывает новый подход в лечении гиперпаратиреоза, позволяя обходить или компенсировать негативные эффекты классических методов лечения, отмечают авторы.
Источник
Liu, Y. et al. An optogenetic approach for regulating human parathyroid hormone secretion. // Nature Communications 13, 771 (2022). DOI: 10.1038/s41467-022-28472-9


 Меню
Меню





 Все темы
Все темы




 0
0











