Раковые клетки молочной железы превратили в жировые клетки
Исследователи из Университета Базеля заблокировали способность опухолевых клеток к метастазированию, превратив их в клетки жировой ткани при помощи двух известных терапевтических малых молекул. При этом способность к конверсии оказалась присуща тем клеткам опухоли, которые претерпевают дедифференцировку и ответственны за агрессивность и лекарственную устойчивость новообразования.
Для опухолевых клеток характерна способность к дедифференцировке. Это один из самых главных процессов, вызывающих малигнизацию — эскалацию злокачественности. В норме дедифференцировка активируется во время эмбрионального развития, когда клетки мигрируют с места на место и формируют новые органы и ткани. Повышенная пластичность опухолевых клеток позволяет им быстро приобретать лекарственную устойчивость, защищаться от атаки иммунной системы, осуществлять инвазию в ткани и метастазировать. Однако накопилось достаточно данных о том, что дедифференциацию можно развернуть вспять, блокируя полезные для опухоли, но вредные для организма свойства трансформированных клеток.
Проблема состоит в том, что вновь дифференцированные клетки могут быть способны и к повторной дедифференциации. Швейцарские исследователи предположили, что удачным решением может оказаться транс-дифференциация — иначе говоря, не реверсия фенотипа опухоли, а его конверсия в какой-то иной, высокодифференцированный фенотип. Возможно, вероятность реверсии к злокачественности у таких клеток снизится.
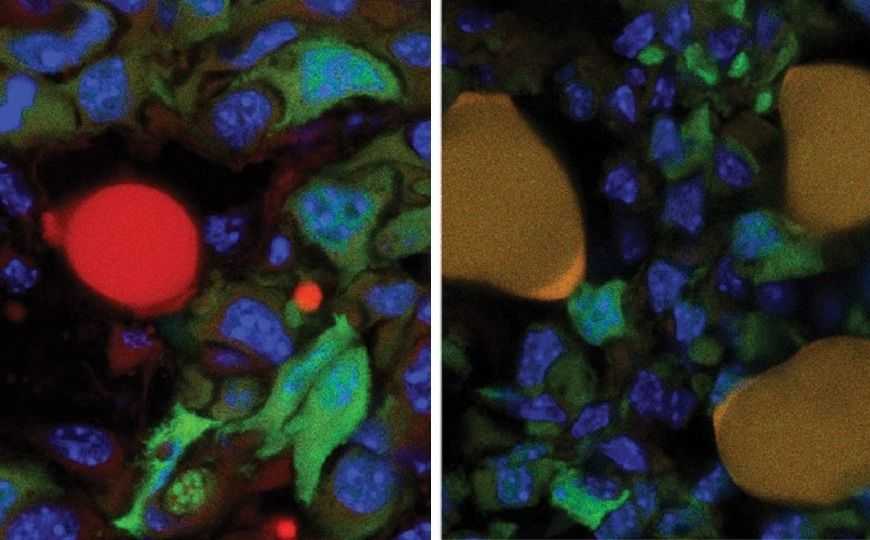
Исследователи попытались конвертировать злокачественные клетки молочной железы мыши, у которых путем индуцибельной рекомбинации с потерей гена Е-кадхерина вызывали метастатический фенотип, в клетки жировой ткани. Способ такой конверсии известен и включает обработку клеток дексаметазоном, инсулином и антидиабетическим препаратом росглитазоном. Неизвестна была реакция злокачественных клеток. Тем не менее конверсия прошла успешно, клетки опухоли стали накапливать жировые гранулы и приобрели другие свойства адипоцитов. Но главное — они утратили злокачественность! Набор транскриптов в процессе превращения опухолевых клеток в жировые изменялся так же, как при формировании жировой ткани, особенно в части блокировки клеточного деления, присущей адипоцитам.
Опухолевые клетки обретают пластичность в ходе так называемого эпителиально-мезенхимального перехода, необходимого для малигнизации. Этот процесс исследователи сумели развернуть в сторону формирования неделящихся адипоцитов: «Тот, кто нам мешает, тот нам поможет!» Как омар или паук во время линьки, клетки опухоли в процессе перестройки оказались уязвимыми к атаке извне. Уместно отметить, что исходные клетки опухоли эпителиального типа, не обладающие метастатическим потенциалом, дифференцировать в адипоциты не удалось.
Оптимальный набор «химического оружия», подобранный в ходе исследования, состоял из росглитазона и белка BMP-2, известного индуктора дифференцировки. Эксперименты с этими факторами позволили выявить сигнальные пути, заблокировав которые, теоретически можно будет вызвать желаемую конверсию. Ключевым компонентом, ингибирование которого приводило к «адипоцитной» дифференцировке, оказалась киназа MEK и путь сигнальной трансдукции MEK-ERK. Поэтому когда к росглитазону добавляли низкомолекулярный ингибитор МEK (trametinib), дифференцировка опухолевых клеток в адипоциты проходила не менее эффективно, чем в системе с BMP-2. Под действием этих веществ, клетки опухоли в организме мыши превращались в адипоциты и теряли способность к метастазированию.
Использование двух одобренных FDA низкомолекулярных ингибиторов значительно повышает шансы на быстрый успех клинических испытаний. Комбинация росглитазона и трабетиниба показала себя эффективной в отношении опухоли, пересаженной мыши от пациента: препараты индуцировали адипогенез и в клетках опухоли человека, также блокируя метастазирование и неконтролируемый рост опухоли. Авторы считают, что предлагаемая терапевтическая стратегия позволит элиминировать наиболее опасные клетки, способные метастазировать, быстро развивать лекарственную устойчивость и проникать в здоровые ткани.


 Меню
Меню





 Все темы
Все темы




 0
0











