Третью хромосому 21, вызывающую синдром Дауна, удалили из клеток с помощью CRISPR-Cas9
Японские ученые удалили лишнюю хромосому 21 из культивируемых клеток с трисомией. Редактирующие конструкции были нацелены на определенную хромосому, что позволяло исключить ситуацию, когда в клетке останутся две хромосомы, полученные от одного из родителей. Исследователи показали, что экспрессия генов в клетках с реконструированной дисомией приближается к норме, деление становится активнее, а продукция активных форм кислорода снижается.
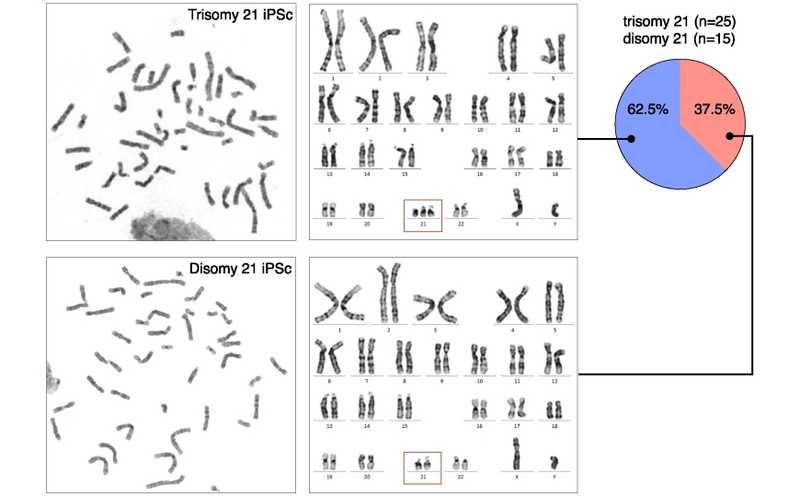
Метафазные кариотипы культивируемых клеток, обработанных CRISPR-Cas9 для элиминации хромосомы 21. Значительная доля клеток вернулась к нормальному кариотипу.
Credit:
PNAS Nexus, 2025, DOI: 10.1093/pnasnexus/pgaf022 | CC-BY-NC
Синдром Дауна, вызванный наличием трех хромосом 21 вместо двух, встречается с частотой примерно 1 на 700 живорождений. Это наиболее распространенная генетическая причина когнитивных нарушений. Его относительно легко диагностировать на ранних стадиях развития, однако лечения не существует.
Известно, что CRISPR-Cas9-редактирование может вызывать потерю хромосом или обширные делеции. Этот эффект рассматривается как нежелательный, но его можно использовать целенаправленно для удаления «лишней» хромосомы. Исследователи из Японии уничтожили с помощью CRISPR-Cas9 третью хромосому 21 в культивируемых клетках. До применения этой технологии хотя бы на животных еще очень далеко, однако на клетках она сработала.
Подобные подходы рассматривали и ранее, но уничтожение третьей хромосомы не было аллелеспецифичным, то есть расщеплена могла быть любая из трех хромосом. Функциональность большинства генов на хромосоме 21 не зависит от того, отцовская это хромосома или материнская. Однако, например, ген молекулы клеточной адгезии DSCAM экспрессируется с отцовской хромосомы, а в материнской его экспрессия подавлена метилированием (это явление называется геномным импринтингом). У генов супероксиддисмутазы типа 1, митохондриального рибосомного белка L39 и SON уровень экспрессии зависит от того, находятся ли они на отцовской или материнской хромосоме. Поэтому имеет значение, какая именно хромосома будет разрушена. Подход, предложенный авторами, — аллельспецифичное таргетирование — позволяет уничтожать определенную хромосому, таким образом, в клетке не останутся две Х-хромосомы от одного родителя.
Ранее авторы создали линию индуцированных плюрипонтентных клеток из фибробластов кожи человека с трисомией 21. В новой работе выбрали мишени для CRISPR в одной из материнских хромосом. Эффективность удаления хромосомы при нацеливании на 13 аллельспецифичных мишеней сравнивали с аллельнеспецифичными.
Клетки с трисомией трансдуцировали вектором, который кодировал редактирующую конструкцию и ген устойчивости к пуромицину. После селекции в присутствии пуромицина исследовали кариотип клеток методами FISH и G-бэндинга. Затем клонировали единичные клетки и проводили STR-анализ, а также полногеномное секвенирование, РНК-секвенирование и MLPA. Исследования показали, что при аллельспецифичном нацеливании теряется преимущественно одна и та же хромосома.
Чтобы повысить долю клеток с потерянной хромосомой, авторы временно ингибировали в клетках способность к репарации двунитевых разрывов, вызываемых CRISPR-Cas9, с помощью коротких интерферирующих РНК.
Структурных аномалий или анеуплоидий по другим хромосомам традиционные цитогенетические методы не выявили, но молекулярные методы обнаружили случаи нецелевого редактирования. После этого авторы сконструировали новую редактирующую конструкцию, нацеленную только на шесть сайтов, по которым нецелевой активности не было. Для нее удалось добиться уровня элиминации хромосомы около 13%.
Удаление лишней хромосомы приблизило к норме как экспрессию генов, так и клеточные фенотипы. В частности, клетки с индуцированной дисомией активнее и быстрее делились, чем исходные клетки с трисомией, и в них снизилась продукция активных форм кислорода.
Эксперимент прошел успешно как с индуцированными плюрипотентными стволовыми клетками, так и с дифференцированными фибробластами, то есть предложенная технология оказалась эффективной и в неделящихся клетках.
Ранее предпринимались попытки коррекции трисомии путем вставки летального трансгена или гена инактивации X-хромосомы XIST в третью хромосому. Однако и тот, и другой подход требуют модификации генома, что неприемлемо для применения в клинике. По мнению авторов, их подход проще. Но очевидно, что для его использования in vivo необходимо решить проблемы доставки редактирующей конструкции, эффективности редактирования, а также добиться отсутствия нецелевого редактирования. Тем не менее авторы считают, что подобные подходы когда-нибудь могут быть применены для редактирования нейронов и глиальных клеток и разработки новых медицинских вмешательств при синдроме Дауна.
Пероральный препарат улучшил когнитивные функции при синдроме Дауна
Источник
Ryotaro Hashizume, et al. Trisomic rescue via allele-specific multiple chromosome cleavage using CRISPR-Cas9 in trisomy 21 cells // PNAS Nexus, 4, 2, February 2025, pgaf022. DOI: 10.1093/pnasnexus/pgaf022


 Меню
Меню





 Все темы
Все темы




 0
0










