Живая аттенуированная вакцина против чикунгуньи прошла фазу 3 КИ
Чикунгунья, вирусное заболевание, переносимое комарами, распространено в некоторых регионах Африки, Азии, Северной и Южной Америки. Разрешенной вакцины против чикунгуньи до настоящего времени не было. Австрийские ученые опубликовали результаты фазы 3 клинических испытаний живой аттенуированной вакцины-кандидата VLA1553. После одной дозы вакцины титры нейтрализующих антител были выше защитного порога у 98,9% участников. Вакцина хорошо переносилась, двое людей с серьезными нежелательными явлениями полностью выздоровели.
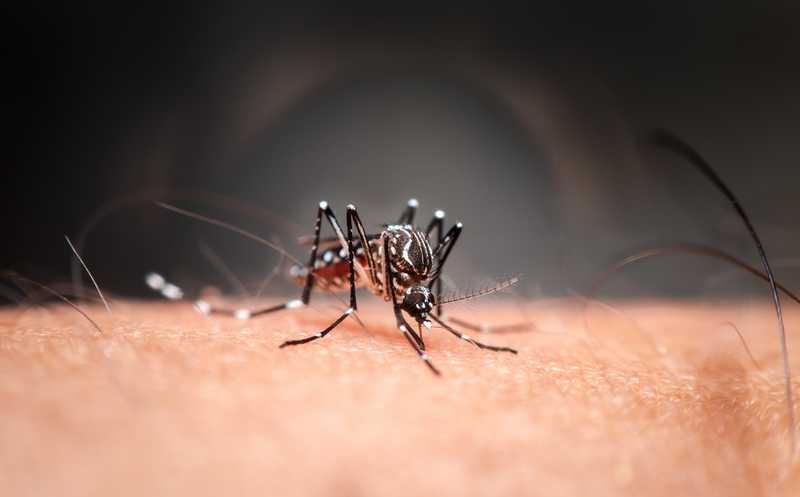
Чикунгунья — вирусное заболевание, переносимое комарами. Встречается в некоторых регионах Африки, Азии, Северной и Южной Америки. За последние 15 лет сообщалось о пяти миллионах случаев заражения. Через 4–8 дней после укуса комара у зараженного развивается лихорадка. Другие симптомы включают в себя головную боль, тошноту, сильную боль в мышцах и суставах. Боль в суставах обычно длится несколько дней, но может сохраняться годами. У детей и людей старшего возраста выше риск неблагоприятного исхода. В настоящее время не существует вакцины или эффективного противовирусного препарата.
VLA1553 — живая аттенуированная вакцина-кандидат, таргетирующая все циркулирующие штаммы вируса чикунгуньи. Вакцина выполнена на основе штамма La Reunion (LR2006-OPY1). Делеция 61 аминокислоты в неструктурном белке 3 аттенуирует вирус. Иммуногенность и сероконверсию при использовании вакцины продемонстрировали в предыдущих клинических испытаниях. Также выбрали оптимальную дозу. В новой работе австрийские ученые представили результаты фазы 3 клинических испытаний вакцины.
В испытании приняли участие 4115 здоровых человек. Их случайным образом распределили в группы, получавшие вакцину или плацебо. Одну дозу препарата вводили внутримышечно. Безопасность и иммуногенность вакцины оценивали через 7, 28, 84 и 179 дней после вакцинации.
Через 28 дней титры нейтрализующих антител были выше защитного порога у 98,9% участников (эффективность вакцины оценивали не у всех рандомизированных участников). Значимой разницы между пациентами 18–64 лет и 65 лет и старше отмечено не выло. Через 180 дней 96,3% участников по-прежнему имели высокие титры нейтрализующих антител.
Уровень сероконверсии через 28 дней составил 99,2%; у 98,3% участников антитела сохранялись в течение периода наблюдения. У двух участников нейтрализующих антител выявлено не было, у одного участника антитела были, но их титры были ниже защитного порога.
VLA1553 в целом хорошо переносилась у всех испытуемых, даже у людей старшего возраста. Нежелательные явления чаще встречались в группе, получившей вакцину, чем получившей плацебо. Только два серьезных нежелательных явления были признаны связанными с вакцинацией. У 58-летней женщины развилась умеренная миалгия, которая потребовала госпитализации. У пациентки была история фибромиалгии. Также у 66-летнего мужчины были зафиксированы лихорадка (39,6°C), мерцательная аритмия и гипонатриемия, потребовавшие госпитализации. Оба пациента выздоровели. Остальные нежелательные явления были в основном легкими или умеренными. Клинические анализы не изменились. Также 15% участников испытывали нежелательные явления, связанные с местом укола, такие как повышенная чувствительность.
В ходе испытания 15 участниц забеременели, из них 13 получали VLA1553. Девятеро родили здоровых детей, три беременности завершились выкидышем, данных по еще одной участнице нет. Исследователи не признали связи между выкидышами и вакцинацией.
Таким образом, фаза 3 клинических испытаний завершилась успешно: под действием вакцины через 28 дней у 98,9% участников титры антител достигли защитного уровня и держались в течение 180 дней. По мнению авторов, это говорит о потенциальной хорошей защите от чикунгуньи. VLA1553 хорошо переносилась, даже два серьезных нежелательных явления полностью разрешились. Процент выкидышей у участниц был немного выше, чем в общей популяции, но авторы связывают это с малыми размерами когорты. Чикунгунья обычно не связана с повышенным риском выкидышей.
Исследование проходило в регионе, где чикунгунья не распространена, поэтому нельзя было оценить эффект уже существующего иммунитета на иммуногенность вакцины, как и полный профиль безопасности. Также вакцина основана на живой аттенуированной вирусной платформе, так что, скорее всего, не подойдет для людей с серьезными нарушениями работы иммунитета. В дельнейшем требуется проведение исследования на детях, а также оценка долговременного эффекта вакцинации.
Источник:
Martina Schneider, et al. Safety and immunogenicity of a single-shot live-attenuated chikungunya vaccine: a double-blind, multicentre, randomised, placebo-controlled, phase 3 trial // The Lancet (2023), published June 12, 2023, DOI: 10.1016/S0140-6736(23)00641-4


 Меню
Меню





 Все темы
Все темы




 0
0











