Нобелевская неделя 2025. Мэри Брункоу о мышах из Ок-Риджской лаборатории и открытии гена FOXP3
«FOXP3 стал для исследователей ключом, открывшим для них целый новый мир регуляторных Т-клеток. Теперь мы знаем, что FOXP3 программирует регуляторные Т-клетки и направляет их дифференцировку, а мощь регуляторных Т-клеток используется для разработки терапии аутоиммунных заболеваний, рака и реакции отторжения трансплантата». — Лекция лауреата Нобелевской премии 2025 года по физиологии или медицине Мэри Брункоу. Стокгольм, 07.12.2025.

Мэри Брункоу начала свою лекцию с благодарностей наставникам — Лэрри Сэндлеру, эксперту в генетике дрозофил из Вашингтонского университета (Сиэтл), и Ширли Тилгман, молекулярному биологу из Принстонского университета. В лаборатории Сэндлера Мэри Брункоу провела полтора года в начале своей карьеры и благодаря ему поняла, что хочет посвятить себя исследованиям, хотя до этого собиралась стать врачом. А диссертацию Мэри Брункоу писала под научным руководством Тилгман, и этот опыт развил в ней критическое мышление и непредвзятость.
Исследования, которые привели к открытию гена FOXP3, изначально не были посвящены иммунологической толерантности — способности иммунной системы реагировать на чужеродные антигены, при этом не реагируя на собственные. Ученых больше интересовало состояние иммунитета, при котором толерантность нарушается и возникают аутоиммунные заболевания, отторжение трансплантатов и т.д. Используя генетический подход, они хотели найти мишени для дальнейшей разработки лекарств против таких состояний.
История FOXP3 началась с линии мышей scurfy (англ. «паршивый, покрытый чешуйками»). В Ок-Риджской национальной лаборатории, которая была создана в рамках Манхэттенского проекта, не только разрабатывали ядерное оружие, но также исследовали влияние радиации на организм. Секцией генетики млекопитающих в этой лаборатории руководили Уильям и Лиана Расселл, которые получили множество мутантных линий мышей.
Большинство этих линий появились из-за воздействия радиации, но мутация, характерная для линии scurfy, была спонтанной. Впервые этих мышей описали в 1949 году, и в течение 40 лет после этого линия мышей поддерживалась, но не исследовалась. Самцы линии scurfy (это была первая описанная Х-сцепленная мутация у мышей, и фенотипические аномалии проявлялись именно у самцов, поскольку у них одна Х-хромосома) отличались крайним истощением, шелушением кожи, патологическим увеличением селезенки, печени и лимфоузлов, при этом тимус, напротив, был уменьшен. На фото слева представлен самец линии scurfy, а справа — самка, обладающая нормальным фенотипом несмотря на носительство мутации.

В 1980-х годах патогенез мутации, вызывающий фенотип scurfy, был подробнее описан Вирджинией Годфри и Джоном Уилкинсоном. Они показали, что у животных развивается лимфопролиферативное заболевание, которое каким-то образом вызвано бесконтрольно активируемыми CD4+ Т-клетками и сопровождается повышением уровня цитокинов. Это заболевание, которое приводило к гибели самцов примерно за три недели жизни, посчитали аутоиммунным.
В 1990-х годах Мэри Брункоу работала в биотехнологической компании Darwin Molecular Corporation, которая искала новые мишени для лекарств против аутоиммунных заболеваний, рака и ВИЧ. У одного из основателей компании, Дэвида Галаса, были связи с Ок-Риджской национальной лабораторией — так Darwin Molecular, заинтересовавшись мышами с необычным аутоиммунным заболеванием, получила линию scurfy.
В 1994 году перед Мэри Брункоу поставили задачу найти мутацию, вызывающую этот фенотип. В компании не было специального вивария, поэтому лабораторных животных содержали в мало используемой кладовке.
Брункоу решила сузить интервал для поиска гена, мутация в котором вызывает фенотип scurfy: для этого она проводила масштабные эксперименты по обратному скрещиванию мышей, чтобы выявить новые рекомбинационные события. В 1990-е годы такая задача картирования геномных локусов была нетривиальной: ученые не располагали полной последовательностью генома, но при этом сравнивали свои результаты с картами, полученными другими, опираясь на уже известные маркеры.
Благодаря финансовым возможностям компании ученые получили доступ к передовым на тот момент технологиям, получившим развитие благодаря проекту «Геном человека»: получение библиотек кДНК, автоматизированное секвенирование и т.д. Используя самые современные подходы в молекулярной биологии и биоинформатике, Мэри Брункоу совместно с Эриком Джеффери, Кэтрин Хьеррилд и Брайаном Пэйпером сузили интервал, в котором находилась мутация, до участка Х-хромосомы длиной примерно в 500 тысяч пар оснований. С помощью биоинформатических инструментов BLAST и GENSCAN определили, что в этом участке находится всего 20 генов. Некоторые из них были уже известны, другие оказались новыми.
Сравнивая последовательности генов у животных дикого типа и мутантных животных, ученые обнаружили, что последний из 20 генов, который они проверили, вызывает фенотип scurfy.
 Cтраница из лабораторного журнала Кэтрин Хьеррилд, где описано обнаружение мутации
Cтраница из лабораторного журнала Кэтрин Хьеррилд, где описано обнаружение мутации
Изначально ген называли FKH из-за высокой гомологии с белками — транскрипционными факторами семейства Forkhead. Фенотип scurfy вызывался инсерцией двух аденинов в этом гене со сдвигом рамки считывания в участке гена, который кодировал ДНК-связывающий домен белка.
Исследователи также нашли ортолог гена FKH у человека. Полученные последовательности человеческого и мышиного гена они передали в Номенклатурный комитет, задачей которого было валидировать их результаты и присвоить имя найденному гену. В результате ген получил название Foxp3.
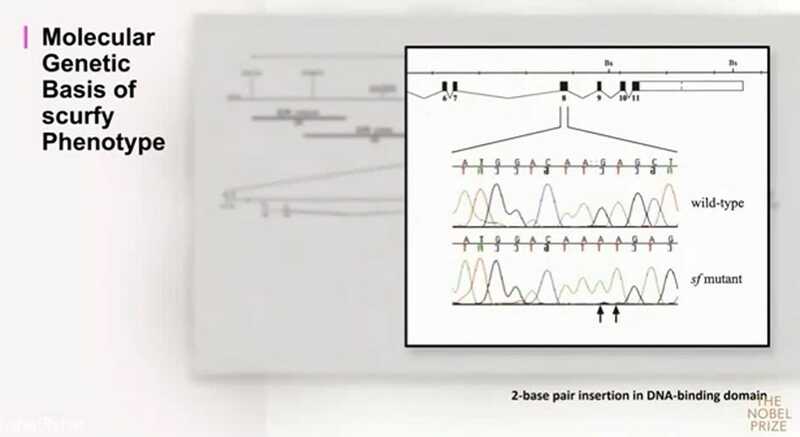
Чтобы подтвердить, что именно мутация в гене Foxp3 вызывает фенотип scurfy, ученые клонировали последовательность Foxp3 дикого типа и доставили ее в ооцит мыши линии scurfy. После доставки трансгена самцы-носители мутации приобрели нормальный фенотип: в частности, их лимфоузлы уменьшились до нормальных размеров. По результатам работы в 2001 году была опубликована статья в Nature Genetics.
Аналогичное фенотипу scurfy у мышей состояние у людей называется синдромом IPEX, по первым буквам основных признаков: иммунодисрегуляция, полиэндокринопатия, энтеропатия, X-сцепленность. Брункоу вместе с коллегами, которые работали с пациентами, имеющими этот синдром, установили, что это заболевание также вызывается мутациями в гене FOXP3. При этом степень тяжести болезни зависит от самой мутации: всего их было известно больше 170. Это открытие напрямую повлияло на то, как врачи теперь работают с пациентами с синдромом IPEX: при подозрении на такой диагноз пациенту назначают генетический анализ локуса FOXP3.
FOXP3 оказался высококонсервативным среди позвоночных транскрипционным фактором. Однако с точки зрения разработки лекарств эта мишень неудачная, что отмечал в своем выступлении и другой нобелиат 2025 года, Фред Рамсделл. Этот белок находится в ядре, поэтому малыми молекулами или биотехнологическими препаратами на него воздействовать тяжело.
Мэри Брункоу рассказала о другом своем проекте, которым занималась параллельно с исследованием мышей scurfy. Его результатом стало открытие гена SOST, который вызывает склеростеоз — аутосомно-рецессивное заболевание, для которого характерно избыточное образование плотной костной ткани. Используя тот же подход, что и с мышами линии scurfy, но с материалом от пациентов с склеростеозом, ученые идентифицировали ген SOST, кодирующий склеростин — белок из семейства секретируемых антагонистов BMP (костных морфогенетических белков). С точки зрения разработки лекарств эта мишень оказалась более удачной: не секретируемый белок легче воздействовать, а сигналинг, связанный с BMP, тогда был уже хорошо известен. На данный момент одобрены к применению лекарства, действующие на склеростин: например, моноклональное антитело ромосозумаб ингибирует склеростин и используется для лечения остеопороза.
И все же открытие FOXP3 позволило исследовать различные сигнальные пути, находящиеся под регуляцией этого белка — в таком случае воздействовать лекарствами можно на их компоненты, а не на сам FOXP3. После открытия гена исследователи показали, что FOXP3 экспрессируется на маленькой (5–10%) популяции CD3+ Т-клеток, которые также экспрессируют CD25. Позднее эти клетки назвали регуляторными Т-клетками, а FOXP3 оказался не просто их маркером, но и ключевым для программирования их «идентичности» фактором. Многие подходы к лечению аутоиммунных заболеваний, рака и других заболеванием основаны на использовании регуляторных Т-клеток.
В заключение Мэри Брункоу поблагодарила всех сотрудников разных лабораторий, причастных к открытию FOXP3.


 Меню
Меню





 Все темы
Все темы




 0
0