Валерия Высоцкая: «Для меня удивительно, что в Москве нет полноценной скрининговой программы»
Не существует одного чудодейственного «средства от рака», но победы над конкретными видами рака — это реальность сегодняшней медицины. Три года назад, в ноябре 2020 года, Всемирная организация здравоохранения представила Глобальную стратегию по ускорению ликвидации рака шейки матки — четкую программу действий, которые уничтожат РШМ как проблему общественного здравоохранения. Первый шаг, который нужно сделать в том числе и нашей стране, — организация массового скрининга женщин. А для этого необходимы современные технологии.
На вопросы PCR.NEWS отвечает Валерия Николаевна Высоцкая — врач клинической лабораторной диагностики, Московский многопрофильный клинический центр «Коммунарка».

Валерия Николаевна, вы как опытный цитолог и при этом молодой прогрессивный специалист, в чем видите основные тренды в цитологии в России?
Цитология давно используется как эффективный метод в скрининге рака шейки матки, но не ограничивается только этим. Тонкоигольная аспирационная биопсия (ТАБ) образований щитовидной, молочной, слюнных желез широко применяется для предоперационной диагностики и выработке тактики лечения пациентов. Также я наблюдаю возвращение цитологии в область интересов врачей-патологоанатомов, что очень важно и радостно для меня. Патоморфология активно развивается, и без цитологии сейчас сложно представить эффективную диагностику. Также важно отметить внедрение молекулярно-генетических исследований в клинику, и все чаще для этого используются цитологические образцы.
Вы упомянули скрининговые исследования. Можно поподробнее?
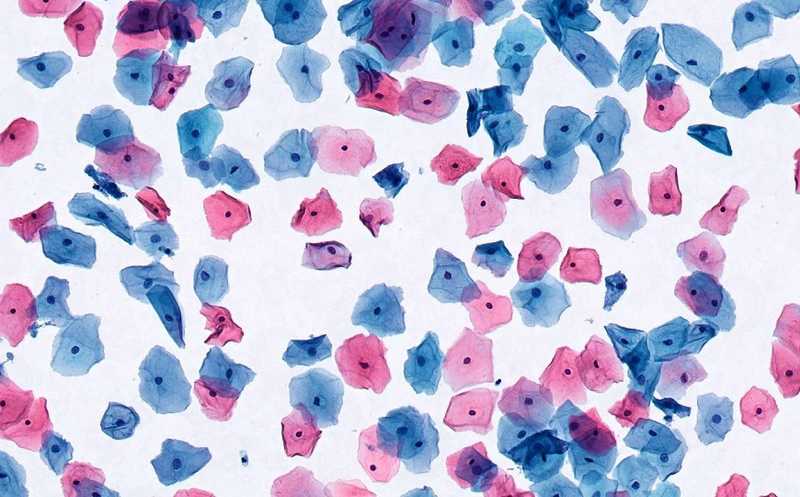
Конечно. Цитологическое исследование цервикальных мазков уже более 60 лет используется как эффективная скрининговая стратегия для предотвращения смертей женщин от рака шейки матки. Своевременное обнаружение предраковых состояний — залог успешного лечения. Даже несмотря на внедрение новых тестов, таких как ПЦР, для выявления вируса папилломы человека (этиологический фактор развития рака шейки матки), цитология не исключается из стратегии по элиминации рака шейки матки ВОЗ и используется повсеместно. Это простой и дешевый тест, который носит имя его изобретателя – американского цитопатолога Георгиоса Папаниколау. Пап-тест был внедрен впервые в США в начале 50-х годов ХХ века и за это время показал свою невероятную эффективность. По данным проекта ВОЗ Global Cancer Observatory, в некоторых странах, например, в Финляндии, где массовый скрининг проводится с 1960-х годов, удалось добиться снижения смертности от РШМ до менее 1 женщины на 100 000 женского населения. К сожалению, в России этот показатель остается на очень высоком уровне, порядка 8 случаев на 100 000 населения, также мы отмечаем ежегодный рост данного показателя и «омоложение» рака шейки матки.
 Из
доклада к.м.н. П.Д. Лопухова (Института общественного здоровья им. Ф.Ф. Эрисмана Сеченовского университета) на конференции «Молекулярная диагностика 2023»
Из
доклада к.м.н. П.Д. Лопухова (Института общественного здоровья им. Ф.Ф. Эрисмана Сеченовского университета) на конференции «Молекулярная диагностика 2023»
Почему это происходит в нашей стране?
Прежде всего, когда мы говорим о скрининговых исследованиях, стоит отметить необходимые для их эффективности условия — охват более 80% человек в целевой группе по конкретной нозологии и использование проверенных методик скрининга. Абсолютно ясно, что данные условия возможно выполнить только при полной и постоянной поддержке государства.
Мы живем в очень большой стране, население которой чрезвычайно разнообразно и по традициям, и по условиям жизни. Существуют регионы, где работают местные законодательные акты, регулирующие скрининг рака шейки, однако, к сожалению, большой общероссийской программы популяционного скрининга не существует. В регионах, где местные власти смогли наладить данные процессы эффективно, мы видим снижение смертности от РШМ. Хорошим примером может служить Тамбовская область. Масштабирование тамбовского опыта на всю страну может изменить ситуацию к лучшему.
Для меня удивительно, например, что в Москве до сих пор нет полноценной скрининговой программы, особенно учитывая очень высокий уровень оказания медицинской помощи в столице. Я, как сотрудник крупной московской больницы, стараюсь отработать некоторые аспекты стратегии скрининга РШМ в рамках своей работы в цитологической лаборатории, и, возможно, в скором времени мы получим возможность разработки московского стандарта скрининга РШМ.
Расскажите, пожалуйста, подробнее о жидкостной цитологии. Чем она отличается от традиционного Пап-мазка?
Да, это относительно новая технология, разработанная в США. Она отличается прежде всего стандартизацией методики забора самого цервикального мазка. В традиционной методике Пап-теста материал с поверхности шейки матки и цервикального канала, взятый при рутинном гинекологическом осмотре при помощи специальной щеточки, наносится непосредственно на предметное стекло и должен быть зафиксирован спиртом. При этом до 70 % клеток остаются на щеточке и выбрасываются без возможности их дальнейшей оценки.
В случае жидкостной цитологии используется такая же щеточка, но ее необходимо погрузить в специальную транспортную пробирку — виалу, которая содержит фиксатор. При этом 100% полученных клеток отправляются в лабораторию и обработка материала происходит уже там с использованием высокотехнологической аппаратуры. Гинеколог или акушерка в этом случае застрахованы от ошибок при нанесении мазка на стекло и в большей степени от ответственности за сохранность материала. Эти виалы, как правило, не требуют соблюдения жестких условий хранения и транспортировки, клетки сохранятся надолго, и имеется возможность их использования для дополнительных методов, таких как ПЦР или иммуноцитохимия.
Интересно, но если технология американская, то как же сейчас обстоят дела в условиях санкционного давления? Ведь известно, что западные страны ограничили использование даже некоторых медицинских технологий для России.
Действительно, до недавнего времени большая часть оборудования, используемая в России для жидкостной цитологии, была именно американского производства. Однако патентное законодательство достаточно мягко работает в данном случае и сейчас мы имеем на рынке аппараты производства Южной Кореи и КНДР.
Сейчас имеются новые аппараты с полной автоматизацией процесса приготовления образца. Это технология позволяет получать препараты, не уступающие по качеству американским аналогам при условии автоматизации процессов. Аппаратура компактна, не занимает много места в лаборатории и освобождает руки лаборантов.
Валерия Николаевна, а сравнивали ли вы американскую технологию с азиатской по результату цитологического исследования и возможности выполнения ПЦР?
Общеизвестно, что из цитологических виал таких марок, как BD SurePath производства американской Becton Dickinson и корейской YD EasyPrep, можно выявлять 14 генотипов ВПЧ, отнесенные ВОЗ к вирусам высокого онкогенного риска, с помощью наборов российского производства. Мы сделали сравнение результатов этих систем. Образцы пациенток собрали в виалы BD SurePath и, сразу же в виалы YD EasyPrep. Результаты получены независимо, было слепое исследование. Стекла смотрели разные цитологи, с этим, возможно, связано некоторое отличие, а также с тем, что в разные виалы могли попасть разные клетки. Результаты по ВПЧ из материала в виалах совпали.
|
Год рождения пациентки |
ВПЧ виала BD
|
ВПЧ виала EasyPrep |
Комментарий по содержимому виалы |
Цитология BD (1-е взятие) |
Цитология EasyPrep (2-е взятие) |
|---|---|---|---|---|---|
|
1986 |
не обнаружено |
не обнаружено |
кровь, 2 щетки |
NILM |
NILM |
|
1993 |
обнаружено |
обнаружено |
сгустки |
HSIL |
HSIL |
|
1990 |
обнаружено |
обнаружено |
кровь |
ASCUS |
LSIL |
|
1987 |
обнаружено |
обнаружено |
слизь |
NILM |
NILM |
|
1984 |
обнаружено |
обнаружено |
слизь, кровь |
HSIL |
HSIL |
|
1991 |
обнаружено |
обнаружено |
сгустки на щетке |
ASCUS |
LSIL |
|
1994 |
обнаружено |
обнаружено |
мутный |
ASCH |
HSIL |
|
1990 |
обнаружено |
обнаружено |
сгустки , кровь |
HSIL |
LSIL |
*NILM — атипичные клетки отсутствуют, LSIL — патологические изменения клеток низкой степени, HSIL — выраженные патологические изменения, ASCUS — атипичные клетки неопределенного значения, ASCH — атипичные клетки, не исключен HSIL
Почему так важна автоматизация?
Скрининг — это обязательно большое количество исследований, максимальный охват населения. Для обработки такого количества мазков необходимо:
-
максимально автоматизировать пробоподготовку;
-
внедрить высокопроизводительное оборудование;
-
минимизировать ошибки ручного труда;
-
минимизировать количество неадекватных препаратов;
-
улучшить качество мазка для снижения скорости просмотра и повышения выявляемости ранних изменений, даже единичных клеток.
Внедрение автоматизированной жидкостной цитологии позволит повысить выявляемость РШМ, снизить долю не установленных диагнозов по стадии РШМ, снизить процент летальности на первом году обнаружения и обеспечить постепенное выполнение максимального охвата скринингом.
Звучит обнадеживающе! То есть повсеместное внедрение жидкостной цитологии поможет предотвратить распространение РШМ?
К сожалению, все не так просто. Необходимо учитывать также кадровый вопрос. Повсеместно отмечается нехватка медицинского персонала, это не так явно в крупных городах, однако в регионах ситуация критическая. Даже при условии закупки качественного оборудования нужно иметь руки, которые будут на этом оборудовании работать, а также глаза врачей, которые будет потом смотреть в микроскоп на эти стекла.
Значит, цитологи на вес золота сейчас?
Да! Причем не только в России, это общемировая тенденция. Сейчас мы в составе рабочей группы разрабатываем проект изменений в законодательстве РФ для решения вопросов допуска специалистов к данной деятельности. В нашей стране были утеряны некоторые традиции в области подготовки кадров, в частности, среднего медперсонала и специалистов без медобразования — биологов. А ведь именно на плечи этих людей в прошлом ложился груз рутинных цервикальных мазков, что было очень удобно и эффективно в СССР. Для подготовки кадров требуются активные незамедлительные меры, иначе эффективного скрининга нам не видать.
Неужели для цервикальной цитологии так значим человеческий фактор?
Безусловно! Для формирования хорошего цитолога требуется время, не менее пяти лет постоянной работы. Это долгий и дорогой процесс, который также невозможно осуществить без поддержки государства и профессиональных сообществ. Конечно, в последнее время мы наблюдаем активное развитие технологий искусственного интеллекта для применения в медицине, однако и здесь нужны опытные специалисты, только уже для обучения нейросетей.
Нейросети? И в цитологии тоже?
Да! Как и в других областях медицинской визуализации, в патоморфологии уже существуют работающие алгоритмы. Это область — одна из самых активно развивающихся в современном мире. Посудите сами, мы стандартизируем методики получения, приготовления и окраски препаратов, и, соответственно, получаем доступный для цифровизации образец. В первую очередь, основа цервикальной цитологии — это банальная морфометрия, с которой прекрасно справляется компьютер. Далее, есть возможность «обучить» машину отмечать тонкие клеточные особенности и сравнивать их с характеристиками нормальных клеток. Современные алгоритмы уже способны на это, что очень помогает в рутинной работе.
Радостно слышать, что есть изменения. Это вселяет надежду на лучшее!
Меня очень вдохновляют изменения, свидетелями которых мы становимся. Это действительно дарит надежду и помогает работать эффективно на благо наших дорогих пациентов.


 Меню
Меню





 Все темы
Все темы




 0
0










