Анна Воронкова: «Муковисцидоз — не приговор»
Какие мутации вызывают муковисцидоз и почему тяжесть заболевания может быть различной, хотя поврежден один и тот же ген? Как ставится диагноз и какие преимущества дают неонатальный и пренатальный скрининг? Почему для лечения болезни, вызванной нарушениями в одном гене, понадобились целых три малых молекулы в одном препарате, и насколько эффективна знаменитая трехкомпонентная терапия? Эти и другие вопросы — в новой лекции проекта «Метафаза».

Четвертого декабря в рамках лектория «Метафаза» прошла лекция «Муковисцидоз — вчера, сегодня, завтра» Анны Юрьевны Воронковой. Анна Юрьевна — ведущий научный сотрудник научно клинического отдела муковисцидоза Медико-генетического научного центра им. академика Н.П. Бочкова, ведущий научный сотрудник отдела метаболических и наследственных заболеваний, врач-педиатр отделения муковисцидоза Научно-исследовательского клинического института детства Министерства здравоохранения МО.
Частый среди редких
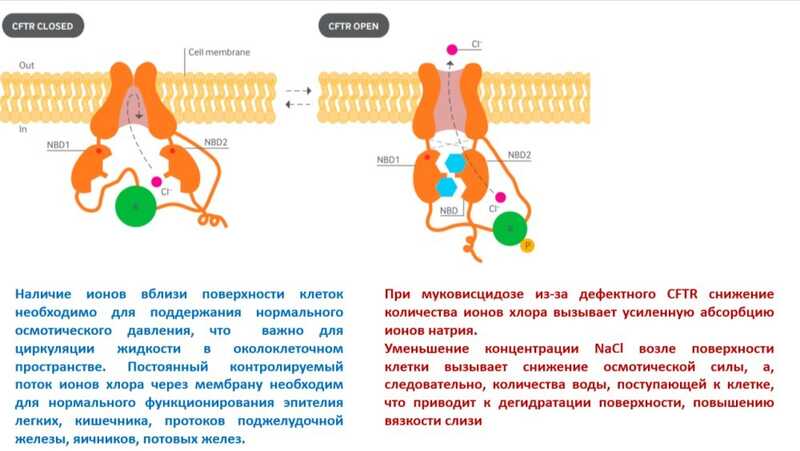
Муковисцидоз (МВ) — одно из самых распространенных орфанных (редких) моногенно наследуемых заболеваний, обусловленное мутациями в гене CFTR, который располагается на длинном плече седьмой хромосомы. Передается патология по аутосомно-рецессивному типу. Продукт этого гена — белок, участвующий в транспорте ионов хлора через мембрану клетки; он также обозначается CFTR (cystic fibrosis transmembrane conductance regulator); русская аббревиатура — МВТР (муковисцидозный трансмембранный регулятор проводимости).
При муковисцидозе увеличивается вязкость секрета экзокринных желез из-за нарушения способности CFTR переносить ионы хлора; это приводит к уменьшению концентрации NaCl возле поверхности клетки, снижению осмотической силы, что нарушает гидратацию слизи. Патология затрагивает потовые и слюнные железы, железы в бронхах, поджелудочной железе, кишечнике, печени, урогенитальном тракте. В результате нарушается функция практически всех органов и систем, что ведет к ранней инвалидизации и смерти. Иногда протоки желез поджелудочной железы страдают уже внутриутробно, из-за чего развивается так называемый мекониевый илеус (врожденная форма кишечной непроходимости) — самое раннее проявление муковисцидоза.
От муковисцидоза страдало множество известных людей — Шопен и его сестра, певец Грегори Лемаршаль, артист Антон Ельчин, триатлонистка Лиза Бентли. Анна Юрьевна отметила, что активный образ жизни и занятия спортом облегчает течение муковисцидоза.
Распространенность муковисцидоза варьируется в разных регионах. Так, в Европе она составляет около одного случая на 2500 человек, а в России — один на 9–10 тысяч. Впервые клиническое проявление этого заболевания — кистофиброз поджелудочной железы — описал в 1936 году знаменитый швейцарский педиатр Гвидо Фанкони. Два года спустя американский патологоанатом Дороти Андерсон дала первое всестороннее описание патологии, в 1947 году появляются другие публикации по теме, а в 1953 году обнаружены повышенные концентрации ионов натрия и хлора в поте больных; на этом наблюдении основан классический метод диагностики муковисцидоза по Гибсону и Куку. В 1961 году американский фонд кистозного фиброза создал сеть аккредитованных центров муковисцидоза.
Ген, вызывающий заболевание, был локализован в 1985–86 гг. Уильямсоном и Броком, а в 1989 году путем позиционного клонирования был открыт ген муковисцидоза и его белковый продукт — CFTR. Тогда же Френсис Коллинз, Лап-Чи Цуй и Джон Риордан открыли первый и наиболее частый патогенный вариант CFTR — F508del. В 1990-х годах разворачиваются международные программы по лечению муковисцидоза; в 1990 году был открыт отдел муковисцидоза в МГНЦ им. Н.П. Бочкова.
Аутосомно-рецессивный тип наследования означает, что если оба родителя — носители мутаций в CFTR, то вероятность рождения ребенка с муковисцидозом составляет 25%, а ребенка-носителя без признаков заболеваний — 50%. Лектор отметила, что «природа не помнит, кто родился в прошлый раз»: следует понимать, что риски постоянны, и если у первого ребенка есть заболевание, при зачатии второго ребенка риск не становится меньше.
На 2023 год в Европейский регистр внесено 56 144 пациента с муковисцидозом; в регистр США 2024 года — около 40 тысяч; в Канаде — 4130; в Австралии и Новой Зеландии — 4174; наконец, в России зарегистрировано 4360 пациентов. При этом частота носительства патогенных мутаций составляет 2–5%. Выявление носителей может происходить при проведении неонатального скрининга, во время обследования членов семьи с историей муковисцидоза, случайно при обследованиях на другие наследственные заболевания, во время пренатальной диагностики (в том числе доноров гамет, что пока не осуществляется в России). Также носителями являются все дети пациентов с МВ.
Необходимо распространять информацию о муковисцидозе и побуждать людей, в особенности тех, кто планирует создать семью, проходить тестирование на носительство патогенных вариантов.
В случае некоторых патогенных мутаций CFTR у носителя даже одного варианта может развиваться CFTR-ассоциированные панкреатит и бесплодие. Носителям этих мутаций рекомендуют регулярные обследования: если это мутации, ассоциированные с панкреатитом, — анализы на амилазу и липазу крови и УЗИ ЖКТ раз в год или чаще; если мутации ассоциированы с бесплодием — консультации репродуктолога, генетика и андролога. Для носителей мутаций рекомендованы консультация генетика по достижении репродуктивного возраста и обследование партнера при планировании беременности.
Муковисцидоз представляет собой хорошо разработанную модель помощи всем пациентам с орфанными заболеваниями. Помощь включает возможность ранней диагностики (неонатальный скрининг) и раннего (до появления симптомов) старта базисной терапии — назначаются дорназа альфа, панкреатические ферменты, специализированное питание, таргетная терапия. Также доступны молекулярно-генетическая диагностика и методы определения разницы кишечных потенциалов и форсколиновый тест на кишечных органоидах, которые позволяют уточнить диагноз, подобрать CFTR модуляторы к редкому генотипу. Научно-исследовательский клинический институт детства — один из немногих центров в мире, проводящих комплексный подбор таргетной терапии на основе пяти этапов генетического анализа и функциональных тестов, в том числе для уникальных, ранее не описанных мутаций.
Принятая ВОЗ и международными ассоциациями классификация МВ включает в себя три категории:
-
классический муковисцидоз с панкреатической недостаточностью (смешанная или легочно-кишечная форма);
-
классический МВ с ненарушенной функцией поджелудочной железы (преимущественно легочная форма) — около 15% пациентов, мягкие патогенные варианты;
-
неопределенный диагноз с положительным результатом неонатального скрининга.
К заболеваниям, ассоциированным с геном CFTR, относятся изолированная обструктивная азооспермия, хронический панкреатит, диссеминированные бронхоэктазы.
Диагностика
Далее Анна Юрьевна рассказала о развитии диагностики МВ в России. До 2006 года диагнозы ставились преимущественно по клиническим проявлениям — определение хлоридов по тесту Гибсона-Кука, определение проводимости пота, разности назальных потенциалов (в Москве и Санкт-Петербурге). В 2006–2007 гг. появились пилотные проекты по внедрению неонатального скрининга в Москве и области, а технологии автоматического теста на проводимость пота (Nanoduct и Macroduct+Sweat-Check) начали применяться в большинстве регионов РФ. Распространение неонатального скрининга выявило большее число пациентов с муковисцидозом, нежели при диагностике по клиническим проявлениям.
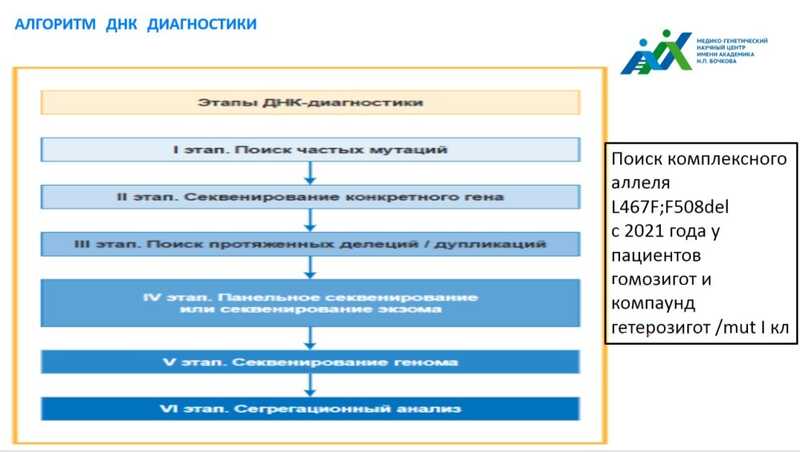
Число тестируемых мутаций росло с 23 в 2000 году до 27 в 2010-м. С 2016 года первый этап диагностики — тест, включающий более 35 частых мутаций, затем проводится секвенирование гена CFTR и MLPA. В 2018–2019 гг. были внедрены методы определения разности кишечных потенциалов и тесты на кишечных органоидах.
Диагноз МВ устанавливается при наличии одного из признаков в двух блоках диагностики. Первый — положительная потовая проба, или две патогенных мутации в CFTR в транс-положении, или положительный результат ОРКП/ОРНП. Второй — положительный неонатальный скрининг (неонатальная гипертрипсиногенемия) или клинические признаки МВ (диффузные брохоэктазы, патогенная микрофлора, экзокринная панкреатическая недостаточность и др.).
Анна Воронкова подчеркнула, что положительный результат скрининга — это еще не диагноз, а лишь повод провести комплексное обследование. Так, если при положительном скрининге у ребенка оказывается нормальная потовая проба, это свидетельствует об отсутствии муковисцидоза. При этом скрининг значительно повышает шансы выявить тех редких детей, у которых действительно есть МВ еще до появления симптомов.
История неонатального скрининга в РФ началась в 1980-х гг. с тестов на фенилкетонурию. В 1993 году были введены тесты на врожденный гипотиреоз; в 2006-м — на врожденный андрогенитальный синдром, муковисцидоз и галактоземию. В конце 2023 года начала работу программа расширенного неонатального скрининга на 36 врожденных заболеваний, включая нарушения обмена веществ, иммунодефицитные состояния, спинальные мышечные атрофии.
Развитая система скрининга бесполезна без четкой системы оказания медпомощи пациентам, особенно в случае муковисцидоза, который требует лечения на протяжении всей жизни. Именно по этой причине начиная с 1961 года по всему миру организуют центры муковисцидоза.
Неонатальный скрининг позволяет выявить реальную частоту заболевания (в России до введения скрининга предполагалась частота 1:4900, сейчас она оценивается в 1:9000-10000), а также повысить выживаемость, предотвратить развитие осложнений и снизить частоту заболевания в популяции за счет предотвращения повторных случаев рождения больных детей в семье. Ранняя постановка диагноза также способствует психологической адаптации родителей и ребенка к болезни, повышает приверженность к лечению.
Схема неонатального скрининга на МВ в РФ в настоящее время выглядит так. Через 1–2 суток после рождения проводится тест крови на иммунореактивный трипсин (ИРТ). При выявлении повышенного уровня на 21–28-й день выполняется повторный тест. Если повышение ИРТ сохраняется, проводят потовую пробу, которая подтверждает или отвергает диагноз МВ. При положительных или пограничных значениях потовой пробы осуществляют ДНК-анализ на выявление патогенных вариантов МВ. При их отсутствии продолжается наблюдение за ребенком, проводятся повторные потовые пробы, секвенирование CFTR, тесты на кишечные потенциалы.

Анна Юрьевна рассказала о восемнадцатилетнем опыте использования неонатального скрининга в Институте детства. За этот период возраст установления диагноза снизился с 3,6 до 0,2 лет, у пациентов повысилась функция внешнего дыхания, снизилась доля патогенной микрофлоры дыхательных путей; частота хронической инфекции синегнойной палочкой снизилась с 28,6% до 2,4%. Рост пациентов в перцентилях после введения скрининга увеличился с 21,7 до 57,4 при норме в 50. Доля применения ингаляционных антибиотиков упала с 75% до 28,57%; бронхолитиков — с 90% до 47,62%.
Если ребенок не проходил неонатальный скрининг, диагностика проводится по клиническим проявлениям. Группы риска включают бронхолегочные нарушения (рецидивирующие пневмонии и бронхиты, бронхиальная астма, торпидная к терапии, и др.), изменения со стороны ЖКТ (гиперэхогенность кишечника во внутриутробном периоде, цирроз печени, сахарный диабет и др.), патологии со стороны других органов (нарушения роста и полового развития, бесплодие, хронический синусит и полипы носа, синдром псевдо-Барттера) и семейная история МВ. При этом для разных возрастных групп характерны различные клинические проявления. Так, у взрослых пациентов может развиваться хронический панкреатит, бесплодие, бронхолегочный аспергиллез и др.
Золотым стандартом для диагностики МВ все еще остается потовый тест. В классическом тесте по Гибсону–Куку норма — это содержание хлоридов менее 30 ммоль/л; пограничное значение — 30–59 ммоль/л; положительным тест считается при 60-150 ммоль/л. При автоматическом анализе — определение проводимости системами «Макродакт» и «Нанодакт» — эти значения составляют <50, 50-79 и 80-160ммоль/л соответственно.
Среди множества клинических проявлений МВ Анна Воронкова особо выделила муковисцидоззависимый сахарный диабет, риск развития которого повышается с возрастом.
Комплексная клиническая картина МВ стала одной из главных мотиваций создания специализированных центров муковисцидоза, поскольку при таком широком разнообразии симптомов полноценное лечение в обычных условиях невозможно. Анна Юрьевна привела 18 основных принципов наблюдения и оказания медпомощи пациентам с МВ. Список включает в том числе амбулаторное наблюдение, многопрофильный стационар, микробиологический мониторинг, ДНК-диагностику, сопровождение эндокринолога, психолога, диетолога и социальной службы, возможность трансплантации легких, печени, сердца и почек.
Схема терапии пациентов с муковисцидозом включает высококалорийное питание, питьевой режим и высокое потребление соли для компенсации потерь организма.
Пациентам со смешанной формой требуется заместительная ферментная терапия панкреатическими ферментами. Также нужны витаминотерапия жирорастворимыми витаминами А, Д, Е, К; уросодезоксихолевая кислота для разжижения густой желчи; муколитическая и бронхолитическая терапия; кинезитерапия (удаление мокроты); противовоспалительная (ГКС, макролиды) и антибактериальная терапия. При возникновении осложнений необходимо их целенаправленное лечение. Также важную роль играют трансплантация органов и паллиативная помощь. В настоящее время в связи с появлением эффективных CFTR модуляторов важное значение для продолжительности и качества жизни приобретает возможность применения таргетной терапии муковисцидоза.
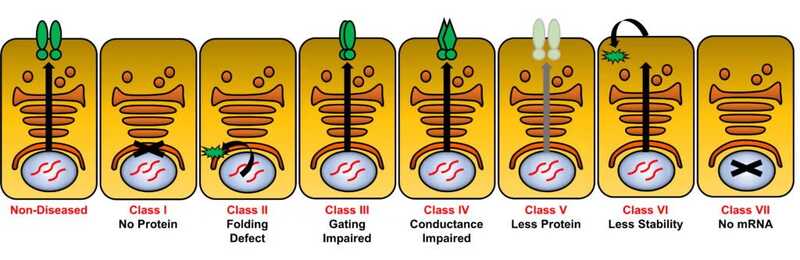
К настоящему времени описано 1085 патогенных вариантов гена CFTR, которые делятся на шесть классов (или семь, согласно другой классификации, выделяющей в класс VII обширные делеции и другие нарушения, при которых отсутствует мРНК). Классы I–III соответствуют смешанной форме с панкреатической недостаточностью. При этих мутациях белок или не синтезируется, или не доходит до апикальной мембраны, или полностью теряет свою функцию. Классы IV–VI — так называемые мягкие мутации, вызывающие преимущественно легочную форму МВ. При таких патогенных вариантах белок попадает на апикальную мембрану в недостаточном количестве или быстро разрушается.
Классы мутаций, в свою очередь, влияют на выбор таргетной терапии. Нарушения, которые сопровождаются полным отсутствием белка (классы I и VII), на данный момент не поддаются терапии CFTR-модуляторами.
Лечение, которое спасает жизни
В 2025 году престижную американскую премию Ласкера присудили Майклу Уэлшу, Хесусу Гонсалесу и Полу Негулеску за создание трехкомпонентной таргетной терапии.

Работы Майкла Уэлша позволили определить функции белка CFTR, он же выдвинул предположение, что нарушение этих функций можно восстановить фармакологически. Хесус Гонсалес разработал метод флуоресцентного анализа, в котором использовался краситель для клеточных мембран, обнаруживающий изменения мембранного потенциала. Этот подход, применяемый при скрининге лекарств от МВ, позволяет тестировать до 10000 препаратов в сутки. Пол Негулеску руководил разработкой трехкомпонентного препарата. В рамках исследования проводились скрининги препаратов на способность компенсировать неспособность белка к созреванию и доставке к апикальной мембране или нарушения открытия ионного канала. Идея была в том, что для исправления двух этих дефектов нужна не одна, а две разные малые молекулы. Почему же в итоге препарат трехкомпонентный?
Первым препаратом, эффективным при МВ, был ивакафтор, восстанавливающий функцию открытия ионного канала, но он не работал у пациентов с мутацией F508del, у которых белок не доходит до мембраны. Вторым препаратом стал лумакафтор, помогающий белку созреть и достичь мембраны при наличии мутации F508del. Комбинация этих двух препаратов была одобрена FDA в 2015 году. Однако затем выяснилось, что лумакафтор не только имеет множество побочных эффектов, но и разрушает ивакафтор. В более поздних разработках лумакафтор заменили на тезакафтор. Комбинация ивакафтора и тезакафтора была одобрена FDA в 2018 году. Третьим препаратом стал элексакафтор, повышающий эффективность первых двух веществ. Комбинация трех препаратов облегчала симптомы у пациентов с мутацией F508del в обеих копиях гена или F508del и другой мутацией — это 90% всех пациентов с МВ. Комбинированный препарат элексакафтор/тезакафтор/ивакафтор получил одобрение FDA в 2019 году.
В настоящее время существует пять препаратов, предназначенных для лечения МВ. Из них два имеют регистрацию в РФ — ивакафтор+лумакафтор и элексакафтор+ивакафтор+тезакафтор. При этом происходит постепенная отмена двухкомпонентной терапии и переход на трехкомпонентную.
Для пациентов с уникальными мутациями проводятся функциональные тесты на кишечных органоидах, чтобы определить эффективность лекарственных препаратов. Для этого органоиды обрабатываются форсколином, который в норме вызывает набухание. При МВ форсколин не попадает в клетку и набухания не происходит, но если препарат восстановил функцию CFTR, набухание под действием форсколина возвращается.

С 2021 года в РФ детям доступна трехкомпонентная таргетная терапия элексакафтор+тезакафтор+ивакафтор. Вначале применение препарата было одобрено с 12 лет, в данный момент этот порог снижен до двух лет. Применение модуляторов CFTR позволяет добиться снижения показателей потового теста до пограничных, а иногда и нормальных значений у множества пациентов.
Применение двухкомпонентной (лумакафтор+ивакафтор) и трехкомпонентной терапии заметно повышает ИМТ, массу тела и рост пациентов; эффект трехкомпонентного препарата более выражен. Улучшается также функция внешнего дыхания вплоть до 20–30% за год (на фоне базисной терапии типично ежегодное снижение на 3–4%). Наблюдаются улучшения и по результатам компьютерной томографии. В отдельных случаях удавалось восстановить функцию внешнего дыхания до нормальных значений с уровня, близкого к необходимости трансплантации. Носовые пазухи очищаются от полипов.
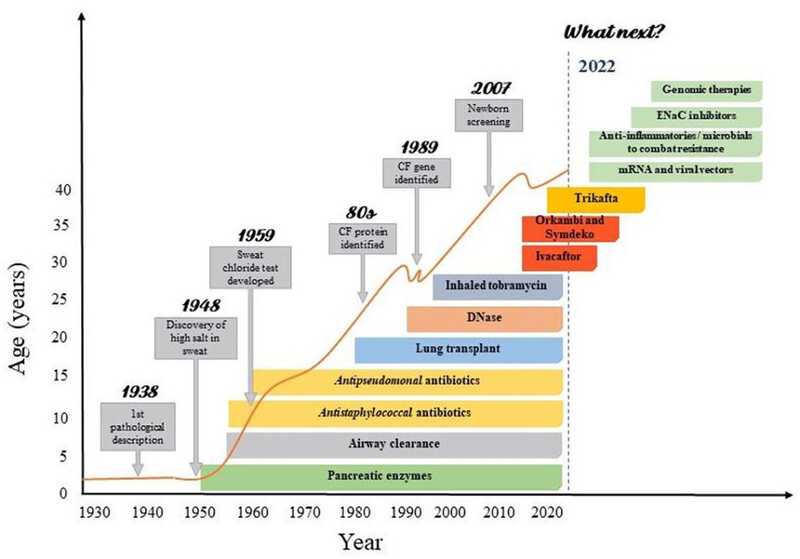
Благодаря современным методам лечения значительно повысилась продолжительность жизни пациентов с муковисцидозом: от нескольких лет в 1940-х годах до более 40 лет в наши дни, а при раннем начале таргетной терапии — и более 80 лет.
Продолжаются исследования новых методов лечения. Например, ингаляционная терапия мРНК CFTR (VX-522, разработанный Vertex Pharmaceuticals совместно с Moderna) эффективна при нарушенном формировании белка независимо от генотипа. В настоящее время проводятся клинические испытания 1-2 фазы.
Тем временем в мире растет доля применения трехкомпонентной таргетной терапии — ее получают уже около 76% пациентов. Таким образом, муковисцидоз из приговора превращается в заболевание, поддающееся лечению и контролю.


 Меню
Меню





 Все темы
Все темы
 Front. Pediatr. DOI:
Front. Pediatr. DOI:




 0
0