Артем Качанов: «Мы живем в эпоху подъема генной терапии»
Новая лекция научно-просветительского проекта «Метафаза» о генной терапии продолжила блок, посвященный разработке лекарств. Артем Качанов рассказал об вошедших в клинику генотерапевтических препаратах, еще не преодоленных трудностях, а также о достижениях своей лаборатории, в которой разработали способы полного удаления вируса гепатита B из инфицированных клеток с помощью комплексной разработки на основе биодеградируемых наночастиц и системы CRISPR-Cas.

Лекция Артема Качанова, научного сотрудника лаборатории генетических технологий в создании лекарственных средств Сеченовского университета, называется «Генетические технологии: лечим неизлечимое».
Генная терапия — любая манипуляция с генами, направленная на лечение заболеваний: это может быть введение, удаление, замена, подавление, изменение или исправление того или иного генетического материала. Такие манипуляции приводят к снижению уровня факторов (белков или РНК), вызывающих заболевание, или их полному удалению, или обеспечивают продукцию нормальных факторов.
Обычно принято считать, что генная терапия призвана лечить наследственные заболевания. Однако с помощью тех же подходов можно разработать лечение инфекционных, аутоиммунных и онкологических болезней.
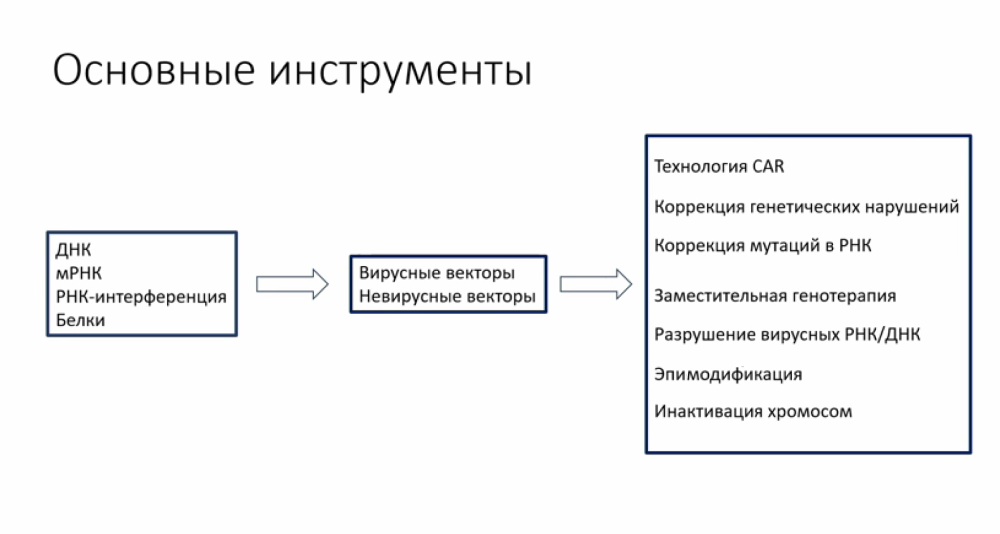
История генной терапии
Многие открытия в биологии были сделаны случайно. Так, например, Александр Флеминг открыл пенициллин, когда заметил, что на забытой чашке Петри с бактериями выросла плесень, способная подавлять их рост. А английский врач Эдвард Дженнер предложил способ вакцинации против натуральной оспы, когда прислушался к рассказам о том, что люди, переболевшие коровьей оспой, не болеют оспой натуральной.
Открытие нуклеиновых кислот также было частично обусловлено случайностью. В 1869 году швейцарский физиолог Фридрих Мишер собирался исследовать функции белков лейкоцитов человека, выделив клетки из гноя пациентов. В экстракте ядер клеток исследователь обнаружил не только белки, но и новое вещество, названное им нуклеином. Теперь известно, что в состав «нуклеина» входила ДНК.
Впоследствии многие ученые внесли свой вклад в понимание функций ДНК и принципов хранения информации в ней: Эдвард Тэйтем предложил концепцию «один ген — один белок» (1941), Освальд Эйвери, Колин Маклеод и Маклин Маккарти доказали, что ДНК отвечает за хранение наследственной информации (1944), Уильям Чаргафф представил принцип комплементарности (1949–1951), а Джеймс Уотсон, Фрэнсис Крик и Розалинд Франклин выяснили, что ДНК имеет форму двойной спирали (1953).
Вскоре после этого появились первые идеи, связанные с генной терапии. В 1961 году американская исследовательница Лоррейн Крауз впервые продемонстрировала, что экзогенную ДНК можно доставить в эукариотические клетки. А в 1966 году Эдвард Тэйтем сформулировал концепцию генной терапии, предложив доставлять гены в клетки человека с помощью вирусов. Нобелевский лауреат считал, что за этим подходом будущее медицины.
Впервые генная терапия была успешно применена в клинической практике в 1990 году. Пациентка, четырехлетняя Ашанти Де Сильва, страдала от тяжелого комбинированного иммунодефицита (SCID), вызванного мутацией в гене аденозиндеаминазы (ADA). Исследовательский проект проводился под руководством Майкла Блейза, Френча Андерсона и Кеннета Калвера в Национальных институтах здравоохранения США. В ходе исследования у пациентки отобрали лейкоциты, модифицировали их, доставив правильную копию гена ADA, и ввели лейкоциты назад в кровь. В результате Ашанти Де Сильва смогла побороть заболевание, при котором дети погибают, не дожив до 10 лет.
Как можно заметить, в ХХ веке началось стремительное развитие молекулярной биологии. На сегодняшний день молекулярная биология все также стремительно развивается и вносит существенный вклад в развитие медицины.
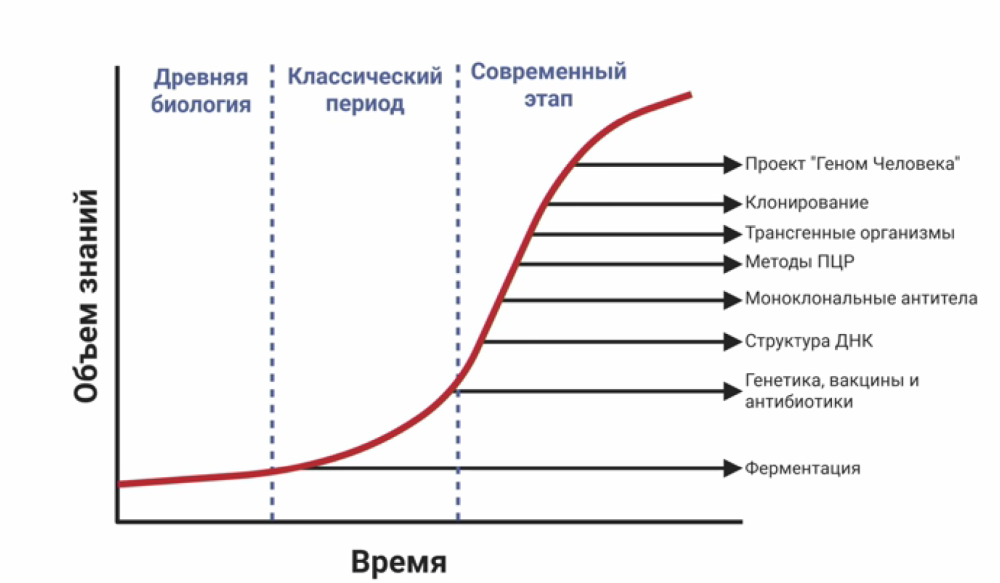
Разработка генной терапии
Как и любое лекарство, генная терапия проходит через множество стадий исследований под постоянным контролем. За разработкой генной терапии — во время этого этапа исследователи проводят эксперименты in vitro на клеточных культурах — следуют доклинические испытания, в которых на животных оценивают токсичность и эффективность препарата. Перспективные препараты попадают в клинические испытания на людях, состоящие из нескольких этапов, в которых оценивается безопасность и эффективность лечения. После выхода препарата на рынок регуляторные службы продолжают отслеживать побочные и нежелательные эффекты препаратов. В случае появления эффектов, которые не были выявлены во время клинических испытаний, разрешение на использование может быть даже отозвано.
Скрининг потенциальных лекарств на основе малых молекул сейчас облегчен благодаря методам компьютерного моделирования. Такой скрининг позволяет «отфильтровать» из нескольких тысяч молекул пару сотен веществ, которые обладают требуемой активностью и могут быть протестированы на животных. Однако до клинических испытаний все равно доходит меньше 5% молекул, проверенных в доклинических исследованиях. Весь этот процесс может занимать от нескольких лет до несколько десятков лет.
В случае с биотехнологическими препаратами все сложнее, поэтому для них предусмотрена система fast-track, позволяющая сократить длительность клинических исследований.
Однако «воронка» все равно остается: после каждой фазы клинических испытаний многие молекулы-кандидаты отсеиваются, и до официального одобрения к медицинскому использованию доходят лишь единицы.
Текущие успехи генной терапии с использованием вирусных векторов
Спинальная мышечная атрофия (СМА) — это наследственное заболевание, для которого характерна прогрессирующая мышечная слабость и которое вызывается мутацией в гене SMN1, важном для нормальной работы моторных нейронов. Заболевание встречается в среднем у 1 на 6–10 тысяч людей. Из-за деградации моторных нейронов люди теряют контроль над мышцами; в критических случаях может требоваться искусственная вентиляция легких.
Компания Novartis вывела на рынок препарат Золгенсма, представляющий собой ДНК-конструкт с правильной последовательностью гена, помещенный в аденоассоцииированный вирус 9 серотипа (ААВ9). При этом ААВ модифицирован таким образом, что в нем практически не осталось вирусных генов. При попадании в организм вирус проникает в целевые клетки, переходит в их ядра и доставляет туда генетический конструкт, что приводит к экспрессии в клетках верной копии гена. Золгенсма — весьма эффективный препарат: если его ввести ребенку в первые месяцы жизни, то он будет полноценно развиваться. Предполагается, что результат терапии пожизненный: одного укола хватает на всю жизнь.
Подобный подход был применен и для лечения миодистрофии Дюшенна. Это заболевание также характеризуется мышечной слабостью, нарушениями движения, прогрессирующей кардиомиопатией и встречается у 1 на 3500-4000 людей. Причина заболевания — мутации в гене дистрофина, считающегося одним из крупнейших белков человека. Компания Sarepta Therapeutics разработала препарат Элевидис: ААВ, несущий укороченную копию гена дистрофина под тканеспецифичным промотором, благодаря чему этот ген будет экспрессироваться только в скелетных мышцах.
Еще один генотерапевтический препарат был разработан для лечения амавроза Лебера — болезни, приводящей к гибели светочувствительных клеток глаза, дистрофии сетчатки, ослаблению или полной потере зрения. Это заболевание вызвано мутациями в гене RPE65, который кодирует фермент клеток сетчатки глаза, обеспечивающий наличие светочувствительного пигмента. Амавроз Лебера встречается гораздо реже: у 1 на 81 000 человек. Для лечения этой болезни компания Spark Therapeutics. предложила препарат Лукстурна. Это ААВ 2 серотипа, несущий правильную копию гена RPE65. Препарат доставляется путем инъекции непосредственно в глаз..
Проблема представленного выше подхода состоит в том, что при использовании ААВ доставленный генетический конструкт находится вне генома в форме эписомы. Из-за этого конструкт не передается в дочерние клетки при делении. В случае быстро делящихся клеток — например, клеток эпителия кожи — доставленный с помощью ААВ трансген в какой-то момент оказывается утерянным.
Наиболее ярко этот недостаток демонстрируется на примере генной терапии буллезного эпидермолиза — болезни, при которой образуются пузыри и эрозии на коже и слизистых оболочках, и они становятся гиперчувствительными к травмам и инфекциям. Это заболевание вызывается мутациями в разных генах, в том числе в COL7A1, KRT5 и др. Оно очень редкое и встречается с частотой от 1:30000 до 1:1000000. Препарат Виджувек, разработанный компанией Krystal Biotech, доставляет ген COL7A1 с помощью вируса простого герпеса HSV-1, чей трансген также находится в ядре в эписомальной форме. Так как трансген доставляется в клетки кожи, препарат требуется топически наносить раз в две недели.
Сложные случаи генной терапии
Еще один удобный инструмент для генной терапии — редакторы оснований. Эти белки часто представляют собой модификации белков системы CRISPR-Cas, которые не обладают нуклеазной активностью, но позволяют заменить одно азотистое основание в цепи ДНК на другое.Редакторы оснований удобны в случаях, когда нецелесообразно заменять весь ген новой копией, так как дефект в нем вызван точечной мутацией.
Кроме того, существуют подходы, позволяющие лечить хромосомные заболевания. Классический пример такой болезни — синдром Дауна, вызванный трипликацией хромосомы 21. В фибробласты пациента можно доставлять ген XIST1, функция которого в норме — инактивация второй Х-хромосомы у женщин. Аналогичным образом, его доставка с интеграцией в дополнительную хромосому 21 приводит к ее инактивации.
Особой сложностью отличается терапия митохондриальных заболеваний: например, синдрома Кернса—Сейра, синдрома MELAS, синдрома MERRF. При митохондриальных болезнях больше всего страдают те органы и ткани, которые активнее всего потребляют энергию: мозг, сердце, мышцы. Генная терапия митохондриальных болезней труднее, поскольку большинство вирусов не способны проходить через двойную мембрану этих органелл, чтобы отредактировать митохондриальную ДНК. Наиболее простой подход — это внутриядерная экспрессия генов, однако этот способ подходит только для белков, которые митохондрия способна импортировать.
Подход на основе такой аллотопной экспрессии митохондриальных белков был разработан для лечения наследственной нейропатии зрительного нерва Лебера, которая вызывается мутациями в генах митохондриальной NADH-дегидрогеназы. Для доставки генов субъединиц этого фермента в ядро уже применялись интраокулярная электропорация и ААВ2.
Как вылечить гепатит B генной терапией?
В лаборатории, сотрудником которой является Артем Качанов, особое внимание уделяется генной терапии инфекционных заболеваний, а именно хронического гепатита B. В мире до 250 млн людей хронически инфицированы вирусом гепатита B, что приводит к хроническому заболеванию печени. До миллиона человек в год погибает от последствий этой инфекции — цирроза и рака печени.
На данный момент основные методы лечения вирусного гепатита B направлены на остановку вирусного цикла: так, применяются аналоги нуклеозидов и нуклеотидов, ингибиторы входа вируса в клетку. Однако такая терапия не может полностью излечить пациента. Кольцевая частично двухцепочечная ДНК (кчдДНК) вируса проникает в ядро клетки и трансформируется в кольцевую ковалентно замкнутую молекулу (ккзДНК), которая продолжает существовать в ядре в виде минихромосомы. Это обеспечивает персистентность инфекции: как только терапия прекращается, вирус снова может начать репликацию с этой кольцевой ДНК.
Для борьбы с этим исследователи решили использовать терапию на основе CRISPR-Cas — «молекулярных ножниц», способных разрезать нуклеиновые кислоты в специфическом сайте. На сегодняшний день, всего через 10 лет после адаптации CRISPR-Cas для генного редактирования, одобрен генотерапевтический препарат на основе CRISPR-Cas — Casgevy. Он применяется для лечения серповидноклеточной анемии ex vivo, т.е. клетки пациента выделяют из организма, а после модификации вводят назад. Генотерапевтические препараты на основе CRISPR-Cas сейчас проходят клинические испытания; это препараты для лечения талассемии, гемофилии, транстиретинового амилоидоза, онкопатологий и т.д.
Еще в 2014 году было показано, что CRISPR-Cas можно использовать для прицельного разрушения генома вируса гепатита B. Если в клетки, экспрессирующие белок Cas9, доставить направляющую РНК к ДНК гепатита B, то можно наблюдать снижение уровня вирусной ДНК. Однако после этого пилотного эксперимента осталось несколько нерешенных вопросов.
Например, что происходит с геномом вируса после разрезания, и не может ли он продолжать функционировать как источник вирусных белков? Обычно разрезание нуклеиновых кислот белком Cas9 приводит к репарации ДНК по пути негомологичного соединения концов (NHEJ), из-за чего в месте разрезания появляются инсерции или делеции, вызывающие сдвиг рамки считывания. Коллеги Артема Качанова показали, что в случае с вирусной ДНК гепатита B после обработки CRISPR-Cas наблюдается снижение уровня ккзДНК, а в сохранившихся копиях повышается количество инсерций и других полиморфизмов, однако количество наблюдаемых мутаций относительно невелико. В то же время применение CRISPR-Cas в присутствии ингибиторов негомологичного соединения концов не приводило к снижению уровня ккзДНК, однако относительное количество мутаций в целевой области возрастало. В совокупности это свидетельствует о том, что основным исходом при действии CRISPR-Cas на ДНК вируса гепатита В является разрушение вирусного генома.
Другая проблема CRISPR-Cas — возможное нецелевое действие. Как и в любой терапии, необходимо направленно воздействовать именно на геном вируса, не затрагивая геном человека. Вирус гепатита B частично интегрируется в геном человека, в этом случае система CRISPR/Cas может разрезать и геном пациента.
Действительно, согласно экспериментальным данным, традиционный Cas9 неспецифически разрезает и геном человека, а не только вирусный геном. Устранить эту проблему удалось за счет использования белка StCas9 — вариации Cas9, выделенной из бактерии Streptococcus thermophilus. За счет того, что узнаваемая этим белком PAM-последовательность в целевой ДНК крупнее, чем у классического Cas9, StCas9 с меньшей вероятностью разрезает ДНК человека, «выбирая» в качестве мишени преимущественно вирус.
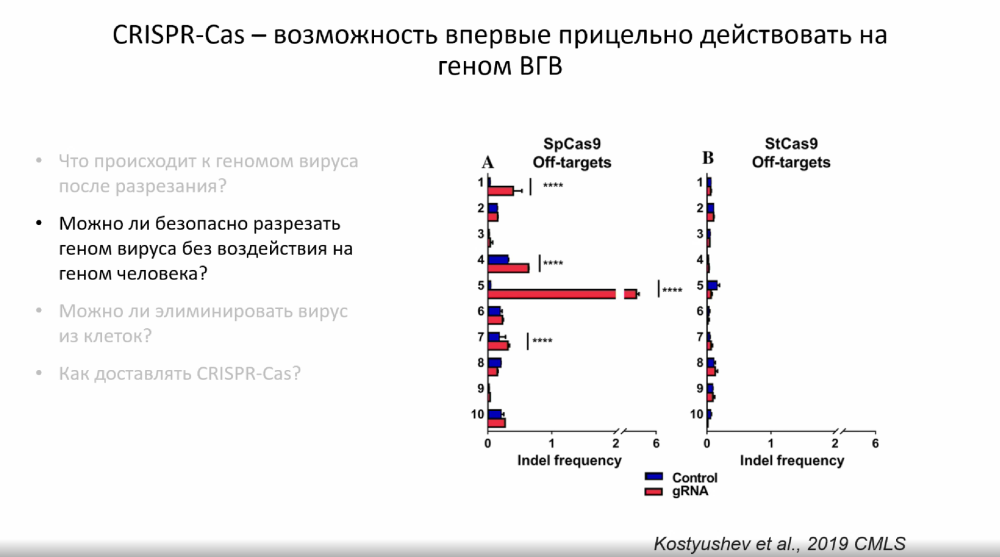
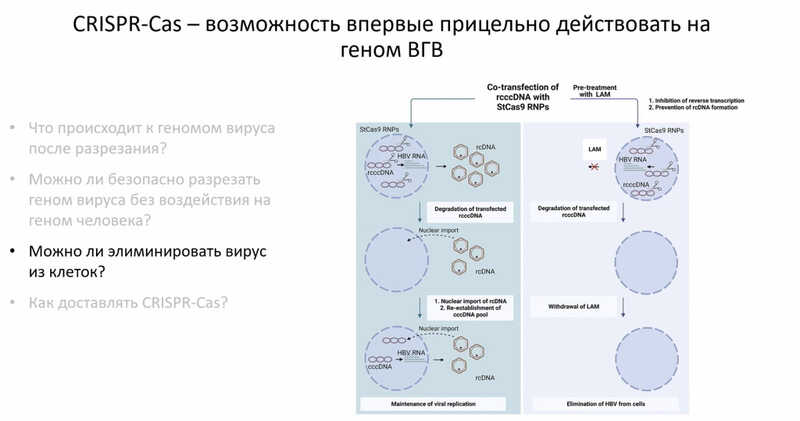
Однако применение CRISPR-Cas не приводит к полной элиминации вируса. Несмотря на то, что кольцевая вирусная ДНК разрушается, спустя какое-то время инфекция реактивируется. Это связано с тем, что одновременно в клетке могут содержаться вирусные капсиды, все еще несущие геном вируса гепатита B в форме кольцевой частично двухцепочечной ДНК (кчдДНК). В результате вирус вновь проникает в ядро и начинает размножаться. Предотвратить это можно, совместив CRISPR-Cas с традиционными ингибиторами клеточного цикла вируса: так, совместное действие StCas9 и ламивудина — нуклеозидного ингибитора обратной транскриптазы — позволило не только полностью удалить ккзДНК из клеток, но и предотвратить последующую реактивацию инфекции.
Отдельный вопрос при использовании CRISPR-Cas — доставка инструмента в клетки. Непосредственно белок человеку ввести нельзя, так как он бактериального происхождения и сразу будет распознан иммунитетом как чужеродный. Часто Cas доставляют в виде ДНК, с которой транскрибируется РНК и затем с нее синтезируется белок. Но и этот способ доставки плох во всех смыслах, так как в данном случае белок будет экспрессироваться на очень высоком уровне длительное время, что резко повышает шансы токсического и внецелевого действия, а также разрушения клеток человека иммунной системой из-за наличия презентированных компонентов бактериального белка Cas9.
Коллеги Артема Качанова рассмотрели альтернативный вариант, а именно — доставку непосредственно белка Cas9 при помощи биодеградируемых наночастиц, напоминающих экзосомы. На их поверхности расположены различные лиганды, позволяющие им скрыться от иммунного ответа. Поверхность наночастиц также можно модифицировать различными белками, чтобы обеспечить целевую доставку в конкретные органы. Кроме того, белок Cas9 полностью элиминируется из клеток за считанные дни, что делает такой подход значительно более безопасным, чем доставка трансгена.
В такие частицы успешно загрузили и белок Cas, и направляющую РНК. Эффективность их доставки в клетки in vitro составила около 99%. Через два дня после введения таких наночастиц в клеточную культуру уровень вирусной кольцевой ДНК в клетках значительно снизился, что доказало противовирусную активность частиц. Протестировать наночастицы удалось и на мышиной модели инфекции: после однократного их введения уровень вирусных антигенов уже на третий день снизился на 99% и оставался на том же низком уровне в течение последующего месяца наблюдений.



 Меню
Меню





 Все темы
Все темы




 0
0











