Павел Вандышев: «Производство вакцин от гриппа — как игра в биатлон»
В новой лекции научно-популярного проекта «Метафаза» о разработке лекарств Павел Вандышев рассказал о производстве вакцин и объяснил, как оптимизация процесса еще на стадии зарождения куриных эмбрионов, использующихся для наработки частиц вируса гриппа, может помочь достичь коллективного иммунитета к гриппу.

Павел Вандышев, и.о. заведующего кафедрой технологии химико-фармацевтических и косметических средств, зам. директора НИЦЭМ им. Н.Ф. Гамалеи, выступил с лекцией «Современные подходы к обеспечению иммунобиологической безопасности».
Иммунопрофилактика в России
Инфекционные заболевания остаются одной из самых распространенных причин смертности в мире, вне зависимости от уровня дохода населения. Но при этом в странах с низким уровнем дохода 8 из 10 основных причин смертей связаны с инфекциями, в странах со средним уровнем дохода инфекции — половина, а в странах с высоким уровнем дохода в топ-10 причин смертности входят только инфекции нижних дыхательных путей. Следует также отметить, что одной из важных причин смертности остаются хронические заболевания, в том числе диабет и сердечно-сосудистые болезни, которые служат дополнительным фактором риска летального исхода от инфекций.
В России выделяют около 34 основных инфекционных заболеваний, в том числе COVID-19. Эти инфекции наносят значительный экономический ущерб стране: в 2022 году он составил 2,5 трлн руб., в 2023 году — 1,5 трлн руб. В России принят федеральный закон N 157-ФЗ «Об иммунопрофилактике инфекционных болезней», согласно которому государство ответственно за финансовую поддержку и реализацию программ вакцинации. Для граждан же зафиксированы обязанности и права на получение профилактических прививок.
Вакцинация — самый эффективный метод профилактики инфекционных заболеваний. В России реализован Национальный календарь прививок, включающий вакцины от полиомиелита, туберкулеза, столбняка, вирусного гепатита B и ряда других инфекций. В некоторых регионах выполняются особые предписания по профилактике, связанные с эпидемиологической ситуацией, ведь в них могут быть актуальны и другие инфекции, например, клещевой энцефалит.
Несмотря на эти усилия по профилактике инфекций, в России не хватает вакцин от ротавируса, ветряной оспы, вируса папилломы человека (ВПЧ) и менингококка. В ряде случаев это связано с отсутствием производств таких вакцин. Однако ситуация постепенно меняется. Так, в НИЦЭМ им. Н.Ф. Гамалеи уже проводятся клинические испытания 3 фазы вакцины против ротавирусной инфекции «Гам-VLP-рота» на основе вирусоподобных частиц. Летом 2025 года компания «Нанолек» завершила клинические испытания 3 фазы вакцины против ВПЧ «Цегардекс» с участием детей от 9 лет; расширение показаний на данную возрастную группу намечено на февраль 2026 года. Ожидается, что в будущем году она может быть включена в нацкалендарь прививок. А Санкт-Петербургский НИИ вакцин и сывороток ФМБА осенью этого года получил разрешение на проведение 2 и 3 фазы клинических испытаний вакцины от менингококка «MCV-5».
H1N1, H3N2, B/Ямагата и В/Виктория
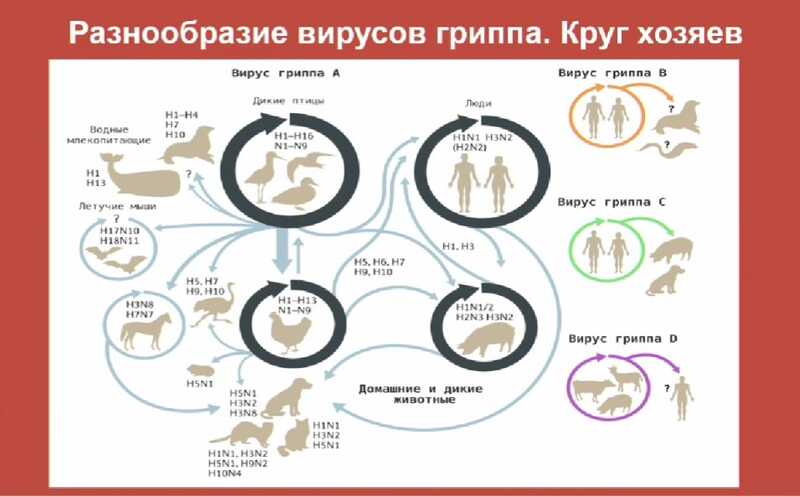
Грипп — это острая вирусная инфекция, которая передается воздушно-капельным путем. Для нее характерны сезонность (зима-весна) и высокая восприимчивость всех возрастных групп. Возбудителями инфекции являются вирусы гриппа, относящиеся к четырем типам (A, B, C, D); штаммы типов A и B вызывают сезонные эпидемии и пандемии. В случае вируса гриппа А природный резервуар поддерживается птицами водного и околоводного пространства. Для человека наиболее актуальными являются вирусы гриппа А (H1N1, H3N2) и группы B — линии Виктория и Ямагата. (С последним ситуация после окончания пандемии COVID-19 неясная. — PCR.NEWS.)
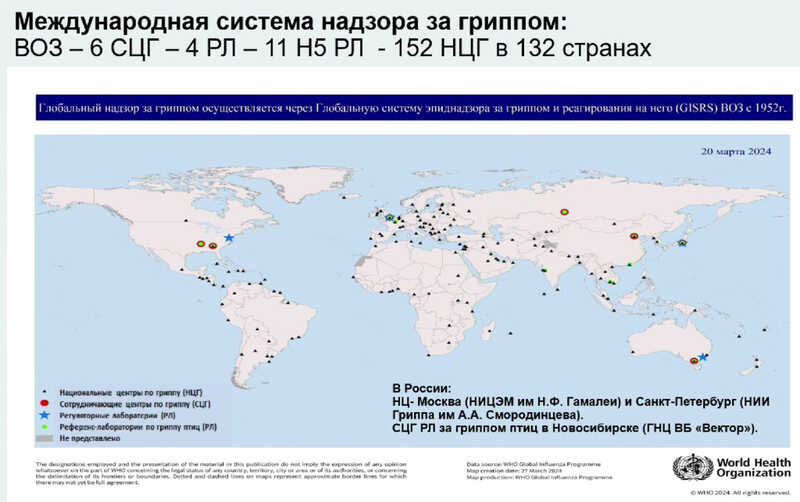
С середины прошлого века была организована международная система надзора за гриппом. По всему миру научно-исследовательские центры изучают распространение вируса гриппа и вспышки этой инфекции. Два раза в год — в сентябре и феврале — ВОЗ собирает экспертов, чтобы определить штаммовый состава для южного и северного полушария. При этом особое внимание уделяется не тем штаммам, которые широко представлены в популяции. Напротив, считается, что к ним уже формируется коллективный иммунитет, поэтому нет смысла вакцинировать население от них. Для иммунного надзора выбирают те штаммы вируса, которые резко расширяют ареал распространения.
Мониторинг эффективности вакцин
Профилактическая эффективность вакцин определяется на основе клинических испытаний, иммунологических показателей (например, защитного титра антител). Если вакцина длительное время массово используется, проводится мониторинг изменения эпидемиологических показателей.
На эффективность вакцин могут влиять тип вакцины, дозировка, интервалы введения, тип антигена, а также индивидуальные генетические особенности организма. От некоторых инфекций, таких как оспа, полиомиелит, столбняк, человек может получить длительный иммунитет, а в случае с другими заболеваниями (например, чума, грипп, холера) иммунитет оказывается непродолжительным. Упомянув об индивидуальных особенностях организма, докладчик отметил, в НИЦЭМ им. Н.Ф. Гамалеи совместно с Институтом им. Герцена активно ведутся работы над персонализированными онковакцинами: иммунный ответ можно направить с помощью вакцин не только против патогенного микроорганизма, но и против клеток опухоли. (Подробнее об онковакцинах на PCR.NEWS.)
Путь от куриного эмбриона до коллективного иммунитета
Первые вакцины от гриппа А появились во второй половине 1930-х годов. В 1936 г. в США была разработана инактивированная вакцина от гриппа, в Советском Союзе в 1937 г. под руководством Анатолия Александровича Смородинцева была произведена живая гриппозная вакцина (ЖГВ). Она содержала живой, но ослабленный вирус и формировала иммунитет против вируса гриппа типа А. Живая гриппозная вакцина широко применялась в СССР, более 100 миллионов взрослых и детей были привиты этой вакциной. В настоящее время ЖГВ на отечественных штаммах «Ленинград» включена в глобальный план ВОЗ по борьбе с пандемическим гриппом.
Живые вакцины имитируют естественную инфекцию, быстро вызывают иммунитет, но для их производства необходимы специальные дорогостоящие эмбрионы от куриц, которые содержатся в сверхчистых условиях.
Развитию вакцин от гриппа поспособствовало появление двух технологий. Во-первых, исследователи стали применятьреассортацию вирусов. Вирусы дикого типа медленно растут в лабораторных условиях. Тогда проводят смешение (рекомбинацию) генетического материала вируса дикого типа с непатогенным вирусом-донором, способным быстро размножаться в лаборатории. Новый вирус гриппа — вакцинный реассортант — состоит из внутренних белков донора и иммуногенных антигенов дикого вируса. Рессортант используется для производства вакцины в больших количествах.
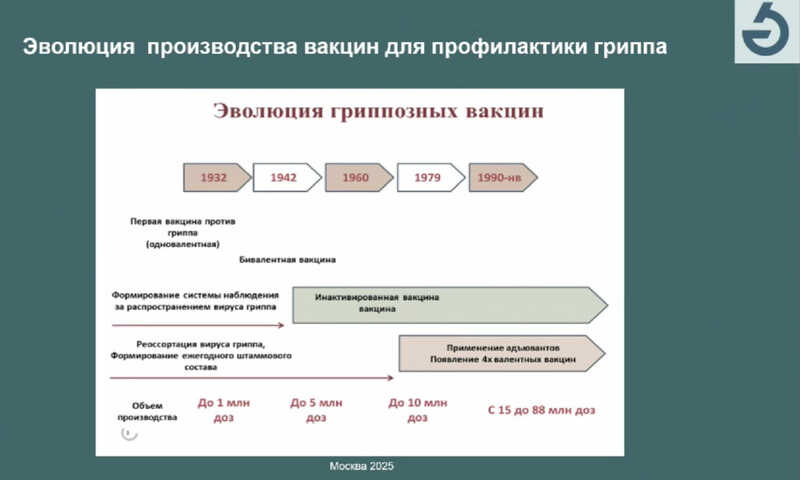
Во-вторых, начали применять инактивированные вакцины — они содержат убитые вирусы, но иммунный ответ у человека на белки-антигены инактивированного вируса все равно возникает. Эти два подхода способствовали росту производства вакцин: в России его объем к 2019 году достигал около 90 млн доз.
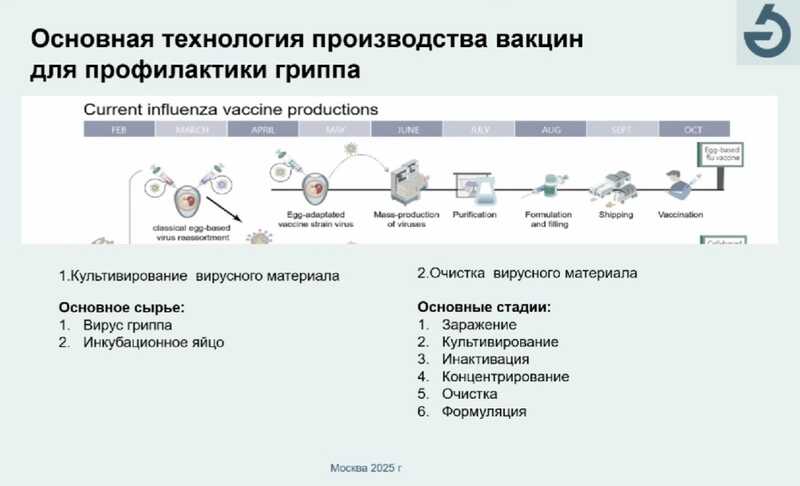
Самым распространенным подходом к получению вакцин остается метод с использованием куриных эмбрионов. Эмбрион в курином инкубационном яйце заражают вирусом, и происходит наработка вирусной массы. После инактивации, концентрирования и очистки получают чистый антиген, который включают в состав вакцины. Этот метод отличается дешевизной и позволяет получать как моно-, так - и трех- или четырехвалентные вакцины, содержащие антигены различных штаммов.
В мире всего 60 компаний занимаются разработкой вакцин от гриппа, и ежегодно они производят 40 кг вирусного гемагглютинина, причем стоимость одного грамма — около 5 млн руб.
В России производство вакцин начинается в декабре, однако производители рискуют, ведь на этот момент актуальный штаммовый состав следующего сезона еще неизвестен. В феврале заводы начинают функционировать в полную мощность, а к маю появляются первые серии препарата. Поскольку каждый год штаммовый состав меняется, то и вакцина каждый год получается новая — следовательно, нужно всегда заново доказывать эффективность вакцины от гриппа. Для этого ежегодно проводятся клинические испытания безопасности вакцины на 60–100 добровольцах. В конце лета производители могут получить заключение по итогу клинических исследований, и тогда новая вакцина может массово выйти на рынок. Сезон вакцинации от гриппа обычно длится всю осень, причем Минздрав старается обеспечить вакциной все регионы страны. Павел Вандышев сравнил работу производителей вакцины с биатлоном — им нужно точно поразить несколько целей: разработать и получить вакцины с учетом штаммового состава и успеть доставить их в регионы.
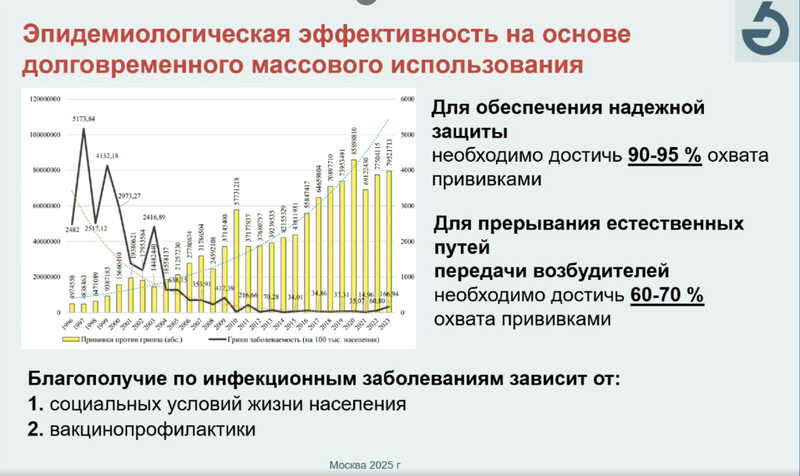
Основная задача вакцинации — формирование коллективного иммунитета. Для обеспечения надежной защиты необходимо достичь 90–95% охвата прививками, а для прерывания естественных путей передачи возбудителей достаточно 60–70% охвата. В 2023 году в России удалось охватить прививками около 79 млн человек, при этом заболеваемость гриппом составила лишь 167 человек на 100 тыс. населения.
Стандартизация куриных эмбрионов
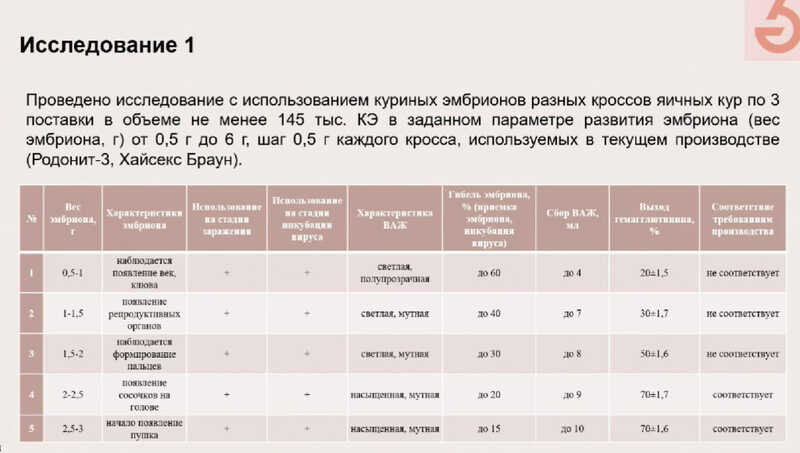
Павел Вандышев рассказал о собственных исследованиях. Одно из них посвящено изучению факторов, которые влияют на эффективность использования куриных эмбрионов для культивирования вирусов гриппа при производстве противогриппозных вакцин. Это исследование было начато еще в 2016 году.
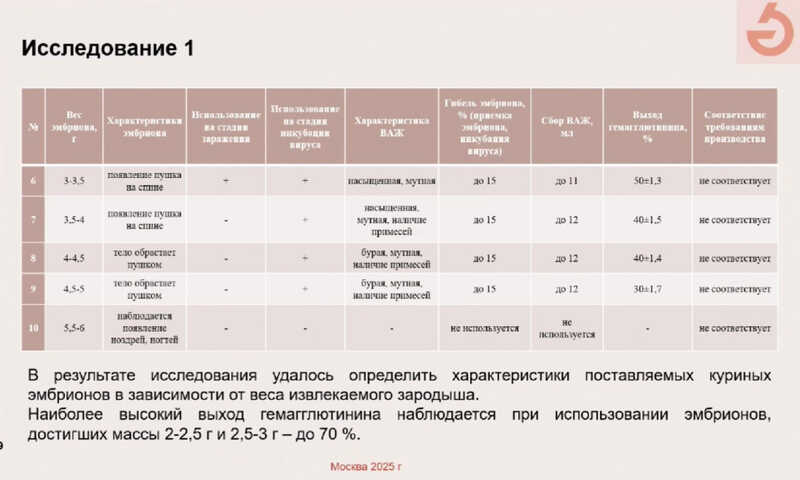
Для начала ученые определили стандартизированные параметры, соблюдение которых позволяет повысить выход гемагглютинина. Исследовали эмбрионы двух кроссов куриц (Родонит-3 и Хайсекс Браун) с различным весом. При весе эмбриона до 2 г наблюдалась высокая смертность эмбрионов и низкий выход гемагглютинина, а оптимальные параметры достигались при весе эмбрионов 2–3 г. При более высоком весе повышалось количество дебриса, который затрудняет процесс очистки.
Классический метод очистки вируссодержащей аллантоисной жидкости, который появился в 1940–1950-х годах, основан на сорбции и элюции гемагглютинина на куриных эритроцитах. Этот метод технологически прост, но требует высокой квалификации персонала и дополнительного сырья — собственно эритроцитов. Кроме того, он низкопроизводителен. Тем не менее в России его продолжали применять в 2000–2010-х годах, что не позволяло нарастить масштабы производства вакцины.
Затем метод очистки антигена сменился на тупиковую фильтрацию на патронных фильтрах. Для него требуется довольно простая аппаратура, но риск контаминации продукции высокий. Из-за этого фильтры нужно было термически стерилизовать ежедневно заменять. Ппроизводительность метода все равно оставалась низкой: большое количество целевого продукта осаждалось на мембране, что снижало выход.
Наконец, на производстве стали внедрять фильтрацию в тангенциальном потоке. Этот метод требует дорогостоящего оборудования, однако очистка производится автоматически в закрытой системе, что обеспечивает высокую степень очистки и производительность.
Определение оптимальных параметров куриных эмбрионов и внедрение фильтрации в тангенциальном потоке позволило более чем на 20% увеличить выход вируссодержащей жидкости. Эта модификация методики легла в основу производства четырехвалентной вакцина «Ультрикс Квадри».
На следующем этапе исследователи оценили, как кросс кур влияет на объем извлекаемой вируссодержащей жидкости. Лучшие показатели из года в год демонстрировал кросс Родонит-3.
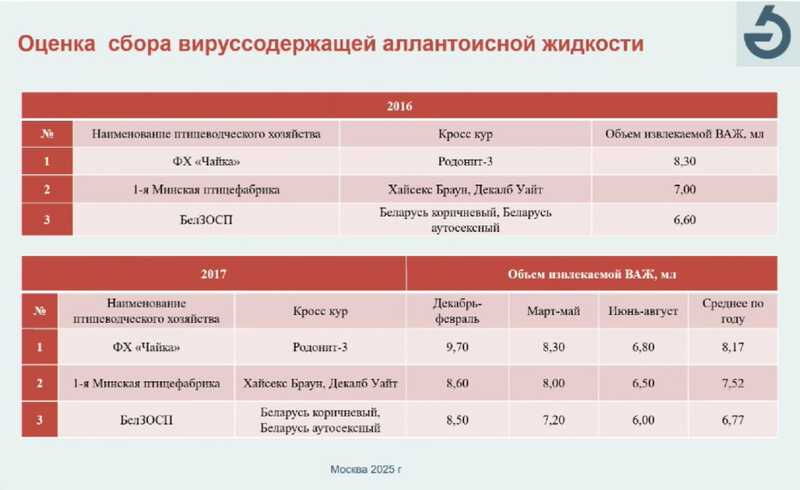
Исследователи также оценили технологические потери куриных эмбрионов на разных стадиях при производстве вакцин. Для кросса Родонит-3 они также были минимальны: ежегодно с 2016 по 2019 г. объем потерь не превышал 10%.
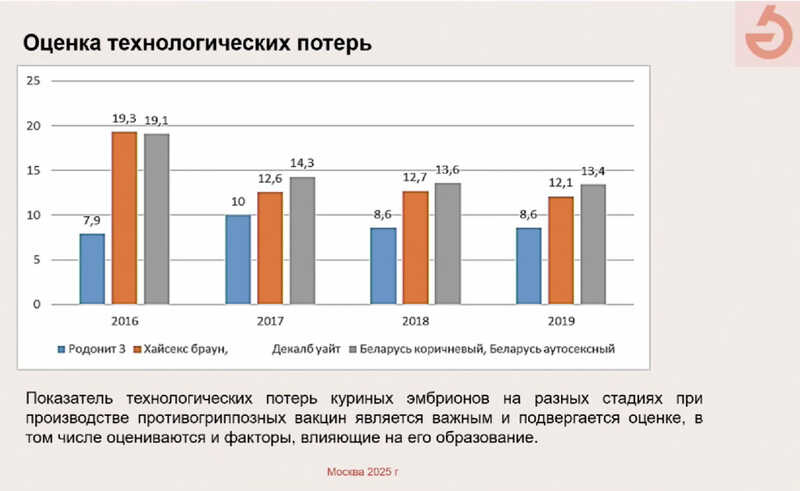
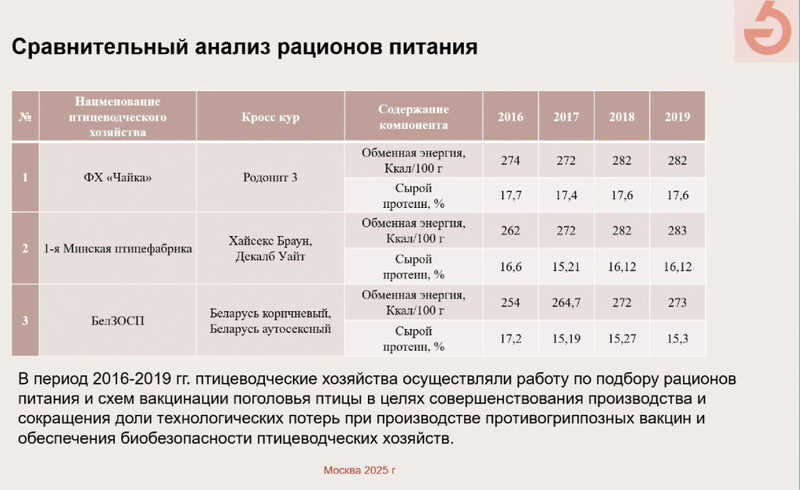
Чтобы понять, чем могут быть вызваны такие различия, ученые проанализировали рационы питания птиц. Для кросса Родонит-3 обменная энергия рациона составляла около 280 ккал/100 г, а содержание белка было около 17,5%. Обмен опытом с разными птицефабриками привел к улучшению показателей и для других кроссов: например, изменение рациона для кроссов Беларусь коричневый и Беларусь аутосексный позволило несколько снизить объем технологических потерь.
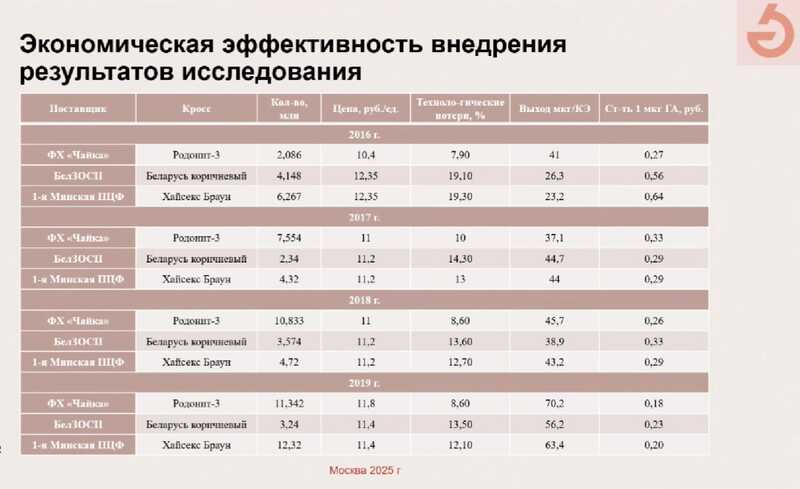
Стандартизация куриных эмбрионов позволила улучшить производственный процесс с экономической точки зрения. Если в 2016 году стоимость 1 мкг гемагглютинина составляла 30 копеек при работе с эмбрионами кросса Родонит-3, то к 2019 году она снизилась до 18 копеек. Стоимость уменьшилась и для других кроссов: так, в 2016 году при применении Хайсекс Браун 1 мкг гемагглютинина стоил 64 копейки, а в 2019 году, после внедрения результатов исследования — всего 20 копеек.
Внедрение улучшенного метода очистки гемагглютинина также повысило его выход. В мире оптимальным количеством гемагглютинина с одного яйца считается 35 мкг, но фильтрация в тангенциальном потоке позволила достигнуть отметки 70 мкг. После этого в России производство гемагглютинина составляло 2 кг в год, то есть 5% от мировых объемов гемагглютинина. Появилась возможность производить четырехвалентную вакцину, не содержащую адъювантов и содержащую 15 мкг каждого штамма, то есть с одного яйца можно было производить одну вакцину. В случае с адъювантными вакцинами, содержащими всего 22 мкг белка, с одного яйца можно получать около трех доз.
В заключение Павел Вандышев отметил, что хотя эмбриональный метод и позволил получать вакцины от гриппа в достаточных количествах, он достиг пика возможностей. С существующей производительностью трудно выполнить требование Роспотребнадзора — начинать вакцинацию во всех регионах 1 сентября. Поэтому на смену эмбриональному методу должны прийти другие. Так, нарабатывать вирусные частицы можно в культурах клеток. Можно также перейти к высокопроизводительной технологии мРНК-вакцин, которые вызывают выработку антигена в самих клетках организма, а кроме того, дешевы и могут быть разработаны быстро. Но пока что нас защищают от гриппа куриные эмбрионы.



 Меню
Меню





 Все темы
Все темы




 0
0











