Вадим Покровский: «В фармакологии биотех будет вытеснять химию»
Новый блок научно-популярного проекта «Метафаза», посвященный разработке лекарств, открыл Вадим Покровский с лекцией о противоопухолевых препаратах. Он рассказал об истории развития препаратов от химического оружия до таргетной и иммунотерапии, о трендах, а также о том, почему так сложно найти лекарство от рака.

Вадим Покровский (д.м.н., профессор, заведующий кафедрой биохимии им. Т.Т. Березова медицинского института РУДН, заведующий лабораторией биохимических основ фармакологии и опухолевых моделей НМИЦ онкологии им. Н.Н. Блохина) выступил с лекцией «Разработка противоопухолевых препаратов: основные этапы и тренды».
Онкологические заболевания занимают второе место среди причин смерти во всем мире и в развитых странах, уступая только сердечно-сосудистым заболеваниям, и третье — в развивающихся странах. В России злокачественные заболевания встречаются у более чем 2500 человек на 100 тыс. населения.
Сфера разработки противоопухолевых препаратов стремительно развивается. Так, по данным за 2018–2021 гг., около трети всех биотехнологических компаний в США, которые занимаются разработкой лекарственных препаратов, заняты в сфере онкологии или имеют флагманские противоопухолевые продукты.
Первые противоопухолевые препараты
История противораковой химиотерапии началась еще в военное время в XX веке. «Вдохновением» для первых препаратов стали вещества, используемые в качестве химического оружия. Например, оказалось, что у людей, пораженных ипритом (ядом кожно-нарывного действия), наблюдается длительная лейкопения, то есть это вещество угнетает кроветворение. Именно из-за этого иприт стал интересен с точки зрения лечения лейкозов. Однако молекулу «обезопасили»: атом серы в иприте заменили на атом азота. В 1942 г. Луис Гудман и Альфред Гилман — ученые из Йельского университета, исследовавшие азотистые аналоги иприта, — впервые протестировали азотистый иприт для лечения лимфогранулематоза у пациента. После курса химиотерапии пораженные лимфоузлы у него уменьшились в размере.
После этого открытия химики по всему миру задались вопросом о том, как же сделать азотистый иприт менее токсичным для здоровых тканей, сохранив эффективность его действия против опухолей. Преследуя эти цели, химики синтезировали ряд производных азотистого иприта — хлорэтиламины: к их числу относятся сарколизин (мелфалан) и циклофосфамид, синтезированные в 1950-х годах. В СССР в этот период школа химиотерапии была основана Леонидом Федоровичем Ларионовым, под руководством которого велась разработка химиотерапевтических препаратов.
Тогда же, в 1950-е гг., были получены первые иммортализованные культуры опухолевых клеток. При культивировании таких клеток в питательные среды включают добавки, необходимые для роста клеток, обычно сыворотки крови животных. Сейчас в основном используются бычья или лошадиная сыворотки, но в прошлом исследовались сыворотки и других животных, включая свиней, собак и даже морских свинок. В 1953 г. американский патолог Джон Кидд описал, что сыворотка крови морских свинок способна угнетать рост опухолевых клеток. А в 1961 г. другой патолог — Дж. Брум — выяснил, что в сыворотке крови морских свинок содержится фермент аспарагиназа, причем у других животных этого фермента нет. Аспарагиназа способна разрушать аспарагин, таким образом лишая опухолевых клеток аминокислоты, которая необходима для синтеза белков. В 1973 г. рекомбинантная аспарагиназа, полученная из E. coli, была зарегистрирована как противоопухолевый препарат. Этот фермент и до сих пор используется для лечения лейкозов и некоторых лимфом.
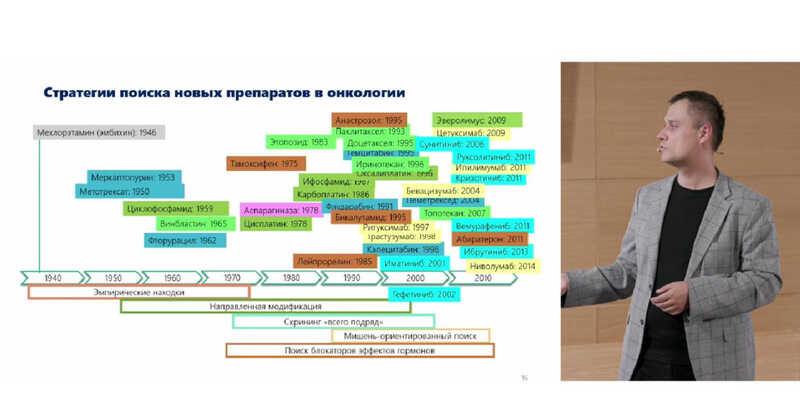
Многие химиотерапевтические препараты были открыты при скрининге растительных экстрактов. В 1960-х гг. из разновидности барвинка (Catharanthus roseus) были выделены винбластин и винкристин — ингибиторы полимеризации микротрубочек. В тот же период были открыты этопозид и тенипозид — ингибиторы топоизомеразы II, обнаруженные в экстрактах подофилла щитовидного (Podophyllum peltatum). В 1980-е гг. также получили таксаны, такие как паклитаксел и доцетаксел: эти вещества, выделенные из клеток тиса, препятствуют делению клеток, так как стабилизируют микротрубочки в веретене деления. Тогда же из камптотеки остроконечной (Camptotheca acuminata) изолировали иринотекан и топотекан — ингибиторы топоизомеразы I. Некоторые из этих препаратов до сих пор используются при лечении рака молочной железы, рака легких, опухолей центральной нервной системы и т.д.
Таким образом, первые противоопухолевые препараты в основном появлялись в результате неожиданных эмпирических находок или при скрининге «всего подряд». В некоторых случаях молекулы направленно модифицировали, пытаясь присоединить к ним функциональные группы, отвечающие за токсичность, либо, наоборот, пытаясь снизить токсичность препаратов к здоровым тканям. Благодаря открытию генов и кодируемых ими белков, а также определению функции таких белков, стало возможным подбирать лиганды с учетом знания мишеней — компонентов сигнальных путей, которые аномально функционируют в опухолях.
Кризис в разработке препаратов
Благодаря прорывам в фармакологии в прошлом удавалось несколько раз значительно повысить ожидаемую продолжительность жизни населения: благодаря разработке средств для наркоза, открытию антибиотиков и введению обязательной вакцинации. Однако в последние годы рост ожидаемой продолжительности жизни замедлился: нет таких прорывов, которые могли бы значимо ее повысить.
Одна из проблем в разработке противоопухолевых препаратов — так называемый кризис интеллектуальной собственности. Фармакологические компании преследуют выгоду, однако разработка далеко не всегда может стать коммерчески выгодной. Из-за этого многие препараты, даже эффективные, не дойдут до пациентов.
Раньше противоопухолевые препараты разрабатывались с целью просто убить опухолевые клетки, поэтому пациентам назначались токсичные препараты в высоких дозировках. Это приводило к большому количеству побочных эффектов. Сейчас подход к разработке противоопухолевой терапии изменился: ученые не пытаются искать простые решения, что тоже усложняет сам процесс разработки.
Кроме того, даже если удается разработать принципиально новые молекулы, они все равно не идеальны. Так, молекула может эффективно подавлять рост опухолей, но в то же время плохо растворяться или иметь неблагоприятный фармакодинамический или фармакокинетический профиль. Все эти проблемы нужно дополнительно решать с помощью модификаций молекул, что не всегда возможно и влечет дополнительные затраты на разработку.
Биотехнологические препараты — новая эра фармакологии
Первый таргетный противоопухолевый препарат был зарегистрирован в 1997 г. Это был ритуксимаб — моноклональное антитело, таргетирующее белок CD20 и использующееся для лечения CD20+ лимфом и других опухолей. Чуть позже, в 2001 г., был зарегистрирован иматиниб — малая молекула, ингибирующая химерную тирозинкиназу и предназначенная для лечения хронического миелолейкоза с BCR-ABL-транслокацией. Эти две разработки ознаменовали начало эры таргетных препаратов, которые действуют направленно на определенную мишень в опухолевых клетках.

С тех пор произошла эволюция таргетных препаратов. Если раньше антитела использовались преимущественно как белковые блокаторы мишеней, то с 2010-х гг. технологии использования антител для создания препаратов расширились. Например, антитела стали использоваться как средства доставки противоопухолевых препаратов: и малых молекул, и радионуклидов. В этом случае антитело помогает доставить препарат напрямую в опухолевую клетку, что позволяет снизить нецелевую токсичность. Сейчас в мире зарегистрировано около 15 таких конъюгатов антител с другими препаратами.
В последнее десятилетие появился и другой класс препаратов — ингибиторы иммунных чекпоинтов. Чекпоинты — это молекулы на поверхности иммунной клетки, способные регулировать ее активность. Так, в норме Т-клетки убивают опухолевые клетки. Но часто Т-клетки не делают этого, так как опухолевые клетки экспрессируют на своей поверхности ингибиторные лиганды. Таким образом опухолевые клетки скрываются от иммунитета. Вместе с открытием этого механизма произошел сдвиг парадигмы: ученые поняли, что можно воздействовать не напрямую на опухолевые клетки, а на иммунные клетки. За счет этого можно стимулировать противоопухолевый иммунный ответ, чтобы иммунная система самого пациента сражалась с опухолью.
Еще одна иммунотерапевтическая технология — это CAR T-терапия. У пациентов берут кровь, выделяют из нее Т-клетки и генетически модифицируют их таким образом, чтобы Т-клетки экспрессировали на своей поверхности химерный антигенный рецептор (CAR). Такой рецептор нацелен на определенные мишени на поверхности опухолевых клеток. Ген, кодирующий рецептор, встраивают в Т-клетки, а затем модифицированные Т-клетки размножают и вводят обратно пациенту. Попав в его организм, специально «обученные» CAR T-клетки более эффективно распознают и уничтожают опухолевые клетки. На сегодняшний день в мире зарегистрировано порядка 10 таких препаратов. В России также ведутся разработки препарата для CAR-T терапии — например, уже зарегистрирована «Утжефра». Все подобные препараты эффективны для лечения онкологических болезней крови, но пока не очень хорошо работают против солидных опухолей.
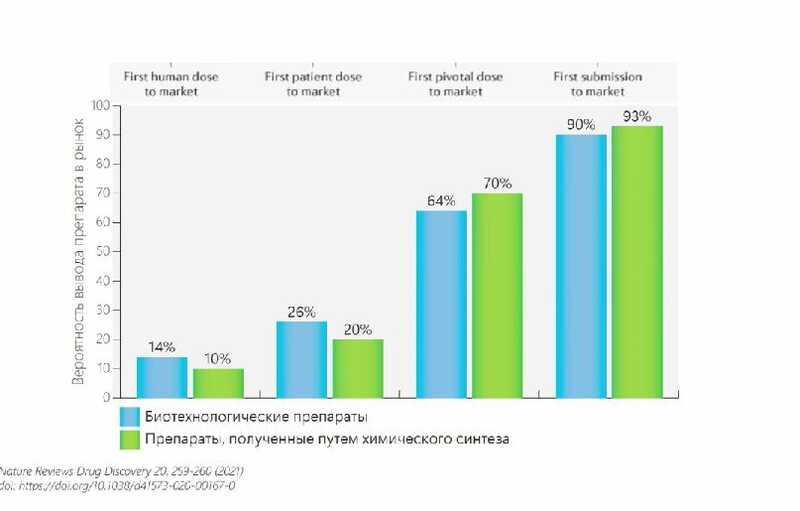
На фоне успеха таких подходов повысилась популярность биотехнологических препаратов. Около 14% биотехнологических препаратов, находящихся на стадии клинических испытаний 1 фазы, доходит до рынка — против 10% препаратов, полученных путем химического синтеза. Из-за того, что биотехнологические препараты потенциально эффективнее доходят до рынка, сейчас уже более половины всех компаний, занимающихся фармразработкой в мире, сосредотачивают свое внимание именно на биотехнологических препаратах.
Тренд на персонализацию терапии
Только во второй половине 20 века в онкологии стали подразделять виды опухолей на более мелкие: если раньше говорили просто о раке легкого, то затем выявили несколько разновидностей — аденокарциному легкого, плоско-, крупно- или мелкоклеточный рак легкого. Такое разделение стало возможным благодаря развитию химиотерапии, ведь врачи и исследователи заметили, что разные типы опухолей по-разному реагируют на лечение. Сейчас выделяют еще больше категорий в каждой разновидности опухолей, опираясь на молекулярно-генетические признаки, в соответствии с наличием мутаций в том или ином гене.
Из-за усложнения классификации опухолей стремительно меняются и рекомендации к терапии. Для каждого молекулярно-генетического вида опухоли имеются определенные группы препаратов и схемы терапии. На сегодняшний день терапевтические рекомендации, на которые должны опираться врачи, содержат ряд обязательных тестирований на те или иные биомаркеры, благодаря которым можно было бы определить молекулярный тип опухоли.
Эта тенденция указывает на то, что сейчас фокус смещается на конкретного пациента и типирование его опухоли и разрабатываются узкие, «точечные» решения. Такой тренд усложняет разработку препаратов: количество необходимых упаковок препаратов сокращается, а стоимость каждого из них растет. Зато препараты, направленные на лечение малой группы пациентов, проходят через упрощенную процедуру регистрации.
Как происходит разработка препаратов?
Сейчас первым шагом в процессе разработки препаратов является идентификация конкретной мишени. Затем отбираются соединения или молекулы, которые наиболее эффективно воздействуют на мишень, и среди них и их модификаций выбирается наиболее перспективный препарат. Он проходит тестирование на клеточных и животных моделях в рамках доклинических испытаний, а затем переходит в исследования на людях в рамках клинических испытаний. Хотя сейчас иногда рамки между разными фазами клинических испытаний размываются, важен сам смысл фаз: тестирование на здоровых добровольцах с целью выявления токсичности, тестирование на пациентах для определения эффективности и побочных эффектов, а затем — тестирование на пациентах для определения эффективности и безопасности. Конечно же, с каждым новым этапом стоимость разработки препарата возрастает, но при этом снижается и риск того, что исследования прекратятся.
Если говорить о всех фармпрепаратах, то около 10% препаратов, дошедших до клинических испытаний, выходят на рынок. В случае же с противоопухолевыми препаратами ситуация сложнее: в этом случае показатель снижается до 5%, т.е. из 20 препаратов, которые дошли до клинических исследований, до пациента дойдет только один.
Доклинические испытания чаще всего начинаются in vitro, где на разных клеточных моделях оценивается цитотоксичность препарата. В качестве моделей могут использоваться как 2D-культуры клеток, так и 3D сфероиды, тумороиды, модели на скаффолдах или «органы на чипе». Впрочем, в сфере разработки препаратов обычно ограничиваются исследованиями на 2D-культурах, ведь 3D-культуры, хотя и более физиологичны, отличаются очень высокой стоимостью и непростым воспроизведением результатов.
Следующий этап разработки — модели in vivo. Чаще всего в онкологии используют мышиные модели. Самый простой способ смоделировать ту или иную опухоль на мыши — привить ей опухолевые клетки нужной клеточной линии. Однако есть и более сложные модели: например, у пациентов изымают опухоль, и ее фрагмент подсаживают иммунодефицитной мыши. В генноинженерных моделях у мышей специально создают мутации в протоонкогенах или генах-онкосупрессорах, которые и приводят к развитию опухолей. Реже встречаются модели с индуцированными опухолями: в этом случае на животное долго воздействуют канцерогеном, и через какое-то время у него развивается опухоль.
Другие животные модели тоже используются в онкологических исследованиях, но реже. Команда Вадима Покровского, к примеру, прививает ксенографты эмбрионам рыбок Danio rerio. Такие модели также позволяют оценивать динамику развития опухоли, а также эффективность противоопухолевых препаратов: их либо добавляют в воду, либо вводят в желточный мешок или в перикард.


Препараты, успешно показавшие себя в тестах на клетках и на животных, доходят до стадии клинических испытаний. Около трети всех клинических испытаний, проводимых в мире, связано с онкологией. В рамках исследований основное внимание уделяется нескольким важным параметрам: продолжительность жизни пациентов, ответ на лечение, время до прогрессирования и качество жизни.
Противоопухолевые препараты в России
В России насчитывается 22 оригинальных противоопухолевых препарата, находящихся на разных стадиях разработки. Часть из них — ингибиторы иммунных чекпоинтов и другие препараты на основе антител — разрабатываются компанией Биокад. Активную разработку препаратов в России также ведет международная компания Астразенека. Есть и ряд других отечественных препаратов — пептидные ингибиторы или малые молекулы, а также онколитические вакцины.


 Меню
Меню





 Все темы
Все темы




 0
0











