Игорь Шохин: как получить терапевтическое моноклональное антитело
Разговор о разработке терапевтических препаратов на лектории «Метафаза» продолжил Игорь Шохин. Он рассказал об особенностях разработки моноклональных антител и о вызовах, с которыми сталкиваются исследователи как в процессе тестов in vitro, так и в клинических испытаниях.

О том, какие исследования моноклональных антител необходимо провести в рамках их разработки и регистрации, рассказывает Игорь Шохин, доктор фармацевтических наук, генеральный директор ООО «ЦФА», главный редактор научно-производственного журнала «Разработка и регистрация лекарственных средств».
Моноклональные антитела — лидеры фармацевтического рынка
История моноклональных антител насчитывает уже 50 лет: в 1975 году был изобретен способ их получения при помощи гибридом. Сегодня существуют различные препараты на основе антител, в том числе для лечения социально значимых заболеваний. Они занимают значимое положение на фармацевтическом рынке: так, последние 10 лет ежегодно самыми продаваемыми терапевтическими препаратами в мире были Хумира (адалимумаб — препарат для лечения аутоиммунных воспалительных заболеваний) и Кейтруда (пембролизумаб — ингибитор PD-1, препарат для лечения меланомы и немелкоклеточного рака легкого). В 2015–2021 гг. лидирующие позиции занимала Хумира, прибыль от продажи которой составила 15–20 млрд в год, а в 2022–2024 гг. на первое место вышла Кейтруда с прибылью 20–25 млрд в год.
Моноклональные антитела могут приниматься как для лечения заболеваний, так и в лабораторной диагностике. Использование антител лежит в основе различных диагностических и лабораторных методов, таких как ИФА, вестерн-блоттинг и проточная цитометрия, где антитела помогают выявить конкретные антигены. Терапевтические моноклональные антитела по большей части применяются в онкологии, а также для лечения аутоиммунных заболеваний или аллергических реакций.
Трудности разработки на этапе in vitro
Разработка моноклональных антител — затратный и длительный процесс. Как подчеркнул Игорь Шохин, в случае разработки биоаналогов ситуация не упрощается: у ООО «ЦФА» есть опыт в разработке биоаналогов адалимумаба и пембролизумаба. Дело в том, что все препараты моноклональных антител уникальны, и нельзя просто повторить молекулу так же, как если бы речь шла о препаратах на основе малых молекул. Поэтому даже при разработке биоаналогов антител до перехода к доклиническим и клиническим исследованиям требуется блок in vitro работ, посвященный анализу биосопоставимости препарата по его физико-химическим и биологическим свойствам.
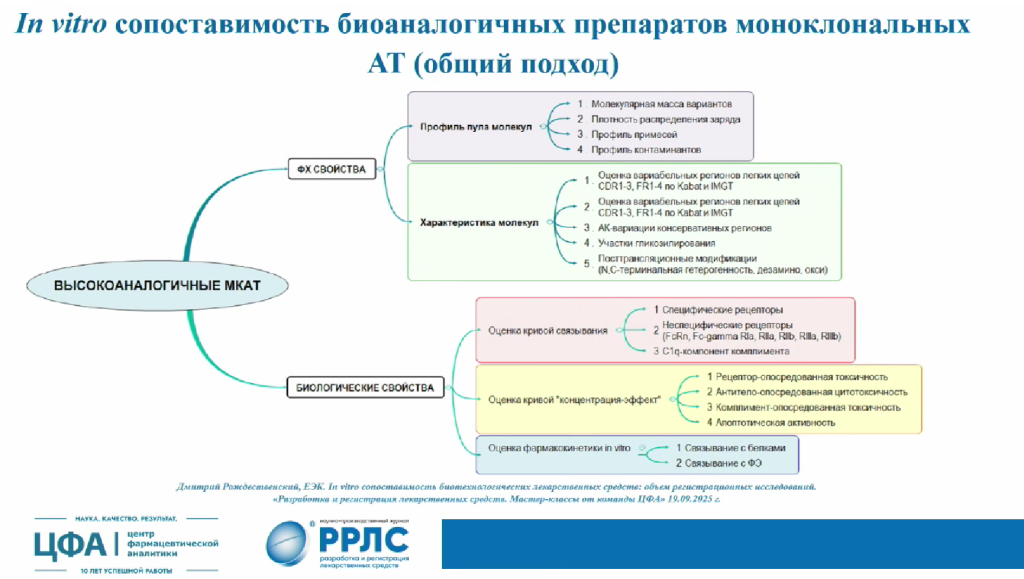
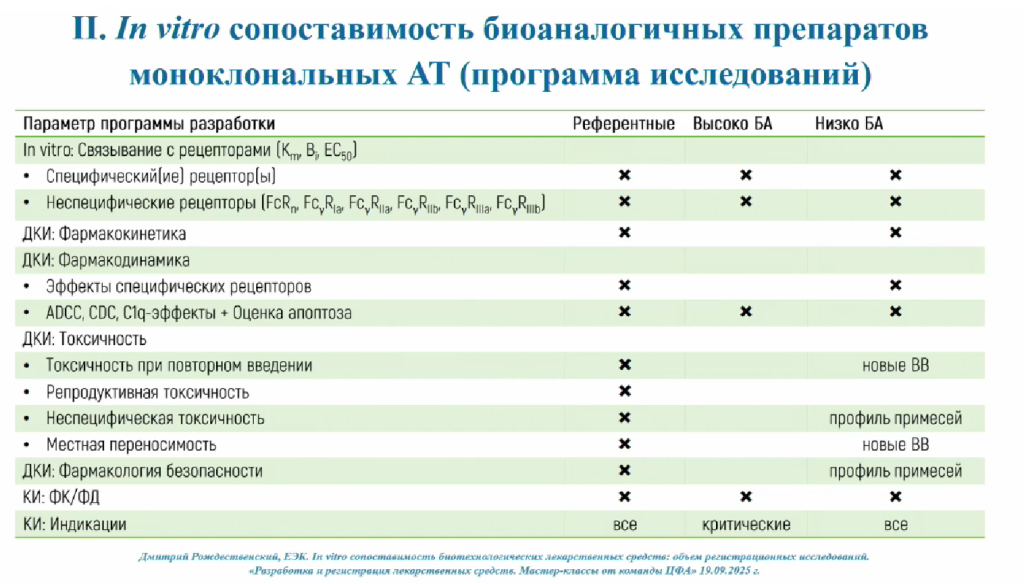
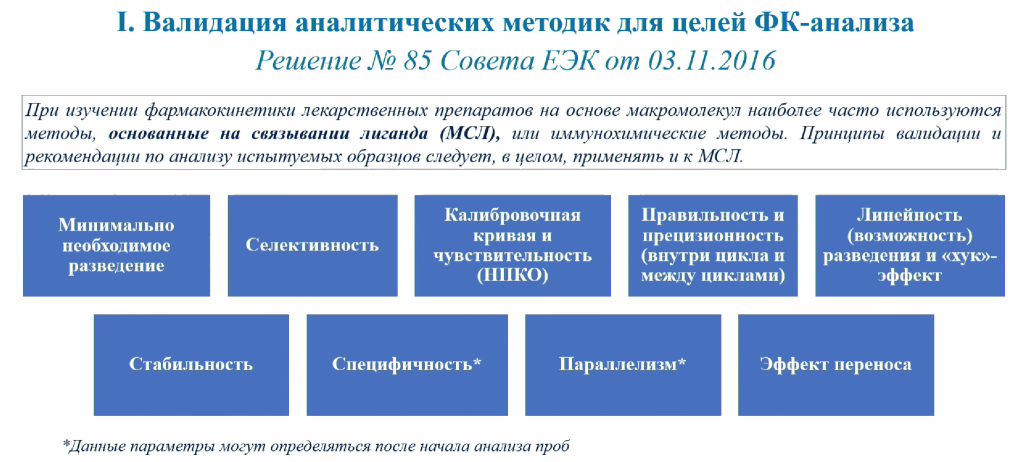
Особое внимание на этапе разработки антител отводится фармакокинетике. Антитела могут циркулировать в крови до нескольких месяцев, что значительно отличает их от привычных лекарств на основе малых молекул. В свою очередь, фармакокинетические параметры антител коррелируют с их фармакодинамическими свойствами. Анализ фармакокинетики в основном проводится с помощью ИФА, причем в России сейчас наблюдается недостаток коммерчески доступных тест-систем ИФА для моноклональных антител. Поэтому перед анализом фармакокинетики лаборатории сталкиваются с задачей валидации методов для ее оценки.
Вызовы в клинических испытаниях
На этапе клинических исследований препаратов антител также возникают трудности. Так, обычно испытания первой фазы проводятся на здоровых добровольцах, чтобы оценить безопасность препарата. Однако в случае антител даже первая фаза должна проводиться на пациентах, причем их количество может достигать 50-100 человек. Ситуация осложняется, если исследуется менее распространенная патология. В этом случае проводят многоцентровые клинические исследования, и центры могут быть «разбросаны» по всей стране. Возникает необходимость обеспечить холодовую цепь для доставки всех собранных образцов.
Еще один важный параметр, который требуется оценивать специалистам, — иммуногенность антител. При введении препарата в организме пациента могут начать вырабатываться антитела к нему — связывающие (которые могут повысить или снизить активность препарата, а могут и не повлиять на него) или нейтрализующие антитела, способные снизить или полностью устранить терапевтическую активность. Иммуногенность лучше оценивать на всех фазах клинических испытаний, но особенно важно — на поздних, когда размер выборки больше и есть возможность исследовать курсовое применение препарата.
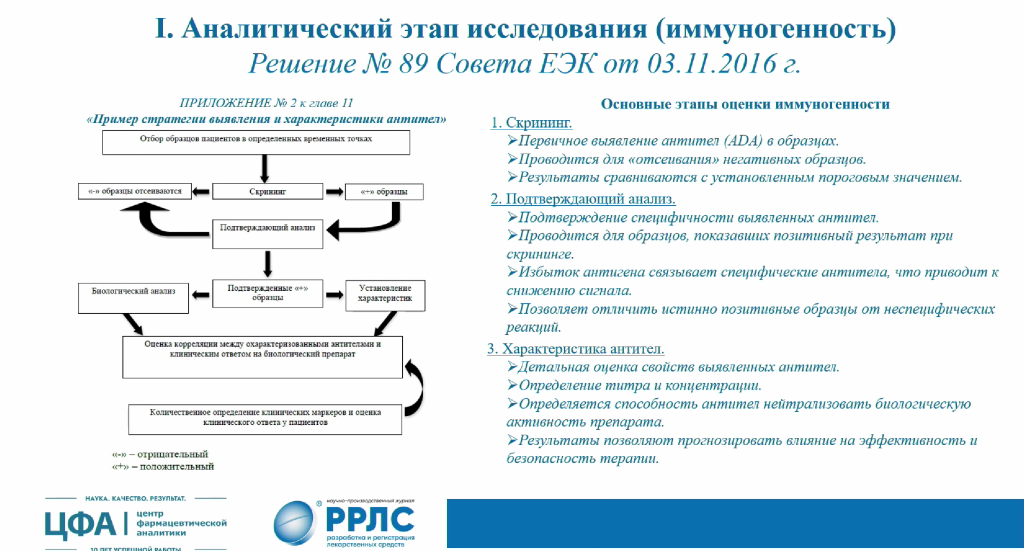
Оценка иммуногенности начинается с нафтолового скрининга проб для выявления образцов, содержащих первичные антитела. Отобранные образцы проходят через подтверждающий анализ с избытком препарата (в этом случае в истинно положительных пробах сигнал подавляется). Затем антитела в пробах более детально характеризуются — определяют титр антител, а также их нейтрализующую способность. В результате даже для анализа всего нескольких истинно положительных проб требуется значительное количество экспериментов.
Собственный опыт разработки биоаналогов
Игорь Шохин поделился опытом собственных исследований in vivo для биоаналога трастузумаба — анти-HER2 антитела, которое применяется для лечения рака молочной железы.
Исследования биоаналога проводились на базе ООО «ЦФА». Перед анализом фармакокинетики препарата ученые разработали и валидировали методику количественного определения трастузумаба в сыворотке крови методом ИФА. Фармакокинетика биоаналога оказалась сопоставимой с параметрами оригинального препарата. Интересно, что разброс значений концентраций антитела в крови добровольцев, принимавших участие в исследовании, оказался существенным: каждая линия на представленных ниже графиках соответствует отдельному человеку. Это еще раз подчеркивает важность персонализации медицины.
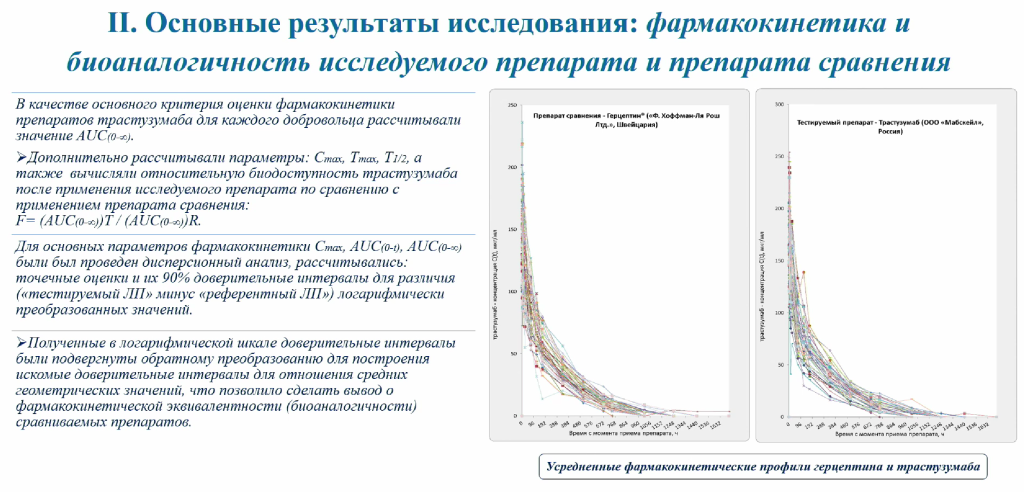
Для оценки иммуногенности исследователи также разработали и валидировали методику полуколичественного определения антител к трастузумабу в сыворотке крови методом ИФА. Чувствительность методики была равна 99,5 нг/мл. Однако в рамках первой и третьей фазы исследований иммуногенность не была выявлена.
В ООО «ЦФА» также оценивались фармакокинетика и иммуногенность ряда других антител — не только биоаналогов, но и оригинальных препаратов.
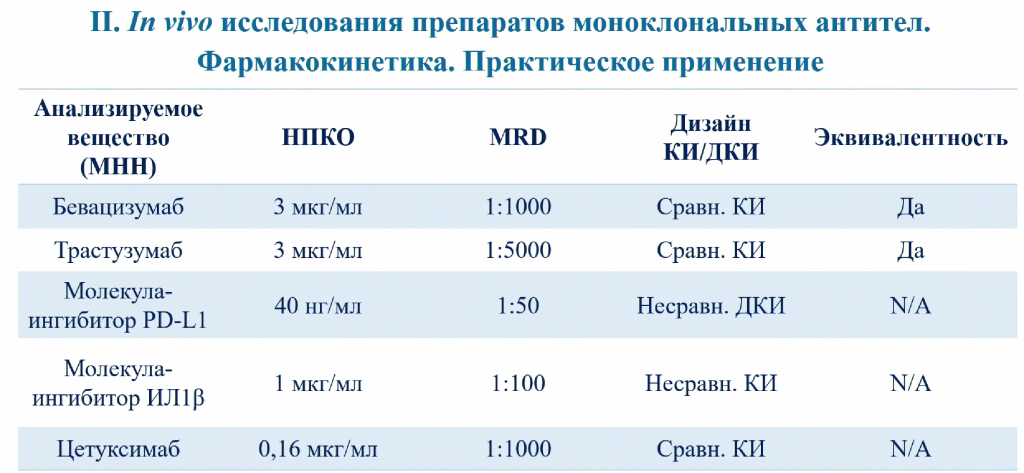
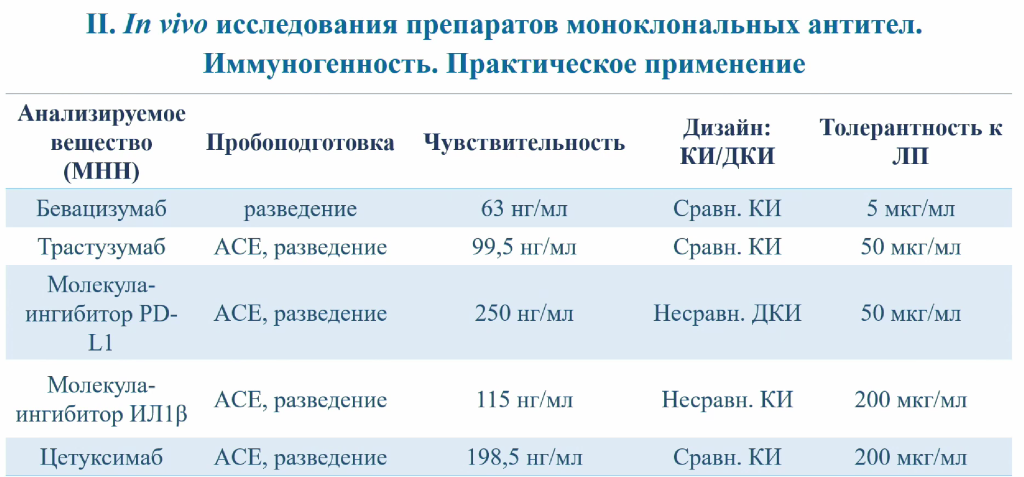
Важность персонализации
После проведения клинических исследований необходимо обратить внимание на два важных фактора — высокую вариабельность индивидуальной фармакокинетики (например, у одного пациента концентрация препарата в крови может составлять 150 мкг/мл, а у другого, получившего такую же дозу, — 600 мкг/мл) и иммуногенности (у одного пациента могут вырабатываться антитела на препарат, а у другого их может и не быть). Соответственно, если нескольким пациентам с одним и тем же заболеваниям выписать лекарство в одной и той же дозировке, нормированной на площадь поверхности тела, у одних препарат может сработать, а у других — нет.
Именно поэтому важна персонализация терапии моноклональными антителами. Персонализация должна производиться на основе равновесной концентрации препарата крови при курсовом применении и наличия нейтрализующих антител к препаратам. При этом нужно учитывать, что антитела к лекарствам могут появиться в любой момент: как в самом начале применения, так и через несколько лет, если человек вынужден непрерывно получать препарат. Чтобы располагать этими данными, важно развивать сферу терапевтического лекарственного мониторинга.
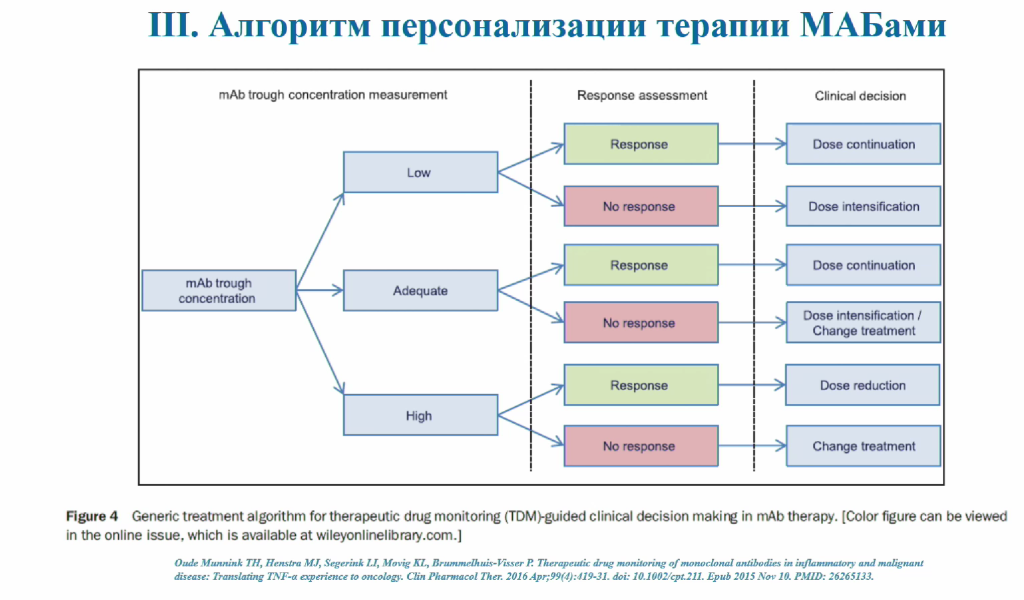
На основе оценки этих параметров, а также ответа пациента на лечение лечащий врач может принимать решения: продолжение лечения с той же дозировкой, изменение дозы или всего курса лечения.
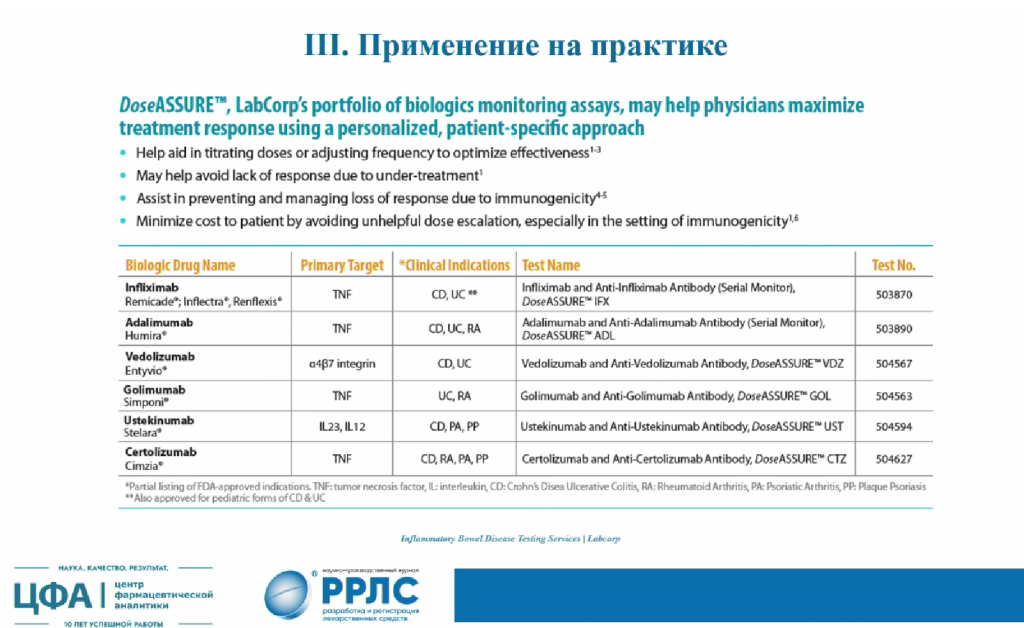
В мире уже существуют коммерчески доступные решения, помогающие врачам отслеживать ответ пациентов на лечение. Например, компания LabCorp выпустила ряд тестов DoseASSURE, интерпретация результатов которых позволяет корректно подобрать дозировку.
Перспективы развития моноклональных антител
Одна из многообещающих разновидностей препаратов на основе антител — конъюгаты антител с лекарственными средствами (ADC, antibody-drug conjugate). Молекула с лекарственной активностью в этом случае присоединяется к антителу с помощью линкера. Особое внимание ADC привлекают в контексте онкологии.
Механизм действия ADC объединяет в себе принципы работы антител и самих цитотоксических препаратов. Например, конъюгат трастузумаб эмтанзин доставляет препарат прямо к опухолевым клеткам, которые оверэкспрессируют HER2. После связывания с рецептором конъюгат попадает в клетки, в результате линкер разрывается, а внутри опухолевых клеток высвобождается эмтанзин — ингибитор сборки микротрубочек.
В ряде стран ADC уже применяются в клинике. В России некоторые оригинальные конъюгаты зарегистрированы зарубежными компаниями, однако так и не дошли до реального применения. ООО «ЦФА» занимается в том числе разработкой биоаналогов таких препаратов.

Однако разработка биоаналогов ADC — еще более сложная задача. Она требует доказательства биосопоставимости свободного антитела, конъюгата, а также высвобожденного цитотоксического вещества. Последний пункт особенно важен: по сути, он требует проверки работы линкера, чтобы исключить ситуацию, когда линкер разрывается в кровотоке и токсин высвобождается, не дойдя до опухоли.


 Меню
Меню





 Все темы
Все темы




 0
0











