Дмитрий Жданов о регуляторных Т-клетках и балансе иммунитета
Год с научно-популярным лекторием «Метафаза» завершила лекция Дмитрия Жданова о регуляторных Т-клетках, открытие которых было отмечено Нобелевской премией. Функции этих неуловимых из-за своей пластичности клеток разнообразны, их дисфункция приводит к аутоиммунным и онкологическим заболеваниям. В то же время регуляторные Т-клетки могут стать основой клеточных терапий.

Д.б.н., доцент Дмитрий Жданов — заведующий лабораторией медицинской биотехнологии, главный научный сотрудник ФГБНУ НИИ биомедицинской химии им. В.Н. Ореховича, профессор кафедры биохимии РУДН. Он выступил с лекцией «Регуляторные Т-клетки: иммунитет под контролем». За открытие этой субпопуляции Т-клеток в этом году получили Нобелевскую премию по физиологии или медицине Симон Сакагути, Фред Рамсделл и Мэри Брункоу.
Как устроен клеточный иммунитет
Клеточный иммунитет можно разделить на врожденный и приобретенный (адаптивный). Врожденный иммунитет — это первое звено иммунного ответа, которое встречает патоген при инфекции. Так, нейтрофилы способны выбрасывать внеклеточные ловушки, состоящие из ДНК, чтобы захватить в них патогены, фагоцитирующие клетки поглощают чужеродные агенты. Если же врожденный иммунитет не справляется, то в игру вступает адаптивный иммунитет. Специализированные клетки, как Т- и B-лимфоциты, в основном и обеспечивают адаптивную защиту от патогенов: например, B-клетки ответственны за выработку антител.
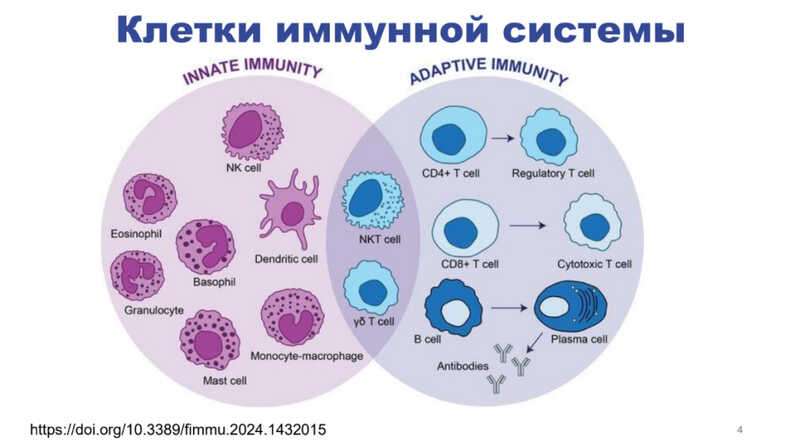
Каждая иммунная клетка происходит от гематопоэтической стволовой клетки, которая находится в костном мозге. В соответствии с получаемыми химическими сигналами стволовые клетки дифференцируются в одном из двух направлений — миелоидном или лимфоидном. От общего миелоидного предшественника, который развивается в костном мозге, происходят тромбоциты, эритроциты, базофилы, нейтрофилы, эозинофилы и макрофаги, а от общего лимфоидного предшественника — NK-клетки, Т- и B-лимфоциты. В-лимфоциты также созревают в костном мозге, а Т-лимфоциты — в тимусе (вилочковой железе).
Дмитрий Жданов отметил, что разделение на врожденный и адаптивный иммунитет довольно условно, ведь многие пути между ними пересекаются. Врожденный иммунитет реагирует раньше (в первые часы инфекции), ответствен за острое и хроническое воспаление; клетки врожденного иммунитета вырабатывают различные факторы, способствующие нейтрализации или гибели патогенов. А вот реакция адаптивного иммунитета возникает позже — до семи суток после инфекции. Клетки адаптивного иммунитета способны обучаться, запоминать те антигены, с которыми встречались, и сохранять эту информацию в виде клеток памяти. Благодаря этому при повторной встрече с патогеном иммунный ответ возникает быстрее.
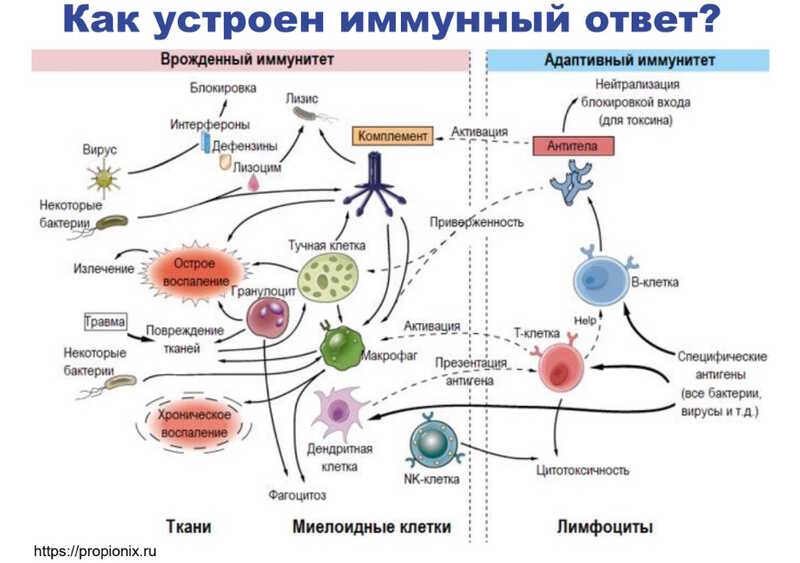
Опасен для патогенов, безвреден для своих
Иногда иммунные клетки атакуют и собственные клетки организма в ходе так называемых аутоиммунных реакций. Как же природа препятствовала тому, чтобы Т-клетки не атаковали «свое»?
Это происходит во время обучения Т-лимфоцитов в тимусе. Механизм, по которому клетки тимуса обучают Т-лимфоциты, до сих пор не до конца понятен. Функциональный тимус есть только у детей, а к 12 годам этот орган уменьшается в размере, его структуры замещаются жировой тканью и перестает функционировать. Во время обучения клетки тимуса презентуют на своей поверхности фрагменты эндогенных белков, и среди Т-клеток отбираются те, рецепторы на поверхности которых не способны распознавать белки организма. Такие клетки мигрируют из тимуса в кровоток, а те, что не прошли отбор, элиминируются.
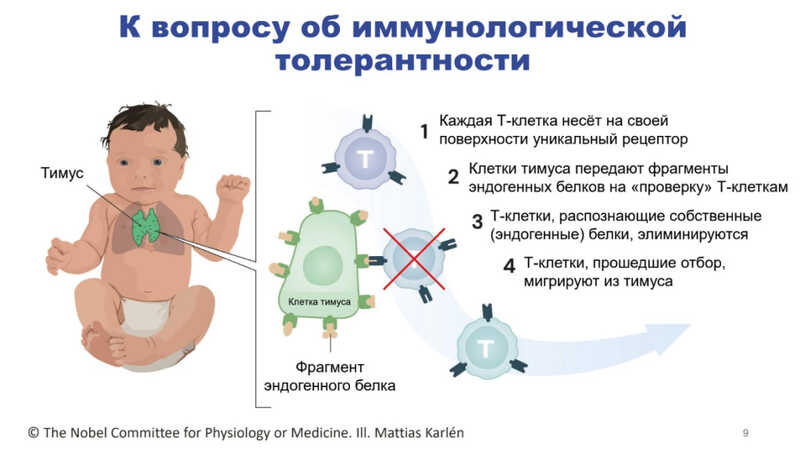
Открытие регуляторных Т-клеток: три независимых сюжета
В 1980-х годах японские ученые попробовали удалить тимус у новорожденных мышей и обнаружили, что это приводит к развитию аутоиммунных заболеваний. У таких мышей выпадает шерсть и нарушается развитие внутренних органов. Но если ввести им зрелые Т-клетки от генетически идентичных здоровых мышей, то гиперактивация иммунной системы предотвращается. Тогда стало ясно, что в популяции Т-лимфоцитов присутствуют клетки, которые каким-то образом подавляют иммунитет. Такие клетки назвали супрессорными, но подробностей о них пока не знали.
В 1990-х годах Симон Сакагути провел эксперимент с бестимусными мышами, в котором животным вводили различные субпопуляции Т-клеток. Если животному вводили CD4+ Т-клетки, среди которых присутствовали CD25+ Т-клеток (CD25 — рецептор к цитокину IL-2, который запускает пролиферацию иммунных клеток), то тогда мышь была здоровой. На этом этапе Сакагути еще не называл найденную субпопуляцию Т-клеток регуляторными, но уже утверждал, что она поддерживает иммунологическую толерантность к своим антигенам.
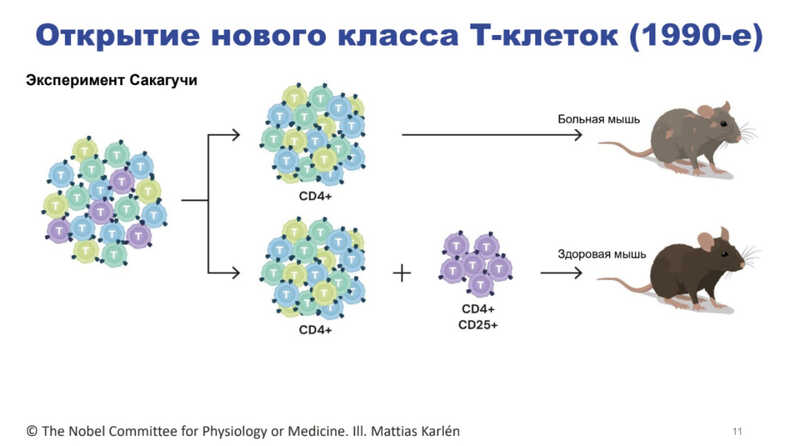
В 2000 году Симон Сакагути с коллегами опубликовали статью в журнале Cell, в которой уже закрепили термин «регуляторные Т-клетки» и суммировали всю известную информацию о них. С тех пор количество публикаций по запросу «regulatory T cell» в базе данных PubMed начинает расти.
Однако позднее выяснилось, что рецептор CD25 на своей поверхности могут нести не только регуляторные, но и эффекторные Т-клетки. Встал вопрос о более специфичном маркере регуляторных Т-клеток (надо отметить, что и сейчас эта проблема не до конца решена).
Параллельно в США происходили другие исследования. С середины ХХ века рамках Манхэттенского проекта изучалось влияние радиации на млекопитающих. Среди мутантных линий мышей, которые получили и поддерживали в ходе этих исследований, были мыши scurfy с прищуренными глазами, маленькими ушами и шелушащейся кожей. Эти животные стали моделью для изучения аутоиммунных реакций, но не было понятно, что является причиной этого фенотипа.
В 2000-х годах в биотехнологической компании Darwin Molecular Corporation, где работали Мэри Брункоу и Фред Рамсделл, заинтересовались мышами этой линии. Исследователи поняли, что этот фенотип сцеплен с Х-хромосомой, так как проявлялся только у самцов. После некоторых экспериментов они выявили участок ДНК на Х хромосоме, в котором может быть патогенная мутация. Мутация, связанная с фенотипом scurfy, была найдена в гене Foxp3. Два лишних аденина вызывали сдвиг рамки считывания, что приводило к нарушению трансляции функционального белка FOXP3.
Еще одна история связана с синдромом IPEX, который назван по первым буквам основных симптомов: иммунодисрегуляция, полиэндокринопатия, энтеропатия, Х-сцепленность. Это заболевание довольно редкое: в 2019 году в мире было зарегистрировано лишь 150 клинических случаев. Однако в 2000-х гг. исследователи, в том числе Фред Рамсделл и Мэри Брункоу, показали, что синдром IPEX вызван мутациями в гене FOXP3, которые приводят к такому же сдвигу рамки считывания и синтезу нефункционального белка.
В 2003 году Симон Сакагути с соавторами также пришли к выводу, что FOXP3 — транскрипционный фактор, отвечающий за развитие регуляторных Т-клеток. Этот белок находится в ядре клеток и запускает транскрипцию генов, связанных с идентичностью регуляторных Т-клеток. Сейчас FOXP3 считается одним из главных маркеров регуляторных Т-клеток.
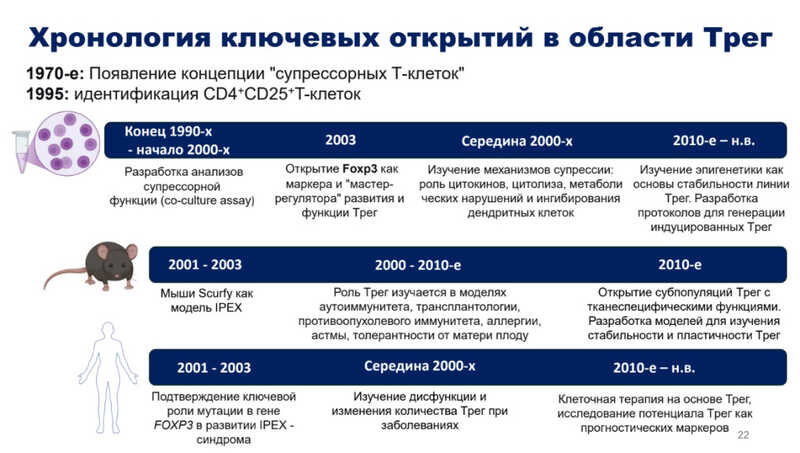
С этого момента регуляторные Т-клетки стали изучаться подробнее. Была открыта их роль в развитии аутоиммунных заболеваний, трансплантологии, формировании противоопухолевого иммунитета, аллергии, астмы и т.д. В 2010-х гг. у мышей были обнаружены тканеспецифичные субпопуляции регуляторных Т-клеток и стали разрабатываться модели, позволяющие изучать их стабильность и пластичность. В то же время появилась концепция клеточных терапий на основе регуляторных Т-клеток, а также использования их в качестве прогностических маркеров.
Неуловимые Треги и их функции
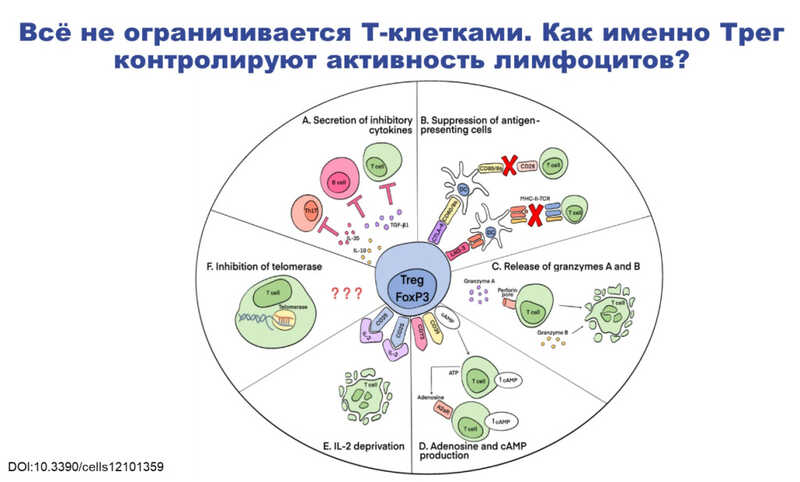
Основная задача регуляторных Т-клеток — подавление эффекторных Т-клеток в том случае, если они неадекватно реагируют на собственные антигены организма. В этой ситуации регуляторная Т-клетка вступает в конкурентное взаимодействие с эффекторной и вырабатывает подавляющие цитокины, которые тормозят ее действие.
Для реализации своих функций регуляторные Т-клетки могут контактировать с лимфоцитами или клетками-посредниками. Они могут секретировать гранзимы — белки, вызывающие апоптоз и лизис эффекторных Т-клеток или подавлять их избыточную активность с помощью супрессорных цитокинов (IL-10, IL-35, TGFb). Также регуляторные Т-клетки могут конкурировать с эффекторными Т-клетками за IL-2, лишая их доступа к этому цитокину. Наконец, регуляторные Т-клетки по еще не установленному механизму могут ингибировать активность теломеразы в эффекторных лимфоцитах, что ограничивает их пролиферацию.
Регуляторные Т-клетки созревают в тимусе, а затем переходят в лимфоузлы. Они также способны мигрировать в очаги воспаления, оказываясь при этом в периферической крови. В этом состоянии регуляторная клетка уже называется клеткой памяти.
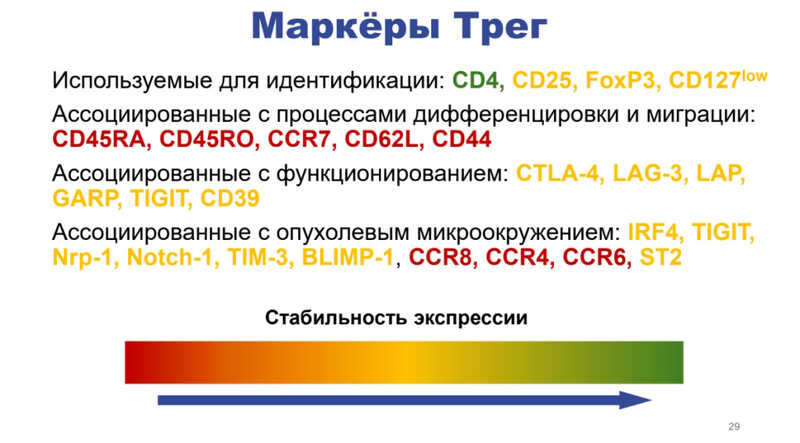
Для регуляторных Т-клеток характерна высокая фенотипическая пластичность. Единственный белок, который постоянно экспрессируется в этих клетках, — CD4. Экспрессия CD25 и FoxP3 может снижаться при инфильтрации в очаги воспаления или в опухолевое микроокружение. В то же время у регуляторных Т-клеток могут появляться новые функциональные маркеры, присущие не только этим клеткам, но и сильно варьирующие между разными типами клеток.
Дмитрий Жданов выделил четыре основных процесса, в которые вовлечены регуляторные Т-клетки. Во-первых, они контролируют силу и продолжительность иммунного ответа. Во-вторых, они предотвращают отторжение плода иммунной системой матери. В-третьих, резидентные регуляторные Т-клетки контролируют локальный иммунный ответ для поддержания толерантности к местной среде и ее специфическим антигенам: например, в случае кишечника — к антигенам микробиоты кишечника. В-четвертых, эти клети предотвращают возникновение аутоиммунных реакций за счет контроля иммунного ответа на собственные антигены.
К чему приводит дисфункция регуляторных Т-клеток
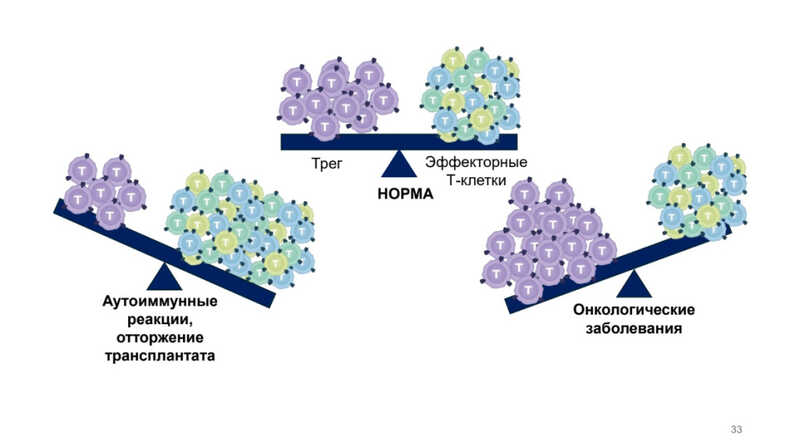
Для функционирования регуляторных Т-клеток важны два параметра: их количество в периферической крови и способность выполнять регуляторное действие. Так, в норме регуляторные Т-клетки составляют до 10% от всех Т-клеток, а при аутоиммунных заболеваниях их доля может снижаться до 5% и менее, при онкологических — напротив, повышаться до 50%. В последнем случае опухоли злоупотребляют гиперактивностью регуляторных Т-клеток, чтобы ускользнуть от уничтожения иммунитетом.
Если же иммунных клеток слишком мало, то иммунные клетки, напротив, гиперактивируются и могут разрушать собственные ткани и органы.
Считается, что при диабете 1-го типа нарушены сигнальные пути, связанные с цитокинами, в том числе IL-2. Кроме того, нарушается пластичность регуляторных Т-клеток: под действием воспалительных цитокинов их доля снижается. Также к диабету 1-го типа могут приводить мутации в генах, ассоциированных с регуляторными Т-клетками.
При рассеянном склерозе активированные лимфоциты могут разрушать миелиновую оболочку нервных клеток периферической системы. В этом случае доля регуляторных Т-клеток также снижена.
Количество регуляторных Т-клеток тоже уменьшается и при отторжении трансплантата. А регенеративная терапия на основе регуляторных Т-клеток может повысить толерантность организма к нему.
Дисфункция регуляторных Т-клеток может способствовать реакции «трансплантат против хозяина», когда после пересадки костного мозга клетки донора воспринимают клетки реципиента как чужеродные и атакуют их. Здесь регуляторные Т-клетки тоже могут открыть новые терапевтические возможности.
Регуляторные Т-клетки в основе терапии
Принцип регенеративной терапии на основе регуляторных Т-клеток предполагает изоляцию этих клеток из организма пациента, модификацию для улучшения их свойств и введение полученного клеточного продукта назад в организм пациента. Источником регуляторных Т-клеток для терапии может быть периферическая кровь, пуповинная кровь или тимус (последний чаще у животных).
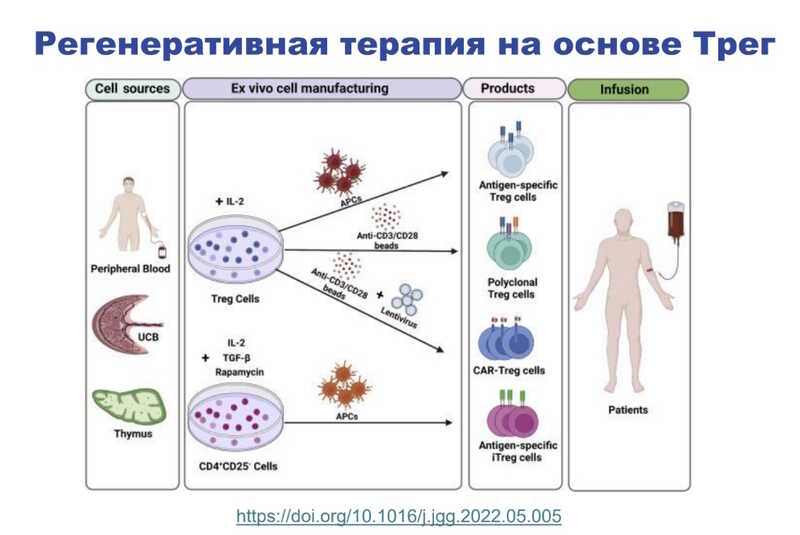
Основная цель терапии — увеличение количества регуляторных Т-клеток. В условиях ex vivo их размножают под действием IL-2 и TGFb, антитела, стимулирующие пролиферацию, и затем вводят пациенту. Генетическая модификация регуляторных Т-клеток также может обеспечить экспрессию в них некоторых нужных рецепторов, которые помогали бы подавлять опухолевый рост или специфические лимфоциты. Сейчас в США проходят клинические испытания несколько клеточных продуктов на основе регуляторных Т-клеток, которые используются для лечения рассеянного склероза, диабета 1-го типа, волчанки и других аутоиммунных заболеваний.
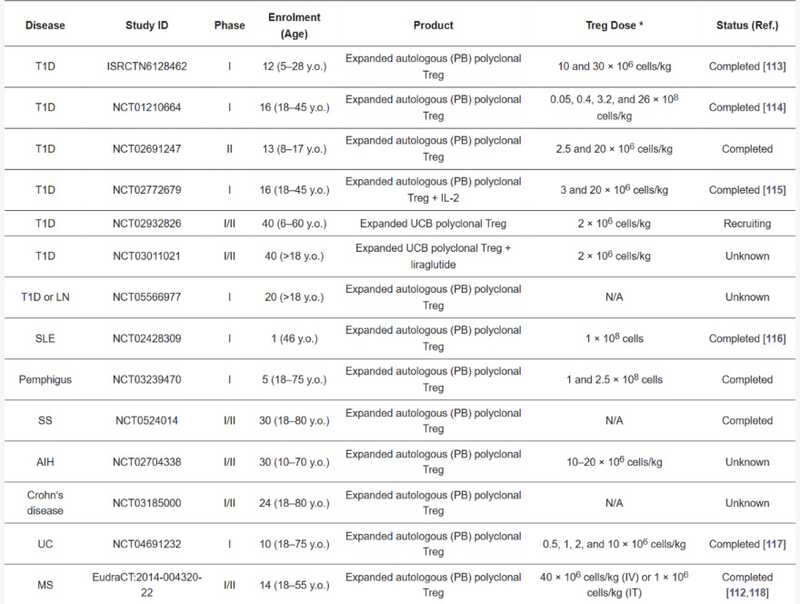 T1D — диабет 1-го типа, LN — волчаночный нефрит, SLE — системная красная волчанка, pemphigus — пузырчатка, SS — системный склероз, AIH — аутоиммунный гепатит, UC — язвенный колит, MS — рассеянный склероз. Credit: Int. J. Mol. Sci., 2025, DOI:
10.3390/ijms262110340
T1D — диабет 1-го типа, LN — волчаночный нефрит, SLE — системная красная волчанка, pemphigus — пузырчатка, SS — системный склероз, AIH — аутоиммунный гепатит, UC — язвенный колит, MS — рассеянный склероз. Credit: Int. J. Mol. Sci., 2025, DOI:
10.3390/ijms262110340
Однако у такой терапии есть ограничения. Во-первых, регуляторные Т-клетки пластичны и, следовательно, недостаточно стабильны. Их фенотип могут изменять даже незначительные воздействия. Выращенные в «тепличных» условиях ex vivo клетки при повторном введении в организм могут вести себя уже по-другому. Во-вторых, при ряде заболеваний функциональная активность регуляторных Т-клеток также может нарушаться, так что при повышении количества этих клеток проблема не будет решена. В-третьих, обычно удается выделить лишь небольшое количество регуляторных Т-клеток — так, из 100 мл периферической крови может выделиться примерно миллион регуляторных Т-клеток, что крайне мало, а процедура их принудительного размножения не всегда предсказуема.
Роль альтернативного сплайсинга FOXP3
мРНК белка FOXP3 содержит 11 экзонов. В 2005 году был описан альтернативный сплайсинг FOXP3, затрагивающий экзоны 2 и 7, что приводит к образованию четырех сплайсоформ белка с разными функциями. Так, известно, что за счет экзона 2 FOXP3 может вступать в белок-белковые взаимодействия, а за счет экзона 7 димеризоваться.
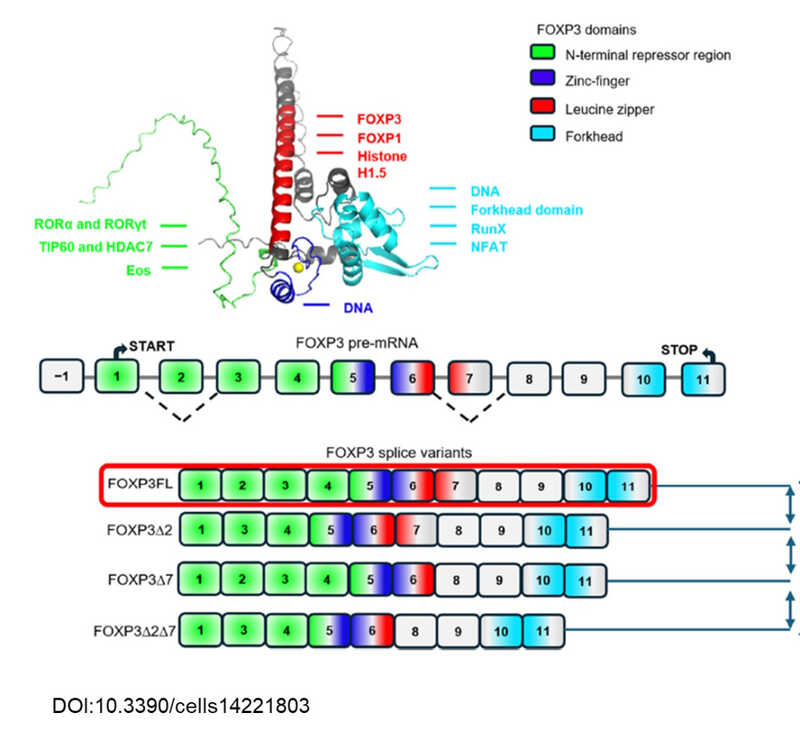
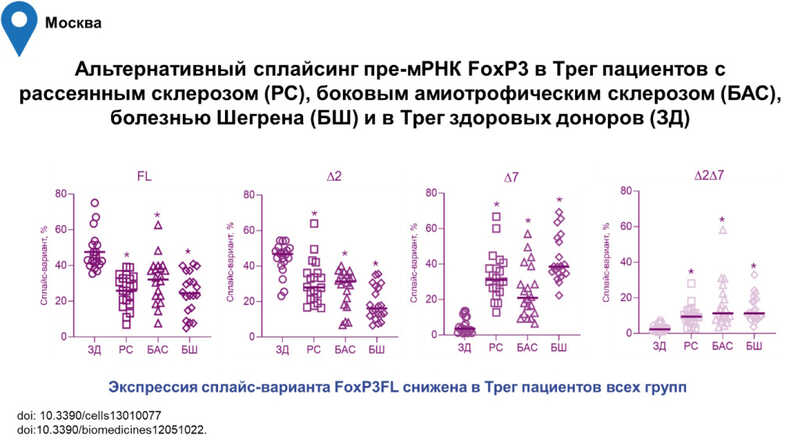
Команда Дмитрия Жданова исследует роль сплайс-форм FOXP3. Ученые выделяют регуляторные Т-клетки у здоровых доноров, а также у пациентов с рассеянным склерозом, боковым амиотрофическим склерозом и болезнью Шегрена. После выделения клеток ученые анализируют в них уровень экспрессии общего FOXP3 и отдельных сплайс-форм. Затем они культивируют эти клетки ex vivo и индуцируют экспрессию разных сплайс-форм с помощью специальных олигонуклеотидов, после чего оценивают супрессорную активность модифицированных клеток.
Исследователи выяснили, что в клетках здоровых доноров преобладает полноценная сплайсоформа, а вот в клетках пациентов с аутоиммунными заболеваниями преобладают сплайсоформы с делецией экзона 2 и/или 7.
Переключающие сплайсинг олигонуклеотиды — это класс терапевтических олигонуклеотидов, способных изменять течение сплайсинга, давая «указания» сплайсосоме. Подобрав такие олигонуклеотиды, ученые действительно смогли модулировать экспрессию индивидуальных сплайс-форм FOXP3 в клетках. Пролиферативная активность таких модифицированных клеток сильно различается. У клеток с полноразмерным FoxP3 пролиферация протекает лучше всего, а вот у клеток с делециями экзонов пролиферация значительно снижена, кластеры пролиферации не наблюдаются.
Супрессорную активность оценивают по способности регуляторных Т-клеток подавлять эффекторные Т-клетки, то есть определяют, какая доля регуляторных клеток необходима для подавления. Например, клетки с полноразмерной формой FoxP3 могут подавлять эффекторные в соотношении 1:96, а клетки с делециями экзонов гораздо менее активны: у них эти пропорции варьируются от 1:8 до 1:1.
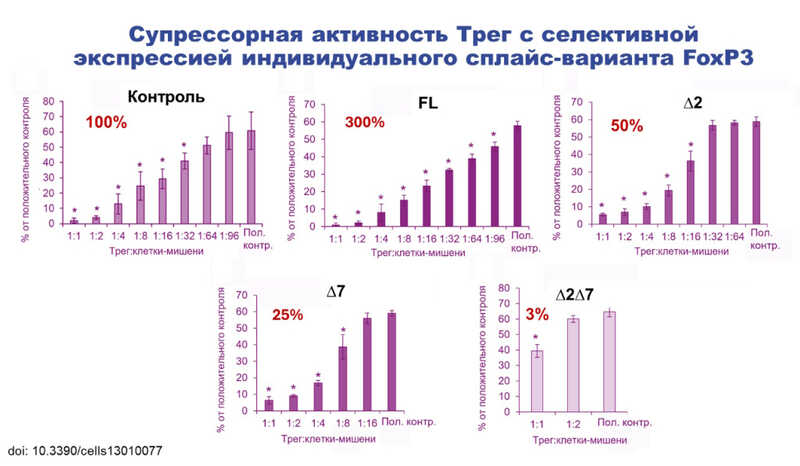
Эти данные соотносятся с информацией о том, что у пациентов с аутоиммунными заболеваниями число регуляторных Т-клеток в крови понижено. Поскольку в их крови преобладают клетки с альтернативными сплайс-формами FoxP3, не способные активно пролиферировать, то их число и остается сниженным. Эти клетки менее активно делятся и менее активно подавляют лимфоциты.


 Меню
Меню





 Все темы
Все темы




 0
0











