Чувствительный к венетоклаксу переключатель снизил токсичность CAR T-клеток
Цитокиновый шторм и истощение Т-клеток — одни из основных проблем CAR-Т-терапии, которые можно решить за счет регуляции активности Т-клеток «извне». Ученые из Германии и Швейцарии разработали DROP-CAR-Т-клетки, активность которых снижается в присутствии венетоклакса, и показали, что ими можно управлять в тестах in vivo, а также при моделировании цитокинового шторма in vitro. Благодаря модульной конструкции система DROP может использоваться и в других синтетических рецепторах.
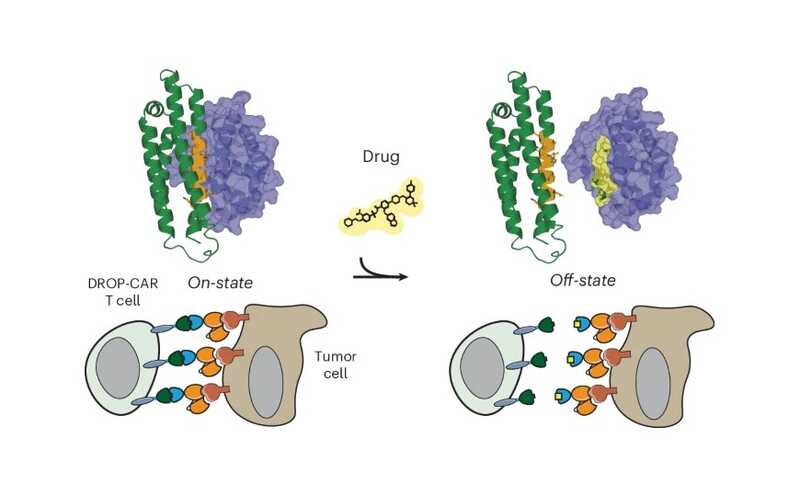
Nature Chemical Biology (2026). DOI: 10.1038/s41589-026-02152-x | CC BY 4.0
Одно из существующих ограничений CAR T-терапии — это целевая, но внеопухолевая токсичность, а также истощение Т-клеток из-за хронического контакта с целевым антигеном. Преодолеть эти проблемы можно за счет создания CAR T-клеток с контролируемой активацией. Например, если переделать CAR-рецептор таким образом, чтобы в его состав входил чувствительный к какой-нибудь малой молекуле белковый элемент, то можно дистанционно управлять активностью Т-клеток. Однако до сих пор такие решения мало применяются на практике, в том числе из-за малого разнообразия белковых элементов человеческого происхождения (с минимальной иммуногенностью), способных реагировать на одобренные к применению в клинике малые молекулы.
Ученые из Германии и Швейцарии разработали DROP-CAR T-клетки, которые чувствительны к венетоклаксу. В основе работы этой системы лежит взаимодействие между белком Bcl-2 в составе химерного антигенного рецептора (CAR) и дизайнерским белком LD3, которое нарушается в присутствии венетоклакса — специфического ингибитора Bcl-2, разрешенного к применению при онкозаболеваниях. Таким образом, во внеклеточной части CAR находятся последовательно LD3, Bcl-2 и scFv-фрагмент, распознающий целевой антиген. В присутствии же венетоклакса Bcl-2 отщепляется вместе с соединенным с ним scFv-фрагментом, из-за чего CAR T-клетка теряет свои CAR-рецепторы.
В in vitro тестах ученые использовали DROP-CAR-Т-клетки линии Jurkat, нацеленные на антигены HER2 и PSMA. Диссоциация scFv-фрагментов от рецепторов начиналась уже через 5 часов после инкубации с 1 мкМ венетоклакса, а спустя 24 часа практически все Т-клетки теряли способность распознавать антиген. При этом ученые показали, что уменьшается количество межклеточных взаимодействий между DROP-CAR Т-клетками и целевыми опухолевыми клетками.
Такая система позволяет конструировать и двойные CAR T-клетки — несущие CAR двух типов, нацеленные на два антигена, что предотвращает антигенное уклонение. В случае с двойными DROP-CAR T-клетками ученым удалось контролировать активность против каждого из двух антигенов — CD19 и PSMA — по отдельности за счет использования разных белков, связанных с LD3. В одном случае рецептор содержал Bcl-2, а в другом — родственный ему белок Bcl-xL. При этом в первом случае для «остановки» Т-клеток требовался венетоклакс, а во втором — малая молекула A-1155463. Так как оба ингибитора специфичны к своим мишеням, каждый из них не мешал Т-клеткам детектировать второй антиген.
Модуль DROP, состоящий из белков LD3 и Bcl-2, оказалось возможным встраивать и в другие системы синтетических рецепторов. Например, система GEMS представляет собой рецепторы, состоящие из scFv-фрагментов к нужному антигену, внеклеточной и трансмембранной частей рецептора к эритропоэтину (EpoR), внутриклеточных доменов для передачи сигнала и запуска сигнальных каскадов. Такая система позволяет активировать за счет специфических воздействий интересующие сигнальные каскады (например, JAK/STAT, PI3K/Akt). В своем эксперименте ученые встроили модуль LD3:Bcl2 между EpoR и нанотелами к кофеину и экспрессировали такую систему в клетках HEK293T. В результате можно было активировать целевой сигнальный путь с помощью кофеина, но прекращать его активацию с помощью венетоклакса. Таким образом, ученые показали, что с помощью комбинации разных модулей можно реализовывать логические операции типа «И–НЕ».
Работу системы протестировали в первичных Т-клетках человека. Ученые сравнили обычные CAR T-клетки и DROP-CAR-Т-клетки, нацеленные на PSMA, в тесте с опухолевыми клетками PC3-PIP. Уровни продукции интерферона-гамма у Т-клеток обоих типов был сравнимыми, и в тесте на цитотоксичность IncuCyte они показали себя схоже, причем цитотоксическая активность DROP-CAR T-клеток ожидаемо снижалась под действием венетоклакса.
В эксперименте на мышиной модели с подкожной опухолью линии PC3-PIP и обычные CAR T-клетки, и DROP-CAR T-клетки эффективно подавляли рост опухоли. При введении венетоклакса действие DROP-CAR-Т-клеток, но не обычных CAR-Т-клеток прекращалось. Как только прием венетоклакса прекращался, DROP-CAR-Т-клетки снова становились активными.
Работу DROP-CAR-Т-клеток также сравнили с другими CAR-Т-клетками, регулируемыми малыми молекулами, — DEG-CAR-Т-клетками. Последние несут в своих рецепторах дегроны, поэтому в присутствии леналидомида рецепторы убиквитинируются и разрушаются в протеасоме. (Подробнее о CAR с дегронами на PCR.NEWS; кстати, эту работу 2024 года сделала та же исследовательская группа.) DEG-CAR T-клетки неиммуногенны и одобрены клинически, а так как принцип их регуляции не влияет на DROP-CAR-Т-клетки, авторы предположили, что в теории эти подходы можно комбинировать. В тестах in vitro ученые показали, что 2.5 мкМ венетоклакс предотвращает цитотоксическое действие DROP-CAR Т-клеток, и такой же эффект для DEG-CAR Т-клеток наблюдается при воздействии 100 нМ-1 мкМ леналидомида. Оба вещества никак не затрагивают обычные CAR Т-клетки, также не наблюдалось перекрестных эффектов между венетоклаксом и леналидомидом.
Наконец, ученые сделали in vitro эксперимент, показывающий, что система DROP может предотвратить развитие цитокинового шторма — наиболее опасного побочного эффекта CAR T-терапии. CAR T-клетки культивировали вместе с моноцитами и целевыми опухолевыми клетками в присутствии малых молекул (венетоклакса или леналидомида в зависимости от используемой системы) и периодически измеряли уровень IL-6 в культуральной среде. Под действием венетоклакса выработка IL-6 DROP-CAR Т-клетками полностью прекратилась, в то время как леналидомид справился с подавлением выработки цитокинов DEG-CAR Т-клетками только один раз из трех. Таким образом, DROP-CAR T-клетки лучше, чем CAR Т-клетки с дегроновой системой, могут регулироваться «извне» для подавления цитокинового шторма.
Атаку CAR T-клеток друг на друга предотвратили с помощью редактирования оснований CRISPR-системой
CAR T-клетки можно дистанционно «включать» и «выключать» малыми молекулами
Источник
Scheller L., et al. Drug-controlled CAR T cells through the regulation of cell–cell interactions // Nature Chemical Biology (2026). DOI: 10.1038/s41589-026-02152-x


 Меню
Меню





 Все темы
Все темы




 0
0











