Эффективность существующих лекарств против нового вируса оценил искусственный интеллект
Корейские биоинформатики прогнозируют активность уже представленных на рынке препаратов против 2019-nCoV, оценивая in silico их способность связываться с вирусной протеиназой. Наилучшие результаты показал антиретровирусный препарат атазанавир. Авторы считают, что их результаты могут ускорить поиск лекарства.
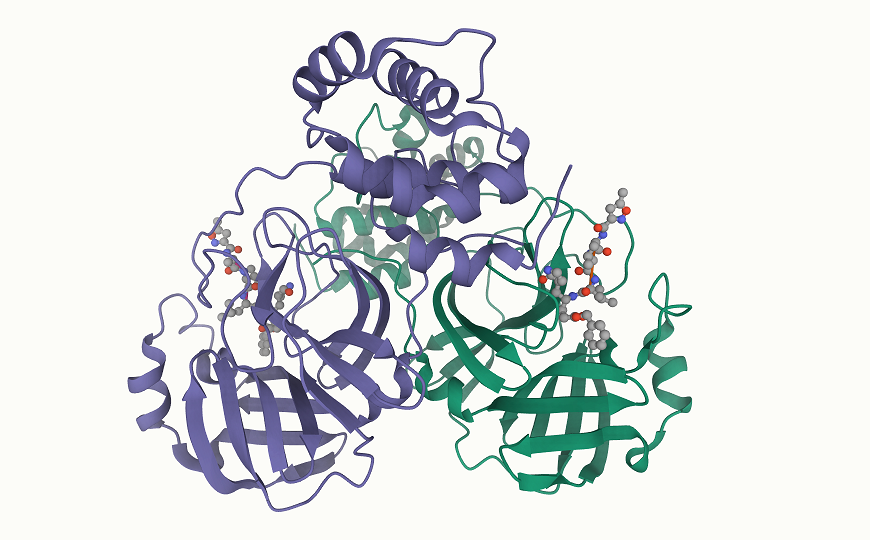
Структура протеиназы 2019-nCoV в комплексе с ингибитором N3 (акцептором Михаэля)
Credit: Wolrdwide Protein Data Bank | https://jvi.asm.org/content/82/5/2515
Для борьбы со вспышкой нового коронавируса важно определить, какие из существующих противовирусных препаратов могут оказаться эффективными. Компания Gilead Sciences помогает организовать в Китае рандомизированное контролируемое исследование ремдесивира в качестве средства против 2019- nCoV. Другой пример — использование антиретровирусного препарата Kaletra AbbVie (лопинавир/ритонавир) в уханьской больнице.
Исследователи из компании Deargen (Тэджон, Корея), которая занимается поиском мишеней лекарств и дизайном лекарственных молекул с помощью платформы искусственного интеллекта, а также университета Тангук в Чхонане (Корея) и университета Эмори (США) предложили метод прогнозирования активности известных противовирусных препаратов против 2019-nCoV. Результаты опубликованы на сервере препринтов bioRxiv.
Чтобы идентифицировать доступные на рынке лекарства, которые могли бы воздействовать на белки 2019- nCoV, команда использовала свою модель взаимодействия «лекарство-мишень» Molecule Transformer-Drug Target Interaction (MT-DTI), (Подробнее о модели.)
Моделирование определяло константы диссоциации (Kd) для 3С-подобной протеиназы 2019 nCoV и ее потенциальных ингибиторов. 3С-подобная протеиназа — типичный белок коронавирусов и других вирусов с однонитевым (+)-РНК-геномом. Она необходима для процессинга вирусной репликазы (РНК-зависимой РНК-полимеразы), поэтому ее часто рассматривают в качестве мишени противовирусных препаратов.
Наиболее перспективным авторы назвали атазанавир (Reyataz), который применяется для лечения и профилактики ВИЧ-инфекции. Для атазанавира Kd к вирусной протеиназе составила 94,94 нМ, за ним следовали эфавиренц (199,17 нМ), ритонавир (204,05 нМ) и долутегравир (336,91 нМ). Напомним, что Kd измеряется в молях; чем она меньше, тем выше аффинность молекулы ингибитора к белку.
Кроме того, авторы нашли, что атазанавир обладает потенциальной аффинностью к другим белкам вируса: РНК-зависимой РНК-полимеразе (Kd 21,83 нМ), хеликазе (Kd 25,92 нМ), 3'-5'-экзонуклеазе (Kd 82,36 нМ), 2'-O-рибозо-метилтрансферазе (Kd 390 нМ) и эндоРНКазе (Kd 50,32 нМ). Если результаты соответствуют реальности, это значит, что атазанавир способен ингибировать все субъединицы комплекса репликации 2019- nCoV.
Есть и другие интересные находки. Например, для дарунавира и вирусной хеликазы Kd составила 90,38 нМ. Дарунавир и кобицистат входят в состав препарата Prezcobix против ВИЧ от Johnson & Johnson, который компания-производитель недавно отправила в Китай для исследовательских целей. Однако подтверждений его активности против коронавируса хотя бы in vitro пока нет.
Ведущий автор работы Кынсу Кан из университета Тангук ответил на вопросы Genetic Engineering & Biotechnology News (издание специализируется на новостях высокотехнологичной медицины). «Это было просто из научного любопытства: мы хотели посмотреть, может ли наша AI модель предложить какой-либо препарат, который можно использовать против nCoV», — сказал он и отметил также, что в качестве исходных намеренно были выбраны «только те противовирусные препараты, которые доступны на рынке». А уже среди них искали те, у которых значение константы диссоциации с вирусными белками предположительно менее 1000 нМ. Авторы предлагают учитывать список противовирусных препаратов, идентифицированных моделью MT-DTI, при разработке эффективных стратегий лечения 2019-nCoV.
По словам Кана, в настоящее время Deargen не занимается разработкой противовирусных препаратов, но в принципе разработка препарата против 2019-nCoV может быть рассмотрена. У компании есть модель AI для оптимизации/генерации лекарственных молекул, прочно связывающихся с белками-мишенями, под названием MolEQ (molecule equalizer).
Появляются и другие подобные работы. Исследователи из Военно-медицинского университета в Чунцине (Китай) опубликовали на bioRxiv препринт статьи, в которой рассказывается о поиске, также in silico, препаратов, теоретически способных взаимодействовать с протеиназой коронавирусов. Проведя высокопроизводительный скрининг библиотек клинических препаратов, они выбрали четыре молекулы, способных связываться с протеиназой SARS-CoV и при этом не относящихся ни к токсинам, ни к препаратам с особенно сильными побочными эффектами (например, противораковым): синтетический антибиотик и три противовирусных препарата.
Та и другая работы пока не опубликованы в рецензируемых журналах, и очевидно, что компьютерное моделирование не может заменить реальные испытания препарата. Но, возможно, эти результаты ускорят подбор оптимальной стратегии лечения. Очевидно также, что получить разрешение на использование уже разрешенного препарата по другим показаниям намного легче, чем довести до клиники совершенно новый препарат.
Источники
Bo Ram Beck, et al. // Predicting commercially available antiviral drugs that may act on the novel coronavirus (2019-nCoV), Wuhan, China through a drug-target interaction deep learning model. // BioRxiv, 2020; DOI: 10.1101/2020.01.31.929547
Julianna LeMieux. // AI Predicts Coronavirus Vulnerable to HIV’s Atazanavir.


 Меню
Меню





 Все темы
Все темы




 0
0